Iedzimta patogēna noteikšanas stratēģija, kas ietver baktēriju virsmas proteīnu ubikvitināciju, 1. daļa
Jul 28, 2023
IEVADS
Patogēna invāzija izraisa imūnreakciju akumulatoru, ko stimulē saimnieka uzraudzības mehānismi. To parasti ierosina, atpazīstot konservētas mikrobu molekulārās struktūras, kas pazīstamas kā ar patogēniem saistītie molekulārie modeļi (PAMP). Šo PAMP efektīva noteikšana ar modeļa atpazīšanas receptoriem (PRR) ātri izraisa dažādas saimnieka imūnās atbildes, aktivizējot sarežģītus signalizācijas ceļus, kas izraisa patogēna klīrensu.
Pēdējos gados, attīstoties biotehnoloģijai un nepārtraukti pilnveidojoties pētniecības tehnoloģijām, cilvēki padziļināti izprot mikrobu molekulu saistību ar imunitāti. Konservētās mikrobu molekulas ir mikrobu molekulu klase, ko organismi var atpazīt un izraisīt imūnās atbildes. Tie galvenokārt ietver mikroorganismu, piemēram, baktēriju, vīrusu un sēnīšu, molekulāros komponentus, un tie ir ļoti konservēti un specifiski. Pētījumi liecina, ka konservētas mikrobu molekulas spēj pretoties dažādiem patogēniem un uzlabot imunitāti, aktivizējot organisma imūnsistēmu.
Konservētas mikrobu molekulas izraisa iekaisuma un imūnās atbildes reakcijas, aktivizējot svarīgas imūnsistēmas molekulas, piemēram, T šūnas, B šūnas un makrofāgus. Pēc konservētu mikrobu molekulu atpazīšanas šīs šūnas atbrīvos dažādus imūnmediatorus, tostarp citokīnus un kemokīnus, tādējādi piesaistot citas imūnās šūnas, lai pievienotos imūnreakcijai. Tajā pašā laikā konservētas mikrobu molekulas var kalpot arī kā antigēni, lai aktivizētu antivielu reakcijas organismā, tādējādi veidojot antivielu aizsardzību. Šo šūnu un imūno faktoru mijiedarbība var labāk aizsargāt organismu no patogēniem.
Daudzi pētījumi ir parādījuši, ka konservētas mikrobu molekulas var uzlabot organisma imunitāti, tādējādi novēršot un ārstējot dažādas slimības, piemēram, infekcijas slimības, alerģiskas slimības, vēzi utt. Piemēram, plaši izmantotā rekombinantā B hepatīta vakcīna ir izgatavota, pamatojoties uz konservēta mikrobu molekula uz B hepatīta vīrusa virsmas antigēna. Ķermeņa imūnreakciju var izraisīt vakcīnas inokulācija, lai radītu B hepatīta vīrusa virsmas antivielas, lai sasniegtu mērķi novērst B hepatīta vīrusa infekciju.
Noslēgumā jāsaka, ka pastāv cieša saikne starp konservētajām mikrobu molekulām un imunitāti. Pilnībā izmantojot konservēto mikrobu molekulu imūnmodulējošo funkciju, var uzlabot organisma imunitāti, kā arī labāk novērst un ārstēt dažādas slimības. Tāpēc aktīvi jāpievērš uzmanība konservēto mikrobu molekulu lietišķajiem pētījumiem un jāveicina to pielietošana slimību profilaksē un ārstēšanā. No šī viedokļa mums ir jāuzlabo imunitāte. Cistanche var ievērojami uzlabot imunitāti, jo gaļas pelni satur dažādas bioloģiski aktīvas sastāvdaļas, piemēram, polisaharīdus, divas sēnes un Huangli u.c. Šīs sastāvdaļas var stimulēt imūnsistēmu. Dažāda veida šūnas, palielina to imūno aktivitāti.

Noklikšķiniet uz cistanche ieguvumiem veselībai
Līdz šim ir atklātas un raksturotas vairākas PRR klases, piemēram, Toll līdzīgie receptori, retīnskābes inducējamie gēna I (RIG-I) līdzīgi receptori, NOD līdzīgi receptori un DNS receptori (citosola sensori DNS) (1). ). Šie PRR ir gan ārpusšūnu, gan intracelulāro patogēnu atpazīšanas priekšgalā un uztver dažādas molekulu klases mikrobios, tostarp olbaltumvielās, lipīdos, ogļhidrātos un nukleīnskābes (2). Tas ir ļoti svarīgi, lai apturētu slimības progresēšanu un veicinātu saimnieka izdzīvošanu.
Lai saglabātu citozola sterilitāti, ļoti svarīga ir intracelulārās vides uzraudzība patogēnu proliferācijas ierobežošanai. Šādu aizsardzības mehānismu pārkāpums nodrošina patogēnam patvērumu no ārpusšūnu iedzimtas imunitātes un piedāvā iespēju ātri pavairot un izplatīties saimniekorganismā (3). Tāpēc spēcīgi patogēnu noteikšanas mehānismi un šūnu autonomās aizsardzības sistēmas ir būtiskas, lai ierobežotu invazīvos patogēnus. Ubikvitinācija ir viena no stratēģijām, kam ir galvenā loma patogēnu atpazīšanā un izvadīšanā (4).
Degradācijas ceļš, ko nosaka ubikvitinācija, darbojas kā pēdējā robeža pret citozolā mītošajām baktērijām, kuras bieži izvairās no klasiskās endocītiskās nogalināšanas, pārraujot patogēnu saturošas vakuolas, lai iebruktu saimnieka citozolā. Ir identificētas vairākas saimniekorganisma E3 ubikvitīna ligāzes, kas rotā kravas, tostarp intracelulāros patogēnus ar poli-ubikvitīna (Ub) ķēdēm (5), un, lai gan ir atklāti daži baktēriju mērķi, piemēram, ārējās membrānas proteīni (6), joprojām ir plašas zināšanas par substrāta identifikācijas stratēģiju. ierobežots.
Nesen veikts pētījums ir pierādījis, ka izdalītie efektorproteīni satur ar ubikvitīnu saistīto domēnu (UBA) Mycobacterium tuberculosis (Mtb), kas pasīvi piesaista ubikvitīna daļas, galu galā nogādājot patogēnu ar mikrotubuliem saistītā proteīna 1A/1B-vieglās ķēdes 3 (LC3) saistītās autofagosomās. (7). Līdzās neparasti ubikvitīna substrāti, piemēram, lipopolisaharīds (LPS) un glikāns, ir eleganti ilustrēti dažos baktēriju patogēnos, parādot ubikvitinācijas substrātu daudzpusību (8, 9).
Turklāt tika atklāts, ka Rickettsia parkeri aktīvi modificē virsmas proteīnus, aizsargājot tos no ubikvitinācijas un sekojošas nogalināšanas (10). Kopā šie neatkarīgie pētījumi uzsver ubikvitīna substrāta virsmas lokalizācijas nozīmi. Tomēr proteīna substrāta identitāte patogēnā un tas, kā tos varētu precīzi identificēt ar saimnieka E3 ligāzi, joprojām ir nenotverama.
Diezgan daudz saimnieka ubikvitīna ligāžu, piemēram, ar leicīnu bagāts atkārtojums un sterils motīvs, kas satur 1 (LRSAM1), Parkin, zeltneša proteīns 166 (RNF166), RNF213, Ariadne RING-BetweenRING-RING (RBR) E3- Tiek ziņots, ka ubikvitīna proteīna ligāze 1 (ARIH1), SMAD specifiskā E3-ubikvitīna proteīna ligāze 1 (Smurf1) un Skip-Cullin-F-box proteīna 2 saturošais komplekss (SCFFBXO2) rotā patogēnu vai patogēnu saturošas vakuolas. ar dažādām ubikvitīna ķēdes topoloģijām (8, 9, 11-18). Jo īpaši LRSAM1, izmantojot auto-ubikvitināciju, iespējams, rada spēcīgu ubikvitīna signālu ap baktērijām, lai pieņemtu darbā autofagiskās iekārtas (19, 20). Ubikvitīna ligāzes, kas ir atbildīgas par patogēnu marķēšanu, ir iesaistītas arī šūnu homeostāzes uzturēšanā, radot ārkārtīgi taupīgu sistēmu efektīvai un optimālai resursu izmantošanai.
No dažādām ubikvitīna ķēdes topoloģijām, kas veidojas uz patogēna, M1-Ub dekorēšana galvenokārt veicina iekaisuma indukciju (21), savukārt gan K48-, gan K63-Ub ķēdes topoloģijas efektīvi vērš mikrobus pret autofagija vai proteasomāla sistēma, attiecīgi (22). Mēs nesen parādījām, ka K48-Ub ķēdei ir dominējošāks antibakteriālais efekts, salīdzinot ar K63-Ub (23). Parasti šūnu proteīnus, kas paredzēti proteasomu degradācijai, marķē ar K48- Ub ķēdei specifiskām ligāzēm. Kritiskais signāls substrāta atpazīšanai ar šādām ligasēm galvenokārt ir vērsts ar degrona motīvu (24).
Šajā pētījumā mēs identificējam degrona motīvu esamību gan grampozitīvas, gan gramnegatīvas izcelsmes filoģenētiski daudzveidīgu baktēriju virsmas proteīnos. Šādu substrātu mērķēšana, izmantojot ubikvitinācijas mehānismus, veicina efektīvu patogēnu izvadīšanu no saimniekšūnas. Izmantojot to, mēs demonstrējam nenubikvitinējama virsmas proteīna pārvēršanu ubikvitīna substrātā, konstruējot degrona ievietošanu, lai veicinātu baktēriju klīrensu. Šis vienkāršais, bet vispārīgais baktēriju substrātu identificēšanas princips potenciāli kalpo kā konservēts citozola patogēnu atpazīšanas mehānisms, kas sola būt efektīvs un daudzfunkcionāls baktēriju infekciju novēršanā.

REZULTĀTI
K48-Ub ķēde veicina citozola baktēriju patogēnu noteikšanu
Sajūtot patogēnu citozola invāziju, saimnieks tos apzīmēja ar poli-Ub ķēdēm, lai aktivizētu to klīrensu (22). Tā kā šādas poliUb ķēdes galvenokārt sastāv no K48- un K63-Ub, mēs vispirms izpētījām šo ķēžu tipu pārsvaru un telpisko izvietojumu uz diviem filoģenētiski atšķirīgiem patogēniem, Streptococcus pneumoniae (SPN) un Salmonella enterica serovariem. Typhimurium (STM), kas cilvēkiem izraisa attiecīgi pneimoniju un gastroenterītu. Šiem patogēniem ir dokumentēta izdzīvošana un proliferācija saimniekšūnas citozolā (13, 25). Izmantojot ubikvitīna saitei specifiskās antivielas, mēs novērojām, ka ievērojami lielāka intracelulāro baktēriju daļa tika atzīmēta ar K48- Ub ķēdes tipu (~26 procenti SPN un 37 procenti STm) atšķirībā no K63- Ub (1.A att.).
Telpiskās atrašanās vietas analīze ar strukturētās apgaismojuma mikroskopijas (SIM) palīdzību liecināja, ka citozola (bez vakuolu paliekām) vai citosola iedarbībai pakļautās baktērijas (bojātās endosomās) galvenokārt ir saistītas ar K48-Ub, savukārt K63-Ub. signāls atradās uz bojātām endosomām, kas apzīmētas ar Galectin-8 (Gal8; endosomu bojājumu uztveršanas marķieris) (1. att., B līdz E) (26). Attiecīgi aptuveni 99 un ~76 procentos K48-ubikvitināto SPN un STm nebija Gal8 (1. att. F). Baktēriju klātbūtne citozolā tika apstiprināta ar transmisijas elektronu mikroskopiju (TEM) un imūnkrāsošanu ar membrānas marķieri FM4-64 (S1 att., A līdz F). Mēs atklājām, ka attiecīgi 78,4 un 80,4 procenti K48-Ub-pozitīvā SPN un STm ir bez membrānas asociācijas, bet attiecīgi 77,7 un 74,4 procenti K63-Ub-pozitīvā SPN un STm bija ierobežoti. vakuolu (1.G attēls). Kopumā šie atklājumi liecināja, ka baktēriju virsmas pārklāšana ar K48-Ub ķēdēm ir galvenais patogēnu noteikšanas mehānisms, ko saimnieks izmanto citozolā mītošo mikrobu atpazīšanai.
Degron ir vispārējs baktēriju ubikvitinācijas kods
Pēc tam mēs mēģinājām identificēt substrātu K48 ubikvitinācijai uz baktēriju virsmas. Būtiski, ka saimniekorganisma E3 ubikvitīna ligāzes, par kurām ziņots, ka tās ir iesaistītas baktēriju ubikvitinācijā, ir saistītas arī ar būtiskām šūnu funkcijām (12, 14), kur K48-Ub ķēdes darbojas kā galvenais signāls šūnu proteostāzei. Mēs izvirzījām hipotēzi, ka saimnieks var izmantot līdzīgus principus, lai identificētu K48-Ub substrātu uz baktēriju virsmas. Tiek ziņots, ka saimniekolbaltumvielām trīspusēja motīva klātbūtne (primārā degrona secība, kam seko proksimālais lizīna atlikums un nesakārtots reģions starp tām) ir priekšnoteikums K48 ubikvitinācijai (24).
Mēs pārmeklējām SPN virsmas proteīnus līdzīgu pazīmju klātbūtnei (1. att. H), identificējot BgaA un PspA kā iespējamos ubikvitinācijas mērķus (1. att. un S2, A un B att.). BgaA ir -galaktozidāze, par kuru ziņots, ka tā darbojas kā SPN adhezīns, savukārt PspA ir holīnu saistošs proteīns, kas saistās ar laktoferīnu un ir nepieciešams komplementa izvairīšanai (27, 28). Mēs novērojām K48-Ub ķēdes tipa saistību samazināšanos par ~50 līdz 53 procentiem gan ΔbgaA, gan ΔpspA mutantiem, neizmainot K63-Ub līmeni (1. att.). Šis samazinājums bija izteikts (~ 75 procenti) dubultā izsituma celmā (ΔbgaAΔpspA), kas liecina par šo ubikvitīna substrātu nederīgo raksturu (1. att. I).
Turklāt BgaA-T (proteīna saīsināta versija, kas sastāv no 1. līdz 1049. aminoskābēm) un PspA ekspresija saimniekšūnās noved pie to ubikvitinācijas ar K48-Ub topoloģiju (1. zīm.). Paredzēto mērķu derīgums tika apstiprināts ar komplementāciju, un modelis tika nostiprināts, izmantojot ΔhysA (SPN virsmas proteīna, kas neatbilst trīspusējā degrona kritērijiem) mutantu kā kontroli, lai novērtētu K48-Ub asociācijas līmeņus (1. att. ).
Tālāk mēs pētījām K48-Ub dekorācijas ietekmi uz baktēriju izvadīšanu.
K48-Ub substrātu trūkums kavēja baktēriju klīrensu, kā rezultātā ievērojami uzlabojās abu mutantu SPN celmu intracelulārā noturība (~18- reizes ΔbgaA un ~2- reizes ΔpspA) ( 1.K att.). Mūsu substrāta prognozēšanas pieejas universālums tika apstiprināts, identificējot vairākus uz virsmas pakļautus proteīnus dažādos citos patogēnos kā iespējamos substrātus ubikvitinācijai (S1 tabula). Viens no šādiem iespējamiem kandidātiem, ārējās membrānas proteīns RlpA uz STm tika apstiprināts kā saimnieka ubikvitinācijas iekārtas mērķis, jo ΔrlpA mutantam bija ~15- reizes mazāka saistība ar K48-Ub, salīdzinot ar savvaļas proteīnu. -tipa (WT) STm (1L att.). Šis atklājums noteica mūsu substrāta atlases stratēģijas plašo pielietojamību. Cik mums ir zināms, šie ir pirmie baktēriju virsmas proteīni, par kuriem ziņots, ka saimnieka ubikvitinācijas iekārta ir atpazinusi patogēnu noteikšanai un attīrīšanai.
Trīspusējs motīvs ir priekšnoteikums precīzai baktēriju virsmas proteīnu ubikvitīnai marķēšanai

Pēc substrāta identifikācijas mēs centāmies pārbaudīt trīspusējā motīva kritiskās iezīmes, kas veidoja mūsu ekrāna mugurkaulu (2. att. un S2 att.). Degrona sekvences (102VTPKEE107) dzēšana BgaA-T izraisīja K48-Ub ķēdes tipa asociācijas samazināšanos par ~50 procentiem, salīdzinot ar WT SPN, neatkarīgi no līdzīgas augšanas kinētikas un šūnu adhēzijas spējas (2. att. un S3, A un B att.). Šis samazinājums bija salīdzināms ar ΔbgaA knockout celmu, apstiprinot degronam raksturīgo fenotipu. Neatkarīgi no degrona secības, lizīna atlikums tiešā tuvumā ir būtisks ubikvitīna daļas pievienošanai substrātam. BgaA gadījumā degronu secību papildina divas proksimālās ievērojami samazinātas K48 ubikvitinācijas, salīdzinot ar BgaA-T (2. att. D). Proti, iespēja, ka BgaA-TΔDegron proteīnā varētu būt nopietnas konformācijas izmaiņas, kas ietekmēs ubikvitināciju, tika atcelta, izmantojot attīrīta BgaA-TΔDegron proteīna in silico prognozēšanu un cirkulārā dihroisma (CD) spektroskopiju, kas uzrādīja līdzīgus strukturālos parakstus kā BgaA-T (att. S3, C un D). Tāpat kā BgaA, degrona sekvences (327PETPAPE333) dzēšana un lizīna mutācija (K315R) PspA arī izraisīja ievērojami samazinātu K48-Ub asociāciju kopā ar ilgstošu izdzīvošanas spēju (S4. att., A līdz D).


Pēc tam mēs izstrādājām SPN virsmas proteīnu HysA, kuram sākotnēji trūka primārās degrona sekvences, pievienojot degronu sekvenci strukturāli nesakārtotā proteīna reģionā, kas satur lizīna atlikumu (2. att., F un G, un S2., C. att.). uz E). Šī modifikācija nodrošināja iepriekš nenubikvitinējamā HysA proteīna atpazīšanu un K48 ubikvitināciju. K48-Ub asociācijas līmeņi SPN celmiem, kas satur inženierijas ceļā izveidoto HysA proteīnu (ΔbgaA:pHysADegron-BgaA un ΔpspA:pHysADegron-PspA), bija 2.2- un 3.2-reizes augstāki, salīdzinot ar vai nu ΔbgaA un ΔbgaA: attiecīgi pHysA vai ΔpspA celmi (2H att.).
Uzlabotā ΔbgaA:pHysADegron-BgaA un ΔpspA:pHysADegron-PspA celmu dekorēšana ar K48-Ub atņēma SPN izdzīvošanas pieaugumu, ko nodrošināja degrona trūkums ΔbgaA un ΔbgaA: pHysA vai Δpsp2I (Fig.pspA). Visi izstrādātie SPN celmi radīja līdzīgus poras veidojošā toksīna pneimolizīna (Ply) līmeņus (2. att., B un G), kas ir priekšnoteikums endomembrānas bojājumiem un tai sekojošai ubikvitinācijai (25). Tas novērš iespējamo zemu vai plašu membrānas bojājumu ieguldījumu, veicinot ievērojamas ubikvitinācijas līmeņa izmaiņas mutantu SPN celmos. Kopumā tie liecina, ka mākslīga degrona sekvences pievienošana veicina ubikvitīna izraisītu patogēnu noteikšanu un likvidēšanu. Proti, degrona secība BgaA bija ļoti konservēta dažādos pneimokoku serotipos (S5A att.).
Tomēr 19F serotipa gadījumā, kas bieži ir saistīts ar paaugstinātu nāves risku no bakterēmiskās pneimonijas un sepses (29–31), tika konstatēts, ka primārais degrons ir mutēts (P104Q). Mēs novērojām, ka šīs mutācijas atdarināšana BgaA (S5B att.) izraisīja sliktu ubikvitināciju un uzlaboja ΔbgaA: pBgaA-TP104Q izdzīvošanas spēju, salīdzinot ar ΔbgaA: pBgaA-T (S5, C un D att.). Tas izceļ degrona atpazīšanu kā stratēģiju, ko saimnieks izmanto, lai aizsargātu sevi pret smagām bakteriālām infekcijām.
SCFFBW7 ir pretmikrobu E3 ubikvitīna ligāze
Paredzams, ka atlasītajos ubikvitīna substrātos esošo kanonisko degronu secību identificēs SCFFBW7 E3 ubikvitīna ligāzes komplekss (24), kas ir iesaistīts šūnu cikla un augšanas regulēšanā (32). Tas sastāv no diviem konservētiem proteīniem, ar S-fāzes kināzi saistītā proteīna 1 (SKP1) un Cullin proteīnu saimes locekļa, kā arī mainīga F-box proteīna, kas nodrošina substrāta specifiku (33). Lai pārbaudītu SCFFBW7 iesaistīšanos SPN ubikvitinācijā, mēs vispirms novērtējām FBXW7 saistību ar SPN. Imunofluorescences analīzē mēs atklājām, ka ~ 31 procents intracelulāro SPN ir saistīts ar FBXW7 (3. att. un S6. att.). Paredzams, ka FBXW{16}}pozitīvais SPN arī tika kolokalizēts ar K48 ubikvitīnu (S6B attēls). Lai pierādītu SCFFBW7 iesaistīšanos, baktēriju marķēšana ar K48-Ub ķēdēm tika pārbaudīta ar imunofluorescenci pēc Cullin1, SKP1 un FBXW7 gēnu ekspresijas pazemināšanas, izmantojot mērķtiecīgas mazas traucējošas RNS (siRNS; att.). S7, A līdz C).
Jo īpaši FBXW7 klusēšana tika apstiprināta ar ciklīna E1 uzkrāšanās līmeni siFBXW 7- apstrādātajās šūnās (S7F attēls). Mēs novērojām SPN saistību ar K48-Ub samazināšanos par aptuveni 45 līdz 60 procentiem Cullin1, SKP1 un FBXW7 notriekšanas šūnās (3.B att.), kas savukārt izraisīja ~1.{12}} līdz. 1.{14}}kārtīgs SPN noturības pieaugums saimniekšūnās (3. E attēls). SCFFBW7 specifiskā degrona motīva mērķēšana tika pierādīta ar nemainīgām atšķirībām K48-Ub kolokalizēšanā un ΔpspAΔbgaA un ΔbgaA:pBgaA-TΔDegron celmu izdzīvošanas spējās siFBXW{19}}treated S8 šūnās. D). Šie atklājumi tika pamatoti ar ievērojamu BgaA-T K48 ubikvitinācijas samazināšanos saimniekšūnās pēc FBXW7 notriekšanas (3. att. C).
Turklāt in vitro ubikvitinācija ar attīrītu BgaA-T (att. S9, A līdz D) un SCF kompleksa komponentiem nepārprotami parāda SCFFBW7 kā bona fide E3 ligāzi, kas ir atbildīga par BgaA ubikvitināciju. Rekombinantā SCFFBW7 spēja ubikvitināt attīrītu BgaA-T, bet nespēja ubikvitināt ar degronu dzēsto variantu BgaA-TΔDegron vai lizīna-arginīna aizstāšanas variantu BgaA-TK97R (3. att.). Turklāt saimniekšūnām, kas ekspresē FBXW7R505C variantu, kuram ir traucēta ciklīna E1 (FBXW7 substrāts) atpazīšanas spēja (S7E att.), tika novērota samazināta (~50 procenti) SPN K48 ubikvitinācija, kā arī ~2- reizes. augstāka SPN izdzīvošana, salīdzinot ar WT šūnām (3. att., F un G). Šie eksperimenti pierāda SCFFBW7 E3 ligāzes galveno lomu citozolā mītošu patogēnu noteikšanā un mērķtiecībā uz to nogalināšanas ceļiem.
GSK3 -mediētā degrona motīva fosforilācija pastiprina SCFFBW7 pretmikrobu aktivitāti
Kopumā F-box proteīni atpazīst fosforilētus substrātus, lai veicinātu to ubikvitināciju (34). Tāpēc mēs pētījām baktēriju substrātu fosforilēšanās iespējamību un ietekmi uz patogēna K48-Ub pārklājumu. Bioinformātikas analīze atklāja iespējamu fosforilējamo treonīna atlikumu (102VT * PKEE107) BgaA degrona secībā. Mēs novērojām, ka SPN celmam, kurā ir BgaA-TT103A mutācija (ΔbgaA:pBgaA-TT103A) (4.A att.), ir par 71% mazāka kolokalizācija ar K48-Ub, salīdzinot ar WT (4.B attēls), atklājot fosforilācija substrāta atpazīšanā ar SCF kompleksu.
Kritiski ir tas, ka samazinātā BgaA fosforilēšanās tendence ΔbgaA:pBgaA-TT103A atcēla saimnieka spēju novērst intracelulāro baktēriju slodzi (~1{3}} reizes) (4. att. C). Paralēli BgaA PspA degrona variants (ΔpspA:pPspAT329A) arī uzrādīja K48-Ub kolokalizācijas samazināšanos par 51%, kas bija saistīta ar ilgstošu intracelulāro noturību (S10. att., A līdz C). Parasti SCFFBW7 mērķa substrātiem ir treonīns/serīns (T/S*) blakus prolīna atlikumam, ko fosforilē uz prolīnu vērsta proteīnkināze GSK3 (35–37). Tāpēc mēs mēģinājām noskaidrot GSK3 iesaistīšanos substrāta atpazīšanas palielināšanā.
Vispirms mēs parādījām, ka GSK3 ir cieši saistīts ar ubikvitinātu SPN, kas apzīmēts ar FBXW7 (4. att., D un E). Pēc tam, veicot in vitro kināzes testu, mēs novērojām, ka GSK3 var fosforilēt rekombinanto BgaA-T. Tajā pašā laikā BgaA-TT103A variants palika nefosforilēts (4. F. attēls). Tas apstiprināja treonīna atlikuma identitāti BgaA-T degronu secībā kā GSK3 -mediētās fosforilācijas mērķi. Mērķtiecīga GSK3 notriekšana ar siRNS (S7D att.) izraisīja SPN K48 ubikvitinācijas samazināšanos par ~ 58 procentiem (4.G att.). Šī samazinātā ubikvitinācija pēc GSK3 ekspresijas regulēšanas samazināja saimniekorganisma spēju attīrīt šūnās iebrukušos patogēnus (~1{19}} reizes) (4H attēls), taču neuzrādīja nekādu ietekmi uz ΔbgaA. : pBgaA-TT103A (S8, E un F att.). Kopumā tas sniedz pirmos pierādījumus par saimniekkināzi, īpaši GSK3, kas regulē baktēriju virsmas proteīnu ubikvitināciju efektīvai patogēnu attīrīšanai (4. att.).

Citozolisko patogēnu ubikvitinācija piešķir atšķirīgus likteņus to likvidēšanai. Jo īpaši K48 ubikvitinācija veicina substrātu mērķēšanu uz proteasomām (22). Tāpat mūsu rezultāti liecina par ubikvitināta SPN saistību ar proteasomu apakšvienību 7 (S11, A un C att.). Turklāt proteasomu inhibīcija ar MG132 ārstēšanu uzlabo WT SPN noturību, bet nemaina ΔpspAΔbgaA izdzīvošanas spēju. Līdzīgi fenotipi tika novēroti STm un ΔrlpA mutantu gadījumā (att. S11, B un D).
Patogēna uzraudzība, ko vada degrons, aizsargā saimniekorganismu no sepses
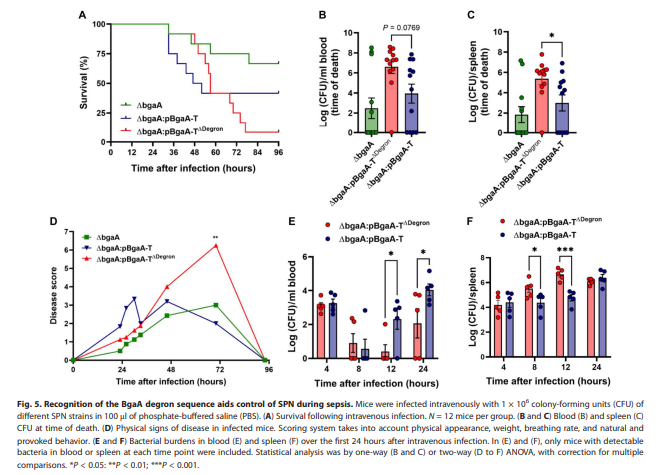
Pēc tam mēs centāmies noteikt SPN atpazīšanas ietekmi, izmantojot šūnu ubikvitinācijas mehānismu, uz infekcijas rezultātiem. Izmantojot izveidoto SPN sepses modeli (38), mēs salīdzinājām ΔbgaA mutanta virulenci ar WT SPN virulenci, kā arī celmiem, kas papildināti ar BgaA-T (ΔbgaA: pBgaA-T) vai versiju, kurai trūkst degrona sekvences ( ΔbgaA:pBgaA-TΔDegron). Saskaņā ar iepriekšējiem ziņojumiem (39) bgaA dzēšanas celms uzrādīja novājinātu virulenci, savukārt peles, kas bija inficētas ar WT, ΔbgaA:pBgaA-T vai ΔbgaA: BgaA-TΔDegron, pakļāvās infekcijai (5.A attēls un S12 attēls, A līdz D). . Tomēr peļu grupai, kas bija inficēta ar SPN celmu, kurai nebija degrona secības, bija lielāks nāves gadījumu īpatsvars, bet ar aizkavētu mirstību, salīdzinot ar ΔbgaA:pBgaA-T inficēto grupu (P=0.0492, log-rank tests) (5.A att.). Baktēriju daudzuma asinīs (5.B att.) un liesā (5.C att.) un redzamo slimības pazīmju laika gaita inficētām pelēm (5.D att.) salīdzinājums apstiprināja ΔbgaA:pBgaATΔDegron celma virulences palielināšanās tendenci.

Iepriekšējie pētījumi ir parādījuši, ka SPN sepse tiek noteikta no baktēriju rezervuāra liesā (38). Lai gan pirmo iebrukušo baktēriju vilni cirkulācijā ātri iztīra saimniekorganisma iedzimtie imūnmehānismi, daļa SPN izdzīvo un vairojas liesas makrofāgos pirms atkārtotas iesēšanas asinīs. Mēs izvirzījām hipotēzi, ka aizkavēta smagas slimības rašanās pelēm, kas inficētas ar ΔbgaA: pBgaA-TΔDegron, varētu būt ilgstošas SPN izdzīvošanas rezultāts liesas makrofāgos, jo saimnieka ubikvitinācijas iekārta samazina baktēriju intracelulāro atpazīšanu. Lai to pamatotu, mēs novērojām aizkavētu otrā bakterēmijas viļņa sākšanos pelēm, kas bija inficētas ar ΔbgaA:pBgaA TΔDegron celmu, salīdzinot ar ΔbgaA:pBgaA-T (24 stundas pret 12 stundām), pēc agrīnas klīrensa fāzes (att. 5E).
Tomēr aptumsuma fāzē, kuras laikā baktērijas tiek iztīrītas no asinīm, liesas baktēriju skaits bija konsekventi lielāks ΔbgaA: pBgaA-TΔDegron inficētām pelēm (5. att. F). Šie atklājumi liecina, ka SPN izplatīšanās fāze liesas makrofāgos tiek pagarināta, ja nav intracelulāras infekcijas atpazīšanas, izmantojot ubikvitinācijas mehānismu. Tā rezultātā palielināts baktēriju blīvums var uzkrāties liesā (5. att. F), pēc tam iesējot asinīs lielākā skaitā, kas var izraisīt aizkavētu, bet palielinātu ΔbgaA: pBgaA-TΔDegron inficēto peļu mirstību. Kopā šie dati parāda, ka intracelulārā SPN atpazīšana un ubikvitinācija veicina patogēnu kontroli sepses laikā.

For more information:1950477648nn@gmail.com
