Aknu kināzes B1 (LKB1) prognostiskā vērtība ar kuņģa vēzi saistītu audzēju mikrovides imunitātē
Dec 14, 2023
Abstract:
Aknu kināze B1 (LKB1) ir audzēja supresora gēns, kura inaktivācija bieži notiek dažādos audzēju veidos. Tomēr nav zināms, vai LKB1 ir saistīts ar kuņģa vēža (GC) klīniskajām pazīmēm un regulē audzēja imunitāti. Šajā pētījumā mēs parādījām, ka LKB1 ir ļoti izteikts veselu indivīdu serumā (n = 176), salīdzinot ar GC pacientiem (n = 416), un tas ir saistīts arī ar klīniskiem rezultātiem un labiem izdzīvošanas rādītājiem GC pacientiem. Turklāt gēni, kas saistīti ar imūnsistēmas kontrolpunktiem un T šūnu aktivāciju, piemēram, PD−1, PD−Tika pierādīts, ka L1, CD8A, CD8B, CD28 un GZMM ir ļoti izteikti GC apakšgrupās ar augstu LKB1 ekspresiju. Salīdzinot ar svaigiem kuņģa vēža audiem, LKB1 bija izteikti ekspresēts CD3+CD8+ un CD3+CD8+CD28+ T šūnās svaigās blakus esošajās ne- vēža audi. CD3+CD8+ T šūnas ražoja IFN−anti−vēža imūnreakcija. Turklāt CD3+CD8+ T šūnu daļai, kas ekspresēja LKB, bija pozitīva korelācija ar IFN−izteiksme. Turklāt GC pacientiem ar zemu LKB1 ekspresiju, ārstējot ar pembrolizumabu, bija vājš objektīvās atbildes reakcijas līmenis un sliktāka dzīvildze bez slimības progresēšanas un kopējā dzīvildze. Visbeidzot, LKB1 var būt potenciāls imūnsistēmas kontrolpunkts GC pacientiem.

Cistanche tubulosa-Antitumor priekšrocības
Atslēgvārdi:
LKB1; kuņģa vēzis; klīniskie rezultāti; imunitātes kontrolpunkts; CD3+CD8+ T šūnas
1. Ievads
Visā pasaulē kuņģa vēzis (GC) ir sabiedrības veselības problēma un ir piektais visbiežāk diagnosticētais ļaundabīgais audzējs [1,2]. Lai gan klīniskajā praksē plaši tiek izmantotas parastās GC ārstēšanas metodes, piemēram, kuņģa rezekcija, ķīmijterapija, staru terapija un mērķterapija [3], 5−gada izdzīvošanas rādītājs progresējošas GC ir < 20%. Pateicoties GC terapijas progresam [4,5], imūnterapija tiek uzskatīta par inovatīvu pieeju [6], kas ir izskaidrojusi šīs slimības ārstēšanu [7]. Imūnterapijas laikmetā ieprogrammēta šūnu nāve 1 (PD−1)/PD−ligands 1 (PD−Ir pierādīts, ka L1) ir biomarķieris vēža diagnostikai un reakcijas uz imūnterapiju prognozēšanai, taču tas nav pietiekami jutīgs. Tāpēc ir svarīgi identificēt jaunus prognozējošus biomarķierus GC imūnterapijā.
Aknu kināze B1 (LKB1), kas pazīstama arī kā STK11, ir serīna/treonīna kināze, kas plaši sastopama daudzos audos [8]. Arvien vairāk pierādījumu liecina, ka LKB1 ir galvenais audzēju nomācējs vairāku veidu vēža gadījumos, piemēram, aizkuņģa dziedzera vēzis [9], melanoma [10,11]−sīkšūnu plaušu vēzis [12,13] un dzemdes kakla vēzis [14]. Turklāt ir zināms, ka LKB1 ir iesaistīts imūno šūnu funkciju regulēšanā [10]. LKB1 deficīts T šūnās veicina kuņģa-zarnu trakta polipozes attīstību [15] un ietver arī IL−11−JAK/STAT3 ceļš, kas noved pie kuņģa-zarnu trakta audzēja ģenēzes [16]. Turklāt LKB1 ir būtiska loma makrofāgu funkcijā, piedaloties tādos procesos kā šūnu augšana, metabolisms un polarizācija [17]. Jaunākie pētījumi liecina, ka LKB1 zudums var būt saistīts ar audzēja imūnās mikrovides modulāciju [18]. Konkrēti, LKB1 deficīts nomāc T−šūnu aktivitāti, veicinot proinflammatorisku citokīnu veidošanos un neitrofilu piesaisti audzēja mikrovidē pacientiem ar plaušu vēzi [19]. Ierobežots skaits pētījumu ir noskaidrojuši saistību starp LKB1 ekspresiju, klīniskajiem rezultātiem, imūnsistēmu un terapeitisko reakciju GC. Šajā pētījumā mēs parādījām saistību starp LKB1 ekspresiju un klīniskajiem rezultātiem GC pacientiem. Turklāt mēs parādījām, ka zema LKB1 ekspresija veicina imūnsupresīvu mikrovidi un var izraisīt sliktu GC pacientu prognozi. Turklāt GC pacienti ar augstu LKB1 ekspresiju saņēma lielākus ieguvumus no ārstēšanas ar pembrolizumabu. Šeit ir apskatīta LKB1 prognostiskā vērtība un iespējamā loma audzēja imunoloģijā, un tā var palīdzēt izprast iespējamo GC pamatā esošo mehānismu.

cistanche tubulosa-uzlabo imūnsistēmu
2. Materiāli un metodes
2.1. Pacienti un asins paraugi
Šo retrospektīvo pētījumu apstiprināja Džedzjanas vēža slimnīcas vietējā ētikas komiteja (IRB−2021−154). Mēs savācām asins paraugus no 176 veseliem pieaugušajiem un 416 GC pacientiem no 2015. gada janvāra līdz 2022. gada augustam un savācām 26 pārus svaigu vēža audu un blakus esošo nevēža audu no 26 GC pacientiem. Pacienti ar citiem ļaundabīgiem audzējiem anamnēzē tika izslēgti.
2.2. CEA, CA19-9, AFP un LKB1 izteiksme
Lai novērtētu LKB1 ekspresijas līmeni plazmas paraugos saskaņā ar standartizētu protokolu, tika izmantots komerciāls ELISA testa komplekts (RX106671H; Ruixinbio, Quanzhou, Fujian, Ķīna). Īsumā, attiecīgie plazmas paraugi (50 µL) un standarta modeļa proteīni (50 µL) tika pievienoti 96 iedobju plāksnēm. Pēc tam tika pievienoti 100 µL ar HRP iezīmētas antivielas un 96 iedobju plāksnes inkubēja 1 stundu 37 ◦C temperatūrā. Pēc tam plāksnes trīs reizes nomazgāja ar mazgāšanas buferi. Tika pievienots substrāta maisījums (100 µL) un plāksnes tika analizētas mikroplašu lasītājā pie OD 450. CEA (CFDA 20163402679, Siemens Healthcare Diagnostic Products., Šanhaja, Ķīna), CA19-9 (CFDA 20173,017) noteikšanai tika izmantota hemiluminescence. Siemens Healthcare Diagnostic Products., Šanhaja, Ķīna), un AFP izteiksme (CFDA 20173400053, Siemens Healthcare Diagnostic Products., Šanhaja, Ķīna). SPSS 19.0 programmatūra (IBM, Armonk, NY, ASV) tika izmantota, lai noteiktu laukumu zem CEA, CA19-9, AFP un LKB1 uztvērēja darbības raksturlīknēm (ROC). Pamatojoties uz TNM patoloģisko stadiju, FIGO stadiju un HER2 ekspresiju, 416 GC pacienti tika sadalīti dažādās apakšgrupās. Lai analizētu LKB1 ekspresiju dažādās GC pacientu apakšgrupās, tika izmantots pāra t-tests.
2.3. LKB1 ekspresijas analīze imūnās šūnās un saistība ar imūnsistēmas kontrolpunktiem
Visaptveroša analīze par imūnterapijas multi-omikas pan-vēža gadījumā [CAMOIP] (http://www.camoip.net/) (piekļuva 1. janvārī, 2. janvārī{{10}}23) ir analīzes rīks. ekspresijas un mutāciju dati no vēža genoma analīzes (TCGA) un imūnās kontrolpunkta inhibitora (ICI) apstrādātajiem projektiem. Lai analizētu imunogenitāti un ceļa bagātināšanu GC pacientiem, tika izmantots standarta apstrādes cauruļvads. CAMOIP tika izmantots arī, lai analizētu dažādas imūno šūnu ekspresijas atbilstoši LKB1 ekspresijai GC pacientiem. UCSC Xena datubāze (https://xena.ucsc.edu/public) (piekļuva 2023. gada 1. janvārī) ir vēža genomikas datu analīzes platforma, kas atbalsta vairāku vēža paraugu histoloģisko datu vizualizāciju un analīzi. UCSC Xena datu bāze nodrošina LKB1, T-šūnu imūnās kontrolpunkta gēnus, T-šūnu aktivāciju un mRNS ekspresijas antigēna prezentāciju. Sarežģīta siltuma karte tika izveidota, izmantojot R valodu (4.2.1.). Lai analizētu LKB1 izteiksmi, pamatojoties uz kvartilēm, tika izmantota programmatūra SPSS 19.0 (IBM, Armonk, NY, ASV). Mēs sadalījām GC pacientus LKB1 augstas un zemas ekspresijas grupās atbilstoši LKB1 ekspresijas starpvērtībai. T-tests tika izmantots, lai analizētu T-šūnu imūnās kontrolpunkta gēnus, T-šūnu aktivāciju un mRNS ekspresijas antigēnu prezentāciju GC pacientiem LKB1 augstas un zemas ekspresijas GC pacientu apakšgrupās. p vērtības < 0,001 tika uzskatītas par statistiski nozīmīgām.

Cistanche tubulosa-Antitumor priekšrocības
2.4. Plūsmas citometrija
Svaigi vēža (n {0}}) un svaigi blakus esošie nevēža audi (n=26), kas iegūti intraoperatīvi, tika samalti audu malšanas šķīdumā 30 minūšu laikā. Malšanas šķīdums un perifēro asiņu mononukleārās šūnas (PBMC) (1 × 106 šūnas/ml) tika savāktas ar fosfātu buferšķīdumā (PBS) (50 µL, CR20012; Zhejiang Crenry, Džedzjana, Ķīna), kas papildināts ar 0,5% liellopu seruma albumīna (BSA) (Thermo Fisher, Waltham, MA, ASV) un inkubēja ar anti-cilvēka monoklonālajām antivielām 15 minūtes. Tika izmantotas anti-cilvēka monoklonālās antivielas, kā parādīts 1. tabulā un S1 papildu tabulā un S1 papildu attēlā: anti-LKB1 (PTG, Uhaņa, Hubei, Ķīna); anti-CD68 (Biolegend, Sandjego, Kalifornija, ASV); anti-CD209 (Biolegend, Sandjego, Kalifornija, ASV); anti-CD28 (Biolegend, Sandjego, Kalifornija, ASV); anti-CD45/CD56/CD19 (Beckman Coulter, Sentluisa, MO, ASV); anti-CD45/CD4/CD8/CD3 (Beckman Coulter, St. Louis, MO, ASV); anti-CD4, CD3 (Beckman Coulter, St. Louis, MO, ASV); anti-CD45RO (Beckman Coulter, Sentluisa, MO, ASV); anti-CD8 (Beckman Coulter, Sentluisa, MO, ASV); anti-CD38 (Beckman Coulter, Sentluisa, MO, ASV); un anti-CD45RA (Beckman Coulter, Sentluisa, MO, ASV). CD3/CD4/CD8/CD28/PD−1 noteikšanas komplekts tika iegādāts no uzņēmuma Raise Care (Hangžou, Ķīna). Rezultātu analīzei tika izmantota CXP analīzes programmatūra un plūsmas citometrs Beckman Coulter FC 500 [20,21]. Citokīnu noteikšanai plazmas paraugos no GC pacientiem tika izmantots citokīnu noteikšanas komplekts (Seager, Dalian, Ķīna) saskaņā ar ražotāja norādījumiem.
1. tabula. GC pacientu un veselu indivīdu ar klīniskajiem parametriem salīdzinājums.

2.5. Imūno šūnu proporcijas svaigos audos
T-tests tika izmantots, lai analizētu imūno šūnu proporcijas svaigos vēža audos (n=26) un svaigos blakus esošajos ne-vēža audos (n=26). Atšķirība starp LKB1+ un PD1+LKB1+ imūno šūnu proporcijām svaigos vēža un svaigos blakus nevēža audos tika analizēta, izmantojot pāra t-testu. SPSS 19.0 programmatūra (IBM, Armonk, NY, ASV) tika izmantota, lai noteiktu korelāciju starp imūno šūnu proporcijām un citokīniem svaigos vēža audos un svaigos blakus esošos nevēža audos.
2.6. Audu imūnhistoķīmija (IHC)
Zhejiang Cancer Hospital Biobank nodrošināja svaigus vēža (n=26) un svaigus blakus esošos audus, kas nav vēža audi (n=26), kas tika izmantoti šajā pētījumā. Lai veiktu IHC saskaņā ar ražotāja norādījumiem, tika izmantots IHC komplekts (Beijing Zhongshan Golden Bridge Biotechnology Co., Ltd., Pekina, Ķīna). Īsumā, parafīna sekcijas tika secīgi deparafinētas, rehidrētas un vārītas antigēna iegūšanai. Primārā LKB1 antiviela (IPB0924 [atšķaidījuma attiecība, 1:100]; Baijia, Taizhou, Jiangsu, Ķīna) un gamma interferona (IFN−) antiviela (IPB0703 [atšķaidījuma attiecība, 1:100]); Baijia, Taizhou, Jiangsu, Ķīna) tika inkubēti 2 stundas istabas temperatūrā. Sekcijas trīs reizes mazgāja ar PBS. Parafīna sekcijām 20 minūtes pievienoja histoķīmisko polimēra pastiprinātāju (400 µL), kam sekoja 3 mazgāšana ar PBS. Pēc tam parafīna sekcijām tika pievienotas sekundārās antivielas un inkubētas 20 minūtes, kam sekoja mazgāšana, DAB krāsošana, pretkrāsošana un montāža.
2.7. GC pacientu ārstēšanas reakcija uz pembrolizumabu, pamatojoties uz LKB1 ekspresiju
Ārstēšanas reakcija uz pembrolizumabu un klīniskie dati par GC pacientiem, kuriem tiek veikta imūnās kontrolpunkta blokāde (ICB), tika iegūti no iepriekšējā ziņojuma [22]. SPSS 19.0 programmatūra (IBM, Armonk, NY, ASV) tika izmantota, lai analizētu LKB1 izteiksmi, pamatojoties uz kvartilēm. Mēs sadalījām GC pacientus LKB1 augstas un zemas ekspresijas grupās atbilstoši LKB1 ekspresijas starpvērtībai. R valoda (4.2.1) tika izmantota, lai noteiktu GC pacientu atbildes reakciju uz ārstēšanu ar pembrolizumabu atbilstoši LKB1 ekspresijai. PD−L1 izpausme tika analizēta, izmantojot SPSS 19.{12}} programmatūru (IBM, Armonk, NY, ASV), pamatojoties uz kvartilēm. GC pacienti tika sadalīti PD−L1 augstas un zemas ekspresijas grupās atbilstoši starpvērtībai. Pamatojoties uz LKB1 un PD−L1 ekspresiju, GC pacienti tika iedalīti LKB1 augsta un zema PD−L1 augstas un zemas ekspresijas apakšgrupās, un Python tika izmantots, lai atspoguļotu pembrolizumaba ārstēšanas reakciju apakšgrupās. Ar pembrolizumabu ārstēto GC pacientu kopējā dzīvildze un dzīvildze bez slimības progresēšanas tika analizēta, izmantojot Kaplan-Meier metodi ar log-rank testu.
2.8. Statistiskā analīze
Statistiskās analīzes tika veiktas, izmantojot SPSS 19.{1}} programmatūru (IBM, Armonk, NY, ASV). Pacientu dzīvildze tika apstiprināta pa tālruni un tika analizēta, izmantojot Kaplan-Meier metodi ar log-rank testu. p vērtības < 0,05 tika uzskatītas par statistiski nozīmīgām. Turklāt, lai apstiprinātu LKB1 (augsta vai zema ekspresija) ietekmi uz GC pacientu izdzīvošanu, tika izmantots Kaplan−Meier Plotter (http://www.kmplot.com) (piekļuvis 2023. gada 1. janvārī). Python tika izmantots, lai atspoguļotu GC pacientu klīniskās pazīmes un parametrus.
3. Rezultāti
3.1. Asociācija starp LKB1 ekspresiju un klīnikas funkcijām GC pacientiem
Šajā pētījumā tika iekļauti 416 GC pacienti (268 vīrieši un 148 sievietes) un 176 veseli indivīdi (87 vīrieši un 89 sievietes). Veselu indivīdu un GC pacientu raksturojums ir apkopots 1.A attēlā un 1. tabulā. Ir apkopoti GC pacientu klīniskie rezultāti, tostarp CEA, CA19-9, AFP un HER2 ekspresija, patoloģiskā pakāpe, Starptautiskā vēža kontroles savienība (UICC). ) audzēja stadija, limfmezglu iesaistīšanās un attālās metastāzes (1.B attēls, 1. un 2. tabula). Kā parādīts 1.C attēlā, CEA, CA19-9 un AFP bija ļoti izteikti GC pacientu serumā, savukārt LKB1 bija ļoti izteikti veseliem indivīdiem. Salīdzinājumā ar CEA, CA19-9 un AFP, LKB1 bija vislabākā specifika un jutība (AUC=0.727; 1.D attēls). Starp klīniskajiem parametriem LKB1 bija ievērojami zemāks T3–4, N2–3, M1 un III–IV stadijā saskaņā ar UICC stadijas kritērijiem (p < {{30}}.0 5, p < 0,05, p < 0,001 un p < 0,01, attiecīgi; 1. E attēls un 2. tabula). Turklāt LKB1 bija skaitliski izteikti izteikti HER2-negatīviem GC pacientiem (1. attēls F). Tādējādi šie rezultāti liecināja, ka LKB1 ir potenciāli iesaistīts GC progresēšanā.

1. attēls. LKB1 ekspresijas un klīnisko raksturojumu attiecības. (A, B), Klīniskās pazīmes veseliem indivīdiem (n=176) un GC pacientiem (n=416) tika kartētas, izmantojot Python. (C), CEA, CA19-9 un AFP ekspresija tika mērīta GC pacientu un veselu indivīdu serumā. (D), Salīdzinot ar CEA, CA19-9 un AFP, LKB1 bija augstāka jutība un specifiskums. (E), LKB1 ekspresija bija zemāka N2-3, M1 un III-IV stadijas GC pacientiem. (F), LKB1 bija skaitliski izteikti izteikti HER2-negatīviem GC pacientiem. HER2-~+: HER2 negatīvi GC pacienti. HER2++~+++: izņemot HER2 negatīvus GC pacientus. Nepāra t-tests, * p < 0.05, ** p < 0.01, *** p < 0,001.
2. tabula. GC pacientu sākuma raksturlielumi.

3.2. LKB1 veicina imūnsupresīvu mikrovidi GC pacientiem
Saskaņā ar TCGA datu bāzēm T-šūnu receptoru komplekss bija ievērojami atšķirīgs starp GC pacientiem ar augstu un zemu LKB1 ekspresiju (2.A attēls). Mēs arī parādījām, ka T šūnu ekspresija GC pacientiem atšķiras ar augstu un zemu LKB1 ekspresijas apakšgrupām, tostarp CD 8+ T šūnām, regulējošām T šūnām, neitrofiliem un eozinofīliem (2.B attēls). Turklāt tika novērotas spēcīgas korelācijas shēmas starp LKB1 ekspresiju un gēnu regulēšanu, kas iesaistīti T-šūnu imūnās kontrolpunktos, T-šūnu aktivācijā un antigēna prezentācijā (2.C attēls). Mēs tālāk stratificējām GC pacientus, pamatojoties uz PD-1, PD-L1, CD8A, CD8B, CD28 un GZMM mRNS ekspresiju LKB1 augstas un zemas ekspresijas apakšgrupās. Interesanti, ka visi gēni bija ļoti izteikti LKB1-augstas ekspresijas apakšgrupā (attēls 2D). LKB1, PD-1 un PD-L1 ekspresija uzrādīja ierobežotas atšķirības gļotādas un difūzā tipa (papildu attēls S2). Šie dati liecina, ka LKB1 varētu būt saistīts ar T-šūnu aktivācijas fenotipu un T-šūnu imūnās kontrolpunktu GC pacientiem.
3.3. LKB1 tiek selektīvi izteikts T (CD3+CD8+) šūnu infiltrācijās GC
Lai noteiktu LKB1 ekspresiju imūnā mikrovidē, mēs izmērījām sešu imūnsistēmas infiltrējošo šūnu ekspresiju perifērajās asinīs (B), svaigos vēža (T) un blakus esošajos ne-vēža audos (N) un 12 citokīnu ekspresijas veidus GC pacientiem ( 3.A attēls). Mēs arī parādījām LKB1 ekspresiju, pamatojoties uz visu sešu imūnās infiltrācijas šūnu, tostarp B šūnu, T šūnu, neitrofilu, makrofāgu un dendritisko šūnu, pārpilnību (3A attēls un papildu attēls S3). Mēs atklājām, ka T šūnu (CD3+CD8+) īpatsvars bija lielāks blakus esošajos ne-vēža audos (N), savukārt T šūnu īpatsvars (CD3+CD{{ 9}}) bija augstāks svaigos vēža audos (T), un citās T šūnās bija nelielas atšķirības starp svaigiem vēža audiem (T) un blakus esošajiem nevēža audiem (N; 3.B attēls). Turklāt T šūnas (CD3+CD8+LKB1+, CD3+CD8+CD28+LKB1+, CD 3+CD8+CD28+PD−1+LKB1+) bija ievērojami augstāka attiecība svaigos blakus esošajos nevēža audos (N; 3. C attēls). LKB1 ekspresija citās imūnās šūnās bija līdzīga starp svaigiem vēža (T) un blakus esošajiem ne-vēža audiem (N), izņemot neitrofilus (papildu attēls S3). Šie rezultāti kopā parādīja, ka LKB1 varētu būt īpaši saistīts ar T (CD3+CD8+, CD3+CD8+CD28+) šūnu infiltrāta mikrovidi. GC pacientiem.
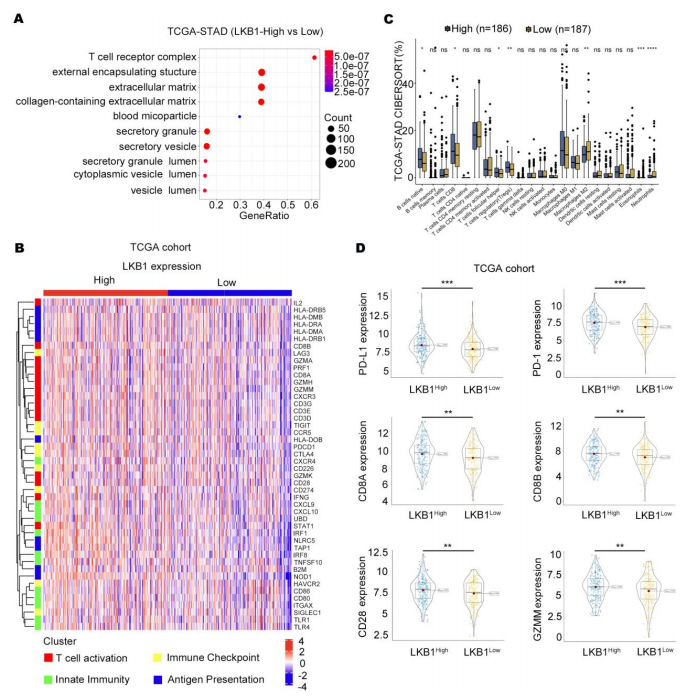
2. attēls. LKB1 ir saistīts ar T-šūnu aktivācijas gēnu un imūnsistēmas kontrolpunktiem. (A) T-šūnu receptoru komplekss uzrādīja vislielāko atšķirību LKB1 augstas un zemas ekspresijas apakšgrupās. (B) CAMOIP datu bāzes analīze par imūno šūnu diferenciālo ekspresiju starp LKB1 augstas un zemas ekspresijas apakšgrupām. (C) Siltuma karte parāda z-score normalizētās log-cpm vērtības paraksta imūno gēnu kopām, pamatojoties uz LKB1 ekspresiju (n=407). (D) PD-1, PD-L1, CD8A, CD8B, CD28 un GZMM bija ļoti izteikti LKB1-augsta GC pacientu apakšgrupā. Nesapārots t-tests, ns: nav būtiskas atšķirības, * p < 0.05, ** p < 0.01, *** p < 0,001 , **** p < 0,0001.

3. attēls. LKB1 ir saistīts ar T-šūnu infiltrāciju GC pacientiem. (A) Siltuma kartē parādīta imūno šūnu proporcija perifērajās asinīs (B), svaigā vēža (T) un blakus esošajos ne-vēža audos (N) un citokīnu ekspresija. (B) dažāda veida T šūnu attiecības svaigos vēža (T) un blakus esošajos ne-vēža audos (N). (C) T šūnu, kas ekspresē LKB1, atšķirīgas proporcijas svaigos vēža (T) un blakus esošos ne-vēža audos (N). Pāra t-tests, * p < 0.05, ** p < 0.01, *** p < 0,001.
3.4. LKB1 ir potenciāli korelēts ar IFN-izteiksmi
Mēs pieņēmām, ka imūnās šūnās ekspresētais LKB1 korelē ar imūno šūnu funkciju. Pamatojoties uz rezultātiem, mēs analizējām saistību starp imūnās infiltrācijas šūnu (LKB1+) proporciju un citokīnu ekspresiju (4.A attēls). Iepriekšējais pētījums parādīja, ka IFN−, ko ražo T šūnas (CD3+CD8+), ir efektīvs rādītājs, lai prognozētu klīnisko efektivitāti un izdzīvošanu ar anti−PD−1 blokādi GC pacientiem [23,24] . Mēs atklājām, ka tikai T šūnu (CD3+LKB1+) un (CD3+CD8+LKB1+) proporcijām bija neliela pozitīva korelācija ar IFN− ekspresija svaigos vēža (T) un blakus esošajos ne-vēža audos (N; 4.B attēls). Pēc tam mēs noteicām LKB1 un IFN- ekspresiju iepriekšminētajos svaigajos vēža (T) un blakus esošajos ne-vēža audos (N) un atklājām, ka LKB1 ekspresija vēža audos bija ievērojami zemāka pretstatā IFN- ekspresijai (4.C attēls). Šie atklājumi liecināja, ka LKB1 varētu būt pozitīva saistība ar pretaudzēju IFN- ekspresiju, ko izdala T šūnas (CD3+CD8+, CD3+CD8+CD{{ 23}}).

4. attēls. LKB1 pozitīvi korelēja ar IFN- ekspresiju. (A) Saiknes analīze starp imūno šūnu infiltrāta (LKB1+) proporciju un citokīnu ekspresiju. (B) T šūnu (CD3+LKB1+) un (CD3+CD8+LKB1+) proporciju korelācija ar IFN- ekspresiju svaigā vēža gadījumā (T) un blakus esošie ne-vēža audi (N). (C) LKB1 un IFN ekspresijas imūnhistoķīmiskās analīzes svaigos vēža (T) un blakus esošos ne-vēža audos (N).
3.5. LKB1 prognozē labu reakciju uz pembrolizumabu GC
Pamatojoties uz rezultātiem, LKB1 varētu būt potenciāls imūnsistēmas kontrolpunkts. Kā norādīts 5.A attēlā, zema LKB1 ekspresija bija saistīta ar ievērojami īsāku kopējo dzīvildzi, pamatojoties uz GC pacientu dzīvildzi no 2015. līdz 2019. gadam. Saskaņā ar šo konstatējumu Kaplan–Meier datubāze (http://kmplot.com/) piekļūts 2023. gada 1. janvārī) arī norādīja, ka LKB1 ekspresija būtiski ietekmēja GC pacientu prognozi, ar ievērojami zemāku kopējo dzīvildzi pacientiem ar zemu LKB1 ekspresiju (5.B attēls). Pēc tam, lai novērtētu LKB1 paredzamo vērtību imūnterapijai, tika analizēta ICB kohorta, kas sastāvēja no GC pacientiem, kuri tika ārstēti ar pembrolizumabu (3. tabula). Salīdzinot ar GC pacientiem ar augstu LKB1 ekspresiju, zemas LKB1 ekspresijas apakšgrupai bija samazināts objektīvās atbildes līmenis (ORR; 5.C attēls). Turklāt GC pacientiem ar zemu LKB1 ekspresiju bija sliktāka PFS un OS (attēls 5D). Iepriekšējais pētījums parādīja, ka PD-L1 mRNS ekspresija bija saistīta ar pembrolizumaba terapijas efektivitāti [6]. Turklāt, pamatojoties uz LKB1 un PD−L1 ekspresiju, GC pacienti tika sadalīti LKB1 ar augstu un zemu PD−L1 augstas un zemas ekspresijas apakšgrupās. Kā parādīts 5E attēlā, GC pacientiem ar augstu LKB1 un PD−L1 ekspresiju bija visaugstākā ORR. Korelācija starp PD−L1/LKB1 ekspresiju un molekulārajiem parametriem GC pacientiem ir apkopota 4. tabulā. Kopumā LKB1 varētu būt potenciāls imūnās kontrolpunkts, lai prognozētu reakciju uz pembrolizumabu GC pacientiem.
3. tabula. Objektīvā kuņģa vēža pacienta reakcija uz pembrolizumabu.
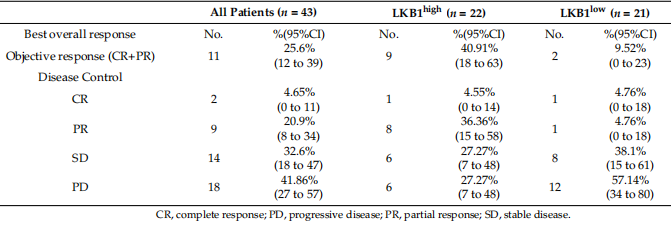
4. tabula. Saistība starp LKB1/PD−L1 ekspresiju un molekulārajiem parametriem.

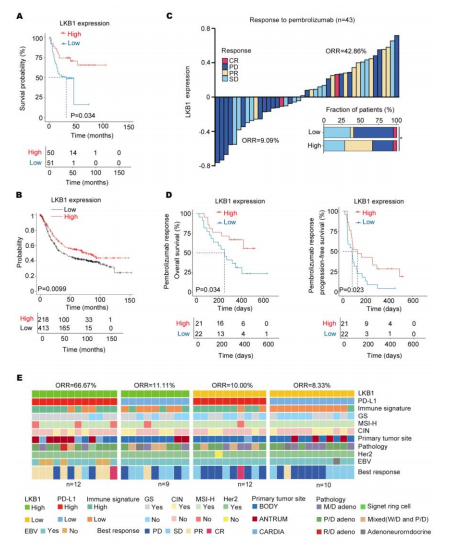
5. attēls. LKB1 ekspresija prognozē reakciju uz pembrolizumabu GC pacientiem. (A) Augsts LKB1 ekspresijas līmenis bija saistīts ar ilgstošu dzīvildzi GC pacientiem no 2015. līdz 2019. gadam. (B) Kaplan-Meier ploteris parādīja, ka augsts LKB1 līmenis pagarināja GC pacientu dzīvildzi. (C) Sarindotie joslu un ūdenskritumu grafiki parāda reakciju uz pembrolizumabu ICB grupā (n=43), pamatojoties uz LKB1 izteiksmi. (Pīrsona χ2 tests). (D) Kaplan-Meier līknes dzīvildzei bez progresēšanas (PFS) un kopējās dzīvildzes (OS) ICB grupā (n=43), pamatojoties uz LKB1 izteiksmi. (E) Pamatojoties uz LKB1 mRNS ekspresiju GC pacientu apakšgrupās ar augstu un zemu PD−L1 ekspresiju, siltuma kartē tika parādīta reakcija uz pembrolizumabu un molekulārajiem parametriem ICB kohortā (n=43). GS, genomiski stabils; MSI-H, mikrosatelītu nestabilitāte-augsta; EBV, EBV pozitīvs; zīmoga gredzenveida šūna: kuņģa zīmogu gredzenveida šūnu karcinoma; ORR, objektīvās atbildes līmenis; SD, stabila slimība; PR, daļēja atbilde; PD, progresējoša slimība; CR, pilnīga atbilde; M/D adeno, vidēji diferencēta adenokarcinoma; P/D adeno, slikti diferencēta adenokarcinoma; W/D adeno, labi diferencēta adenokarcinoma; Jaukta (W/D un P/D), labi diferencēta adenokarcinoma un slikti diferencēta adenokarcinoma.
4. Diskusija
GC ir izplatīta ļaundabīga slimība, un tā ir trešais galvenais vēža izraisīto nāves gadījumu cēlonis visā pasaulē [17,18]. Pēdējo desmitgažu laikā GC terapeitiskās un diagnostikas stratēģijas ir ievērojami uzlabojušās [19]. Tomēr efektīvu diagnostikas marķieru trūkuma dēļ pacienti sākotnēji bieži tiek diagnosticēti vēlīnā stadijā ar 5 gadu dzīvildzi.<20% [25,26]. Therefore, there is an urgent need to explore tumor markers with favorable specificity and sensitivity for GC diagnosis. In this study, we first showed that LKB1 expression was decreased in GC serum. Compared with GC diagnostic biomarkers mainly used in clinical practice, including CEA, CA19−9, and a−1−fetoprotein (AFP), LKB1 showed the best specificity and sensitivity. Furthermore, LKB1 was associated with clinical features of GC patients, such as grade, invasion depth, TNM stage, UICC stage, and vital status. These results suggested that LKB1 serves as a tumor suppressor gene and suppresses GC progression.

cistanche augu paaugstinošā imūnsistēma
Noklikšķiniet šeit, lai skatītu Cistanche Enhance Immunity produktus
【Jautājiet vairāk】 E-pasts:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Sākotnēji LKB1 tika identificēts 1997. gadā un ir pazīstams arī kā STK11 [27]. LKB1 ir svarīgs cilvēka audzēja supresora gēns, un nesīkšūnu plaušu vēža (NSCLC) pacientiem LKB1 mutācijas vai genoma zudums bieži notiek vienlaikus ar KRAS izmaiņām. Šī kombinācija rada ļoti agresīvu fenotipu un samazina izdzīvošanas līmeni [28–30]. Lielākā daļa ziņojumu, kas saistīti ar LKB1, galvenokārt ir vērsti uz plaušu vēzi, un ir ierobežoti ziņojumi par LKB1 lomu GC. Iepriekšējais pētījums parādīja, ka LKB1 ekspresija varētu būt saistīta ar sliktu prognozi GC pacientiem [31]; tomēr, vai LKB1 kalpo kā potenciāls diagnostikas marķieris un imūnterapijas mērķis, nav noskaidrots. Mūsu pētījums pirmo reizi parādīja, ka zema LKB1 ekspresija izraisīja zemāku terapeitisko reakciju pret pembrolizumabu pacientiem ar GC, kas liecina, ka LKB1 varētu būt potenciāls imūnterapijas mērķis.

cistanche tubulosa-uzlabo imūnsistēmu
Nesen imūnterapija ir parādījusi lielas priekšrocības GC klīniskajā ārstēšanā [32, 33]. PD−1/PD−L1 blokāde ir kļuvusi par jaunu un daudzsološu terapeitisku stratēģiju [34], uzsverot pretaudzēju imunitātes nozīmi un normalizējot citotoksisko T limfocītu (CTL, CD8+) disfunkciju vēža gadījumā [35] . Daudzu vēža veidu gadījumā CTL infiltrācija regulē audzēja regresiju un tiek uzskatīta par pozitīvu prognostisko rādītāju [36]. Tomēr pētījumi liecina, ka CTL disfunkcija infiltrācijā izraisa imūnsistēmu izvairīšanos un galu galā nespēju uzbrukt vēža šūnām [37]. Tika pierādīts, ka PD-1/PD-L1 blokāde novērš konstatētos audzējus, izmantojot disfunkcionālus CTL, kas atjauno pretvēža imunitāti [38]. Mēs parādījām, ka PD-1 / PD-L1 bija ļoti izteikts GC pacientu apakšgrupās ar augstu LKB1 ekspresiju, kas liecina, ka LKB1 varētu būt saistīts ar T-šūnu imūnās kontrolpunktiem. Turklāt IFN− ir citokīns, kas inhibē vīrusa replikāciju un uzlabo specifisku antigēnu prezentāciju, ko izdala CD8+T šūnas [39]. Turklāt mēs noskaidrojām, ka T šūnu aktivācijas un antigēnu prezentācijas gēni arī bija ļoti izteikti GC pacientu apakšgrupās ar augstu LKB1 ekspresiju un T (CD3+CD8+LKB1+, CD3+CD8+CD28+LKB1+) šūnām bija pozitīva korelācija ar IFN- ekspresiju svaigos GC pacientu audos. Tādējādi mēs secinājām, ka LKB1 var kavēt T šūnu (CD3+CD8+, CD3+CD8+CD28+) sekrēciju un ir pozitīvi saistīts ar anti −audzēja IFN− ekspresija. Pamatmehānisms, ar kuru LKB1 ir saistīts ar citotoksisku T-šūnu aktivāciju, prasa turpmāku izmeklēšanu.
Atsauces
1. Lībeka, EG; Kērcijs, K.; Džeons, J.; Hazelton, WD Audzēja progresēšanas ietekme uz vēža sastopamības līknēm. Cancer Res. 2013, 73, 1086–1096. [CrossRef] [PubMed]
2. Li, Y.; Viņš, X.; Fan, L.; Džans, X.; Sju, Y.; Xu, X. Jauna imūnās prognostiskā modeļa identificēšana kuņģa vēža gadījumā. Clin. Tulk. Oncol. 2021, 23, 846–855. [CrossRef] [PubMed]
3. Lucs, deputāts; Zalcbergs, JR; Dukrē, M.; Ajāni, JA; Allum, W.; Austs, D.; Bang, YJ; Cascinu, S.; Holšers, A.; Jankovskis, J.; un citi. EORTC St. Gallen starptautiskā ekspertu vienprātība par kuņģa, gastroezofageālā un barības vada vēža primāro terapiju — diferencētas ārstēšanas stratēģijas agrīna gastroezofageālā vēža apakštipiem. Eiro. J. Cancer 2012, 48, 2941–2953. [CrossRef] [PubMed]
4. Tomasens, I.; van Gestels, YR; van Ramshorst, B.; Luyer, MD; Boša, K.; Nienhuijs, DR; Lemmens, VE; de Hingh, IH Kuņģa izcelsmes peritoneālā karcinomatoze: uz populāciju balstīts pētījums par sastopamību, izdzīvošanu un riska faktoriem. Int. J. Cancer 2014, 134, 622–628. [CrossRef]
5. Kahraman, S.; Yalcin, S. Nesenie sasniegumi HER-2 pozitīva progresējoša kuņģa vēža sistēmiskajā ārstēšanā. OncoTargets Ther. 2021, 14, 4149–4162. [CrossRef]
6. Kono, K.; Nakadžima, S.; Mimura, K. Pašreizējais kuņģa vēža imūnkontroles punktu inhibitoru stāvoklis. Kuņģa vēzis 2020, 23, 565–578. [CrossRef]
7. Lordiks, F.; Šitara, K.; Janjigian, YY Jauni līdzekļi kuņģa vēža ārstēšanā. Ann. Oncol. 2017, 28, 1767–1775. [CrossRef]
8. Džans, Y.; Meng, Q.; Saule, Q.; Xu, ZX; Džou, H.; Wang, Y. LKB1 deficīta izraisīta vielmaiņas pārprogrammēšana audzēja veidošanās un neoplastisko slimību gadījumā. Mol. Metab. 2021, 44, 101131. [CrossRef]
9. Kottakis, F.; Nikolajs, BN; Romāne, A.; Kārniks, R.; Gu, H.; Nagle, JM; Boukhali, M.; Heivorda, MC; Li, YY; Čens, T.; un citi. LKB1 zudums saista serīna metabolismu ar DNS metilēšanu un audzēja ģenēzi. Daba 2016, 539., 390.–395. [CrossRef]
10. Su, KH; Dai, S.; Tangs, Z.; Sju, M.; Dai, C. Karstuma šoka faktors 1 ir tiešs AMP aktivētās proteīna kināzes antagonists. Mol. Šūna 2019, 76, 546–561.e8. [CrossRef]
11. Olvēdijs, M.; Tisserand, JC; Lučāni, F.; Boekks, B.; Vouters, J.; Lopess, S.; Rembovs, F.; Aibar, S.; Tīnponts, B.; Barra, J.; un citi. Salīdzinošā onkogenomika identificē tirozīna kināzi FES kā audzēja nomācēju melanomas gadījumā. Dž.Klins. Izpētīt. 2017, 127., 2310.–2325. [CrossRef]
12. Holšteins, PE; Eihners, LJ; Brun, SN; Kamiredijs, A.; Svensons, RU; Vera, LI; Ross, DS; Rymoff, TJ; Hačinss, A.; Galvez, HM; un citi. Ar AMPK saistītās kināzes SIK1 un SIK3 mediē LKB1 galveno audzēju nomācošu efektu NSCLC. Vēža disks. 2019, 9, 1606–1627. [CrossRef]
13. Svensons, RU; Pārkers, SJ; Eihners, LJ; Kolārs, MJ; Volless, M.; Brun, SN; Lombardo, PS; Van Nostrands, JL; Hačinss, A.; Vera, L.; un citi. Acetil-CoA karboksilāzes inhibīcija preklīniskajos modeļos nomāc taukskābju sintēzi un nesīkšūnu plaušu vēža audzēja augšanu. Nat. Med. 2016, 22, 1108–1119. [CrossRef]
14. Zeng, Q.; Čens, Dž.; Li, Y.; Verle, KD; Zhao, RX; Quan, CS; Vanga, YS; Zhai, YX; Vangs, Dž. Jusefs, M.; un citi. LKB1 kavē ar HPV saistīto vēža progresēšanu, mērķējot uz šūnu metabolismu. Onkogēns 2017, 36, 1245–1255. [CrossRef]
15. Pofenbergers, MC; Metcalfe-Roach, A.; Agilars, E.; Čens, Dž.; Hsu, BE; Vongs, AH; Džonsons, RM; Flinns, B.; Samborska, B.; Ma, EH; un citi. LKB1 deficīts T šūnās veicina kuņģa-zarnu trakta polipozes attīstību. Zinātne 2018, 361, 406–411. [CrossRef]
16. Ollila, S.; Domeneks-Moreno, E.; Laajanens, K.; Vongs, IP; Tripathi, S.; Pentinmikko, N.; Gao, Y.; Jans, Y.; Niemela, EH; Vanga, TC; un citi. Stromas Lkb1 deficīts izraisa kuņģa-zarnu trakta audzēju ģenēzi, iesaistot IL-11-JAK/STAT3 ceļu. Dž.Klins. Izpētīt. 2018, 128., 402.–414. [CrossRef]
17. Sungs, H.; Ferlejs, J.; Zīgels, RL; Laversanne, M.; Soerjomataram, I.; Džemals, A.; Bray, F. Globālā vēža statistika 2020. gadā: GLOBOCAN saslimstības un mirstības aplēses visā pasaulē 36 vēža gadījumiem 185 valstīs. CA Cancer J. Clin. 2021, 71, 209–249. [CrossRef]
18. Pons-Tostivints, E.; Lugats, A.; Fontana, JF; Deniss, MG; Bennouna, J. STK11/LKB1 Imūnās atbildes modulācija plaušu vēža gadījumā: no bioloģijas līdz terapeitiskajai ietekmei. Cells 2021, 10, 3129. [CrossRef]
19. Kojama, S.; Akbaja, EA; Li, YY; Aref, AR; Skoulidis, F.; Herter-Sprie, GS; Bučkovskis, KA; Liu, Y.; Avads, MM; Dennings, WL; un citi. STK11/LKB1 deficīts veicina neitrofilu piesaisti un proinflammatorisku citokīnu veidošanos, lai nomāktu T-šūnu aktivitāti plaušu audzēja mikrovidē. Cancer Res. 2016, 76, 999–1008. [CrossRef]
20. Janjigian, YY; Marons, SB; Chatila, WK; Millangs, B.; Čavans, SS; Altermans, C.; Čou, Dž.F.; Segals, MF; Simmons, MZ; Momtazs, P.; un citi. Pirmās līnijas pembrolizumabs un trastuzumabs HER2-pozitīva barības vada, kuņģa vai gastroezofageālā savienojuma vēža gadījumā: atklāts, vienas grupas 2. fāzes pētījums. Lancet Oncol. 2020, 21, 821–831. [CrossRef]
21. Pikārs, E.; Verschoor, CP; Ma, GW; Pawelec, G. Imūno ainavu, ģenētisko apakštipu un atbildes reakcija uz imūnterapiju kolorektālā vēža gadījumā. Priekšpuse. Immunol. 2020, 11, 369. [CrossRef] [PubMed]
22. Kima, ST; Kristesku, R.; Bass, AJ; Kims, KM; Odegaard, JI; Kims, K.; Liu, XQ; Šēra, X.; Jungs, H.; Lī, M.; un citi. Visaptverošs molekulārais raksturojums klīniskajām atbildēm uz PD-1 inhibīciju metastātiska kuņģa vēža gadījumā. Nat. Med. 2018, 24, 1449–1458. [CrossRef] [PubMed]
24. Savas, P.; Virasamijs, B.; Jā, C.; Salims, A.; Mintoff, CP; Karamija, F.; Salgado, R.; Bērns, dīdžejs; Teo, ZL; Dušjantens, S.; un citi. Krūts vēža T šūnu vienšūnu profilēšana atklāj audu rezidentu atmiņas apakškopu, kas saistīta ar uzlabotu prognozi. Nat. Med. 2018, 24, 986–993. [CrossRef] [PubMed]
24. Brūcs, A.; Eikhofs, S.; Dalings, S.; Quast, T.; Bedui, S.; Kročeks, RA; Kurts, C.; Garbi, N.; Baršē, V.; Iannakone, M.; un citi. CD8(+) T šūnas orķestrē pDC-XCR1(+) dendritisko šūnu telpisko un funkcionālo sadarbību, lai optimizētu gruntēšanu. Immunity 2017, 46, 205–219. [CrossRef]
25. Kinošita, J.; Jamaguči, T.; Morijama, H.; Fushida, S. Pašreizējais statuss konversijas operācijas IV stadijas kuņģa vēzi. Surg. Šodien, 2021, 51, 1736–1754. [CrossRef]
26. Du, Y.; Wei, Y. Dabisko killer šūnu terapeitiskais potenciāls kuņģa vēža gadījumā. Priekšpuse. Immunol. 2018, 9, 3095. [CrossRef]
27. Džao, RX; Xu, ZX Mērķtiecība uz LKB1 audzēja nomācēju. Curr. Narkotiku mērķi 2014, 15, 32–52. [CrossRef]
28. Skoulidis, F.; Goldbergs, ME; Greenwalt, DM; Helmans, MD; Avads, MM; Gainors, JF; Schrock, AB; Hartmaiers, RJ; Trabucco, SE; Gejs, L.; un citi. STK11/LKB1 mutācijas un PD−1 inhibitoru rezistence KRAS mutantu plaušu adenokarcinomas gadījumā. Vēža disks. 2018, 8, 822–835. [CrossRef]
29. Kims, Dž.; Lī, HM; Cai, F.; Ko, B.; Yang, C.; Lieu, EL; Muhameds, N.; Reins, S.; Li, K.; Halouls, M.; un citi. Heksosamīna biosintēzes ceļš ir mērķtiecīga atbildība KRAS / LKB1 mutanta plaušu vēža gadījumā. Nat. Metab. 2020, 2, 1401–1412. [CrossRef]
30. Kitadžima, S.; Tani, T.; Springer, BF; Campisi, M.; Osaki, T.; Haratani, K.; Čens, M.; Knelsons, EH; Mahadevan, NR; Riters, J.; un citi. MPS1 inhibīcija veicina KRAS-LKB1 mutanta plaušu vēža imunogenitāti. Cancer Cell 2022, 40, 1128–1144e1128. [CrossRef]
31. Hu, M.; Džao, T.; Liu, J.; Zou, Z.; Sju, K.; Gongs, P.; Guo, H. LKB1 ekspresijas samazināšanās ir saistīta ar epitēlija-mezenhimālo pāreju un izraisīja nelabvēlīgu kuņģa vēža prognozi. Hum. Pathol. 2019, 83., 133.–139. [CrossRef]
32. Hogners, A.; Moehler, M. Imūnterapija kuņģa vēža gadījumā. Curr. Oncol. 2022, 29, 1559–1574. [CrossRef]
33. Kole, C.; Charalampakis, N.; Tsakatikas, S.; Kouris, NI; Papaksoinis, G.; Karamouzis, MV; Koumarianou, A.; Schizas, D. Imūnterapija kuņģa vēža ārstēšanai: 2021. gada atjauninājums. Imūnterapija 2022, 14, 41–64. [CrossRef]
35. Olīva, S.; Troija, R.; D'Agostino, M.; Bokadoro, M.; Gay, F. Solījumi un nepilnības PD-1/PD-L1 inhibitoru lietošanā multiplās mielomas gadījumā. Priekšpuse. Immunol. 2018, 9, 2749. [CrossRef]
35. Farhood, B.; Najafi, M.; Mortezaee, K. CD8 (+) citotoksiskie T limfocīti vēža imūnterapijā: pārskats. J. Cell. Fiziol. 2019, 234, 8509–8521. [CrossRef]
36. Kalathil, SG; Thanavala, Y. Dabiskās killer šūnas un T šūnas hepatocelulārā karcinomas un vīrusu hepatīta gadījumā: pašreizējais statuss un perspektīvas nākotnes imūnterapijas pieejām. Cells 2021, 10, 1332. [CrossRef]
37. Džans, H.; Dzjans, R.; Džou, Dž.; Van, Dž.; Sju, Y.; Džans, H.; Gu, Y.; Fu, F.; Shen, Y.; Džans, G.; un citi. CTL vājināšanās, ko regulē PS1 ar vēzi saistītā fibroblastā. Priekšpuse. Immunol. 2020, 11, 999. [CrossRef]
38. Sjao, M.; Xie, L.; Cao, G.; Lei, S.; Van, P.; Vejs, Z.; Luo, Y.; Fangs, Dž.; Jans, X.; Huangs, Q.; un citi. CD4(+) T-šūnu epitopu bāzes heterologā primārā pastiprināšanas vakcinācija pastiprina pretvēža imunitāti un PD-1/PD-L1 imūnterapiju. J. Immunother. Vēzis 2022, 10, e004022. [CrossRef]
39. Van, V.; Grīns, M.; Choi, JE; Gijona, M.; Kenedijs, PD; Džonsons, JK; Liao, P.; Lang, X.; Kričeks, I.; Pārdod, A.; un citi. CD8+ T šūnas regulē audzēja ferroptozi vēža imūnterapijas laikā. Daba 2019, 569, 270–274. [CrossRef]
