Vienlaicīga aktīna citoskeleta stabilizācija vairākās nefronam specifiskās šūnās aizsargā nieres no dažādiem ievainojumiem
Sep 26, 2023
Hroniskas nieru slimībasunakūts nieru bojājumsir mehāniskiatšķirīgas nieru slimības. Kamēr hroniskas nieru slimības ir saistītas arpodocītu bojājums, akūts nieru bojājumsietekmē nieru kanāliņu epitēlija šūnas. Neskatoties uz šīm atšķirībām,kardināla iezīmeno abiemakūtas un hroniskas nieru slimībasir disregulēts aktīna citoskelets. Mēs to esam parādījušiGTPāzes dinamīna farmakoloģiskā aktivizēšanauzlabo podocītu bojājumushronisku nieru slimību peļu modeļiautorsveicinot aktīna polimerizāciju. Šeit mēs nosakām dinamīna lomu stinguma un polaritātes modulēšanānieru kanāliņu epitēlija šūnassasaistot aktīna pavedienus sazarotos tīklos. Dinamīna šķērssaistīšanas spējas aktivizēšana ar mazas molekulas agonista palīdzību stabilizē apikālās membrānas aktomiozīna garozu pret ievainojumiem, kas savukārtsaglabā nieru darbībudažādos akūtu nieru bojājumu peļu modeļos. Jo īpaši dinamīna agonists vienlaikus vājina podocītu uncauruļveida ievainojumsAlporta sindroma ģenētiskajā peles modelī. Mūsu pētījums sniedz pierādījumus par iespējamību un uzsverjaunu holistisku nefronus aizsargājošu terapiju priekšrocības.

KLIKŠĶINIET ŠEIT, LAI UZZINĀTU CISTANŠES AUGU SASTĀVDAĻU, KAS NODERĪGS AKŪTAS NIERU TRAUMOJUMĀ
Thegalvenie akūtu nieru bojājumu cēloņi(AKI) irišēmija, hipoksija, vainefrotoksicitāte1. Lai gan to var mainīt, AKI ir nozīmīga veselības aprūpes problēma ar augstu mirstību un bez galīgas ārstēšanas. Neatkarīgi no tā etioloģijas AKI galvenokārt ievaino nieru kanāliņu polarizētās epitēlija šūnas, kuru apikālie mikrovilli veido cauruļveida suku robežu, kas piedalās būtiskā elektrolītu un ūdens transporta koordinēšanā2. AKI agrīna morfoloģiskā iezīme ir sukas robežas un šūnu polaritātes zudums aktomiozīna garozas sadalīšanās dēļ apikālajā membrānā1.
Šūnu polaritātes noteikšana un uzturēšana ietver signalizācijas kaskādes, membrānu apriti un citoskeleta dinamiku, kas visas ir ļoti koordinētas3. Apikālās membrānas organizāciju lielā mērā nosaka aktomiozīna tīklu arhitektūra4, kas nosaka garozas stīvumu, tādējādi atvieglojot polaritātes proteīnu klasterizāciju. Lai gan miozīna II motori tiek uzskatīti par primāro garozas stīvuma ģeneratoru5,6, aktomiozīna garozas arhitektūru nosaka neskaitāmi aktīnu saistošie proteīni (ABP)7.

Papildus zināmajiem ABP, nieru kanāliņu sukas apmale ir ļoti bagātināta ar dinamīnu8, GTPāzi, kas vislabāk pazīstama ar savu lomu endocitozē9. Dinaminam ir raksturīga tieksme apvienoties vairākos oligomerizācijas stāvokļos, piemēram, dimēros, tetramēros, gredzenos un spirālēs9. Pirmo reizi mēs identificējām tiešu dinamīna un aktīna mijiedarbību10 un parādījām, ka dinamīna oligomerizācija regulē aktīna polimerizāciju podocītos 11, 12, specializētās šūnās, kas ir būtiskas nieru filtra selektivitātei. Izmantojot CKD peles modeļus, mēs esam parādījuši, ka no dinamīna atkarīgās aktīna polimerizācijas aktivizēšana maina podocītu bojājumus, atjaunojot to unikālo struktūru un funkciju12.
Šeit mēs to parādāmnieru kanāliņu epitēlija šūnas, dinamīns saista pavedienu aktīnu (F-aktīnu) sazarotos tīklos. Dinamīna šķērssaistīšanas spēju nosaka tā oligomerizācijas stāvoklis un F-aktīna garums. Dinamīna oligomerizācijas farmakoloģiskā aktivizēšana neitralizē AKI, stabilizējot aktīna tīklus un tādējādi šūnu integritāti, kas daļēji aizsargā nieru epitēlija šūnas no oksidatīvā stresa izraisītiem bojājumiem. Mūsu pētījums identificē nieru kanāliņu šūnas apikālās membrānas aktomiozīna garozu kā ārstniecisku mērķi AKI, izmantojot dinamīnu kā starpnieku.
Rezultāti Dinamīna oligomerizācija nosaka apikālās membrānas stīvumu un morfoloģiju.
Lai pārbaudītu dinamīna un aktīna mijiedarbības lomu polarizētās nieru kanāliņu epitēlija šūnās, mēs izmantojām Bis-T-23, no aktīna atkarīgas dinamīna oligomerizācijas allosterisko aktivatoru atjaunotā sistēmā13, šūnās11, 13 un viss organisms 12. Šūnu fenotipi tika novērtēti Madin-Darby Canine Kidney (MDCK) šūnās, ievērojot F-aktīna statusu un ciešā savienojuma proteīna zonula occludens-1 (ZO-1) iekrāsošanās modeli, kas ir uzskatīts par šūnu polaritātes biomarķieri. Citohalazīns D (CytoD) un latrunkulīns A (LatA), zināmie aktīna polimerizācijas inhibitori, samazināja F-aktīna līmeni un izraisīja pārtrauktu ZO-1 krāsošanu (papildu 1.a attēls). Turpretim Bis-T-23 izraisīja nelielu F-aktīna līmeņa paaugstināšanos, neietekmējot ZO-1 krāsojumu. Bis-T-23 pievienošana pirms, bet ne pēc LatA, daļēji saglabāja F-aktīna līmeni un šūnu polaritāti. Ne DMSO nesējs, ne dinamīna inhibitors dynols14 neuzrādīja nekādu efektu (papildu attēls 1a).

Skenējošā elektronu mikroskopija (SEM) ļāva mums vizualizēt zāļu izraisītas šūnu morfoloģijas izmaiņas, koncentrējoties uz apikālo membrānu (1.a attēls). Vidējais MDCK šūnu augstums bija 11 ± 2 µm, un vidējais mikrovillu garums bija 0,63 ± 0,2 µm (1. tabula), kas ir nierēs novērotajā diapazonā15. LatA samazināja šūnu augstumu un mikrovillu garumu un vienmērīgi sadalītos mikrovilnīšus pārvietoja klasteros, savukārt Bis-T-23 izraisīja pretējus efektus (1. tabula, 1.a att.). Pievienojot pirms LatA, Bis-T-23 daļēji saglabāja šūnu augstumu un mikrovilnu garumu. Tā kā mikrovilnām ir izsmalcināta garuma kontrole, ko nosaka garozas aktīns to pamatnē16, šie dati liecina, ka Bis-T-23 modificēja aktomiozīna garozu apikālajā membrānā.
Lai noteiktu precīzu Bis-T-23 ietekmi uz kortikālo aktīnu, mēs vizualizējām aktomiozīna garozu lamellipodijā, izmantojot platīna replikas elektronu mikroskopiju (PR-EM). LatA samazināja aktīna tīklu blīvumu, un šis efekts tika daļēji atcelts, pievienojot Bis-T -23 pirms LatA (1.b attēls). Tā kā LatA paātrina aktīna pavedienu depolimerizāciju, atdalot aktīna monomērus, mēs pēc tam pārbaudījām, vai Bis-T -23 novērotā aktomiozīna garozas saglabāšana ir saistīta ar tā pozitīvo ietekmi uz aktīna polimerizāciju. Pretstatā spēcīgajai aktīna polimerizācijas stimulācijai, kas novērota podocītu šūnu ekstraktos10,11, Bis-T-23 tikai nedaudz palielināja aktīna polimerizāciju MDCK šūnu ekstraktā (papildu 1.b attēls). Līdzīgi, endogēnā dinamīna -2 (Dyn2) imūndeficīts no ekstrakta vai tā GTPāzes aktivitātes inhibīcija ar dinodu izraisīja nelielus aktīna polimerizācijas traucējumus (papildu 1.c attēls). Lai gan LatA un CytoD būtiski pasliktināja aktīna polimerizāciju, Bis-T -23 pievienošana pirms LatA vai CytoD nespēja pārvarēt to inhibējošo iedarbību (papildu attēls 1d, e). Jasplakinolīds, zāles, kas inducē aktīna polimerizāciju, stimulējot aktīna pavedienu kodolu veidošanos17, būtiski nepaaugstināja vispārējo polimerizācijas līmeni (papildu attēls 1d), kas liecina, ka MDCK šūnu lizāts uzrāda gandrīz maksimālo polimerizētā aktīna līmeni. Šie dati kopā liecināja, ka Bis-T-23 ietekmi uz apikālās membrānas morfoloģiju MDCK šūnās noteica cits mehānisms, nevis aktīna polimerizācija.
Ņemot vērā vispārpieņemtās zināšanas par Dyn2 un F-aktīna bagātināto lokalizāciju pie nieru epitēlija šūnu birstes8 un dinamīna lomu endocitozē, mēs tālāk pētījām, vai Bis-T -23 ietekmē aktīnu netieši, mainot endocitozi. Kā gaidīts, gan Dyn2, gan F-aktīns vienlaikus lokalizējās aktomiozīna garozā zem apikālās membrānas, mikrovillu iekšpusē un ar klatrīnu pārklātajās bedrēs (CCP), ko nosaka to atšķirīgā forma un izmērs (papildu attēls 1f). Mēs pārbaudījām CCP dinamiku, izmantojot kopējās iekšējās refleksijas fluorescences (TIRF) mikroskopiju 18, 19. Bis-T-23 pat visaugstākajā koncentrācijā neietekmēja CCP kalpošanas laika sadalījumu, turpretim dinols samazināja produktīvo CCP skaitu (papildu 1. g. attēls). Šis korelācijas trūkums starp endocitozes līmeni un šūnu morfoloģijas izmaiņām apstiprina, ka Bis-T- 23 ir vērsta uz kortikālo aktīnu, neietekmējot dinamīna lomu endocitozē.
Tā kā nieru šūnu polaritāti uztur aktomiozīna tīklu arhitektūra un ilgstoša kontrakcija, kas nosaka šūnu stīvumu apikālajā membrānā20, pēc tam mēs izmērījām šūnu stīvumu, izmantojot atomu spēka mikroskopiju (AFM). Nanowizard IV sistēma un JPK analīzes programmatūra tika izmantota, lai noteiktu izmaiņas Young's Modulus21 dažādos eksperimentālos iestatījumos (papildu attēls 2a). Ārstēšana ar LatA izraisīja ievērojamu šūnu un šūnu kontakta stīvuma un apikālās šūnu stīvuma samazināšanos MDCK šūnās (1.c–e att.). Turpretim Bis-T-23 ievērojami palielināja šūnu stīvumu salīdzinājumā ar DMSO nesēju (1.c–e att.), kas atbilst tā pozitīvajai ietekmei uz šūnu augstumu, mikrovillu skaitu un aktīna tīklu blīvumu (1. 1.b att.)22. Bis-T-23 pievienošana pirms LatA ievērojami samazināja LatA negatīvo ietekmi uz šūnu stīvumu (1.c–e att.) saskaņā ar Bis-T-23 pozitīvo ietekmi uz aktīna tīkliem. un apikālo šūnu morfoloģiju (1. tabula, 1.b attēls).
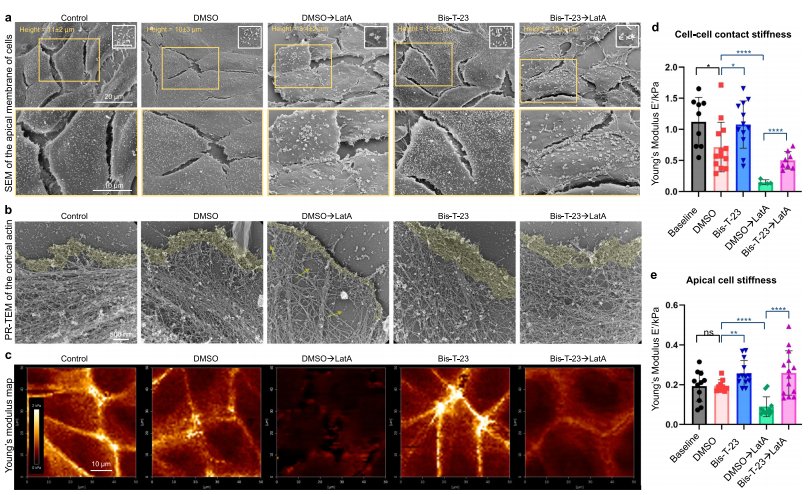
1. attēls. Dinamīna oligomerizācija nosaka šūnu stīvumu, ietekmējot aktīna arhitektūru nieru epitēlija šūnās. a reprezentatīvi SEM attēli MDCK šūnām, kas apstrādātas ar DMSO (0,1%) vai Bis-T-23 (30 µM, 0,1% DMSO) 1 0 min pirms DMSO (0,1%) vai LatA (0,2 µM, 0,1% DMSO) pievienošanas 2{{23} } min. Palielināti ieliktņu attēli (reģioni ar oranžu kastīti) parāda mikrovillu izvietojumu, izplatību un blīvumu apikālajā membrānā. b MDCK šūnu reprezentatīvi PR-EM attēli, kas apstrādāti, kā paskaidrots a) apakšpunktā. Attēli parāda izmaiņas aktomiozīna garozas organizācijā MDCK šūnās norādītajos apstākļos. c Reprezentatīvi attēli Young's Modulus kartēm MDCK šūnām, kas apstrādātas, kā paskaidrots (a). d, e Svītru diagrammas, kas attēlo Younga moduli, kas attēlo šūnu stīvumu, ko mēra šūnu un šūnu krustojumā (d) vai apikālajā membrānā (e). Katrs simbols apzīmē vienas šūnas vidējo stingrību. Rezultāti, kas parādīti d, e, tika iegūti no vismaz 10 šūnām no vismaz trim kultivēšanas traukiem. Kļūdu joslas, vidējais ± SD (*P mazāks vai vienāds ar 0,05, **P mazāks vai vienāds ar 0,01, ***P mazāks vai vienāds ar 0,001, ****P mazāks vai vienāds ar 0,0001, nesapārots divpusējs t-tests). ns, nav nozīmīgi.
Mēs esam arī noteikuši šūnu stīvumu, izmantojot sistēmu BioScope II kā alternatīvu eksperimentālu pieeju AFM. Šajā gadījumā spēka ievilkšanas līknes tika iegūtas pēc Discher un kolēģu modeļa, kas aprēķināts ar Matlab programmatūru23. Līdzīgas tendences attiecībā uz šūnu stīvumu tika reģistrētas mijiedarbībai starp LatA un Bis-T -23 (papildu 2.b, 2.c attēls). Turklāt dinodei nebija nekādas ietekmes uz šūnu stīvumu, savukārt CytoD būtiski samazināja šūnu stīvumu (papildu attēls 2d, e) saskaņā ar to aktīna fenotipiem (papildu 1.a attēls). Kopā šie dati nosaka korelāciju starp aktomiozīna garozas stāvokli, šūnu stīvumu, apikālās membrānas morfoloģiju un šūnu polaritāti. Šie atklājumi arī pārliecinoši parāda dinamīna oligomerizācijas lomu epitēlija šūnu polaritātes mehānisko parametru noteikšanā, izmantojot tās ietekmi uz aktomiozīna garozu.
Dinamīns saista aktīna pavedienus sazarotos tīklos, kas ir šūnu polaritātes pamatā. Lai noskaidrotu molekulāro mehānismu, ar kuru dinamīna oligomerizācija ietekmē aktomiozīna garozas arhitektūru, mēs pēc tam pārbaudījām dinamīna ietekmi uz aktīna pavedieniem atjaunotā sistēmā. Pamatojoties uz pašreizējo hipotēzi, aktīna pavedienu garums nosaka to šķērssavienojuma veidu6. Tā kā kortikālo aktīna pavedienu vidējais garums tīklā priekšējā malā ir no 100 līdz 150 nm24, mēs pārbaudījām dinamīna ietekmi uz īsāku pavedienu organizēšanu, kas radušies, pārklājot F-aktīnu ar gelsolīnu (Gsn-aktīnu) (att. 2a). Dyn2 pievienošanas rezultātā izveidojās lieli, sazaroti tīkli (2.b, c. att.). Pamatojoties uz rekombinantā Dyn2 izmēriem un formām (2.d attēls), tīklus galvenokārt veidoja Dyn2 dimēri (Dyn2DIMER) un tetramēri (Dyn2TETRA), kas mijiedarbojās ar vairākiem aktīna pavedieniem (2.e attēls): Dyn2DIMER bija saistīts ar diviem pavedieniem, Dyn2TETRA saistīja līdz četriem pavedieniem, un Dyn2RING saistīja līdz sešiem pavedieniem. Neliels attēlu palielinājums atklāja, ka no dinamīna atkarīgie tīkli veido mazāku un lielāku gredzenveida formu modeli (2.c att.).

Lai saistītu atjaunotās sistēmas novērojumus ar dinamīna lomu šūnās, mēs pēc tam noteicām endogēnā Dyn2 lokalizāciju garozas aktīna tīklos, izmantojot monoklonālu anti-Dyn2 antivielu, kam sekoja ar zeltu konjugēta sekundārā antiviela (papildu 3.a–c attēls). Kā redzams atjaunotajā sistēmā, dinamīns ir saistīts ar noteiktu skaitu F-aktīna sazarotos tīklos (2. att.). Kopā šie dati identificē jaunu dinamīna aktivitāti, kas ir F-aktīna šķērssavienošana sazarotos tīklos.
Lai saistītu dinamīna šķērssaistīšanas spēju un Bis-T-23 aizsargājošo iedarbību uz aktomiozīna garozu un apikālās membrānas morfoloģiju, mēs pēc tam pārbaudījām Bis-T-23 ietekmi uz dinamīna starpniecību. tīkli atjaunotās sistēmās (3.a att.). Pamatojoties uz kontūru diagrammām, kas nodrošina dažāda kvēldiega blīvuma topogrāfiskus attēlojumus, Bis T-23 palielināja kopējo tīkla blīvumu (3.a attēls), ko varētu izskaidrot ar dinamīnam piesaistītā F-aktīna skaita palielināšanos. tā oligomerizācijas palielināšanās. Turklāt dinamīns spēcīgāk saista īsākus pavedienus nekā garais F-aktīns (3.a–c att.), kas liecina, ka dinamīna spēju veidot sazarotus tīklus nosaka tā oligomerizācijas statuss un aktīna pavedienu garums. Spēja saistīt aktīna pavedienus tīklos bija kopīga divām dinamīna izoformām, visuresošajam Dyn2 un neironam specifiskajam dinamīnam -1 (Dyn1) (3.b, c att.).
Wecistanche atbalsta dienests - lielākā cistanche eksportētāja Ķīnā:
E-pasts:wallence.suen@wecistanche.com
Whatsapp/Tel.:+86 15292862950
Veikals:
Skatīt šeit: https://www.xjcistanche.com/cistanche-shop






