APOBEC{0}}mediētā mutaģenēze vēža gadījumā: cēloņi, klīniskā nozīme un terapeitiskais potenciāls
Oct 17, 2023
Abstrakts
Apolipoproteīna B mRNS rediģēšanas enzīms, katalītiskie polipeptīdi (APOBEC) ir citozīna deamināzes, kas iesaistītas iedzimtajā un adaptīvajā imunitātē. Tomēr daži APOBEC ģimenes locekļi var arī deaminēt saimnieka genomus, lai radītu onkogēnas mutācijas. Rezultātā radušās mutācijas, galvenokārt 2. un 13. paraksts, rodas daudzos audzēju veidos un ir viena no visbiežāk sastopamajām mutācijas pazīmēm vēža gadījumā. Šajā pārskatā ir apkopoti pašreizējie pierādījumi, kas norāda uz APOBEC3 kā galvenajiem mutatoriem, un izklāstīti APOBEC3 ekspresijas un mutācijas aktivitātes eksogēnie un endogēnie ierosinātāji. Pārskatā arī aplūkots, kā APOBEC3-mediētā mutaģenēze ietekmē audzēja evolūciju gan mutagēnos, gan nemutagēnos veidos, tostarp izraisot vadītāja mutācijas un modulējot audzēja imūno mikrovidi. Pārejot no molekulārās bioloģijas uz klīniskiem rezultātiem, pārskats noslēdzas, apkopojot APOBEC3 atšķirīgo prognostisko nozīmi vēža veidos un to terapeitisko potenciālu pašreizējā un nākotnes klīniskajā ainavā.
Atslēgas vārdi APOBEC, Vēzis, Somatiskās mutācijas, Dzimumlīnijas ģenētika, Audzēja mikrovide, Biomarķieri, Imūnterapija

Ķīniešu herb cistanche augs-Pretaudzēju
Fons
polipeptīdi (APOBEC) ir citozīna deamināžu klase ar vienpadsmit primārajiem ģimenes locekļiem: APOBEC1, aktivācijas izraisīta deamināze (AID), APOBEC2, APOBEC3 (A–H) un APOBEC4. Alternatīva APOBEC3B, APOBEC3H un APOBEC3F savienošana vēl vairāk dažādo APOBEC virsģimeni [1–4]. Lai gan visiem APOBEC ģimenes locekļiem ir saglabāts katalītiskais domēns, tiem ir atšķirīgas funkcijas, mutācijas substrāti un audu ekspresijas modeļi [5]. Piemēram, AID tiek ekspresēts aktivētās B šūnās un veicina antivielu dažādošanu, deaminējot imūnglobulīna gēnus [6]. Turpretim APOBEC1 tiek ekspresēts tievajās zarnās un rediģē mRNS, lai nodrošinātu saīsināta, bet funkcionāli svarīga kuņģa-zarnu trakta proteīna audiem specifisku ekspresiju [7–9]. APOBEC3 ir daudz plašāk izteikti cilvēka audos un deaminē un tādējādi bojā vīrusu genomus kā daļu no iedzimtas imūnās atbildes [10]. Lai gan APOBEC3 aizsargā šūnas no vīrusu infekcijas, tie arī padara saimnieka DNS neaizsargātu pret mutācijām. APOBEC3-mediētā mutaģenēze sākas ar citozīna deamināciju, un visi APOBEC3 var deaminēt vienpavedienu DNS (ssDNS) ar dažādu enzīmu aktivitātes līmeni [11–13]. APOBEC3 ssDNS substrāti var īslaicīgi rasties divpavedienu genomā normālu šūnu procesu, piemēram, DNS replikācijas, transkripcijas un genoma remonta, laikā. Piemēram, gan APOBEC3A, gan APOBEC3B DNS replikācijas laikā var deaminēt atpalikušo virkņu šablonus [14–16]. APOBEC3A var iedarboties arī uz matadata cilpām, kas veidojas DNS replikācijas laikā, savukārt APOBEC3B galvenokārt deaminē R cilpas transkripcijas laikā [17, 18]. APOBEC3G var līdzīgi iedarboties uz ssDNS transkripcijas laikā, īpaši 5′ UTR robežās [15]. Turklāt ir pierādīts, ka APOBEC3G deaminē nesalocītu un brīvi salocītu ssDNS (1. att.) [19].

1. attēls. APOBEC3-mediētās mutaģenēzes mehānismi un vēlamie substrāti. Augšējais panelis: APOBEC3s deaminē ssDNS, atstājot uracilu DNS veidnē. Kļūdaini replikācijas un labošanas ceļi var radīt 2. un 13. mutācijas parakstus. Remonts ar translācijas sintēzes (TLS) polimerāzi REVI ģenerē C-to-G mutāciju (13. paraksts), savukārt labošana ar citiem enzīmiem, piemēram, DNS polimerāzi δ, DNS polimerāzi. ε, un TLS polimerāze κ ģenerē C-to-T mutāciju (2. paraksts) [20]. Apakšējais panelis: galvenajiem mutatoriem starp APOBEC3 superģimeni ir atšķirīgas substrāta izvēles, ko galvenokārt nosaka trinukleotīdu konteksts un ssDNS sekundārā struktūra.
SsDNS ietvaros dažādie APOEBC3 deaminē citozīnus atšķirīgos trinukleotīdu kontekstos. Piemēram, APOBEC3A un APOBEC3B, kas ir galvenie mutatori, deaminē tiamīnu pirms citozīna (TpC) motīviem; APOBEC3A galvenokārt iedarbojas uz TpC motīviem pēc pirimidīniem, savukārt APOBEC3B mēdz deaminēt TpC motīvus pēc purīniem [20–23]. Pēc deaminācijas dažādi šūnu procesi var radīt C-toT un C-to-G mutācijas, kas COSMIC ir definētas attiecīgi kā 2. un 13. paraksts [24–26]. Iepriekšējā C-to-T pāreja ir biežāka un rodas no uracilu saturošu DNS veidņu nepareizas replikācijas, savukārt abas aizstāšanas var notikt, kļūdaini labojot uracila glikozilāzes aktivitātes radītās abāziskās vietas (1. att.) [20, 27–29. ]. Papildus šiem tradicionāli definētajiem APOBEC3-inducētajiem mutāciju parakstiem, APOBEC3G var izraisīt C-to-T pārejas TCC, GCC, CCC, CCT un GCG motīvos (1. att.) [30]. APOBEC3-inducētās mutācijas ir visuresošas vēža gadījumā un var rasties izkliedētas visā genomā vai klasteros. Vairāk nekā 75% kateegiju audzēja genomos ir attiecināti uz APOBEC3 aktivitāti, salīdzinot ar 15% difūzāku omikli hipermutāciju [31, 32]. Kopumā APOBEC{33}inducētās mutācijas var veidot līdz pat 68% no audzēja mutāciju sloga un ir konstatētas vairāk nekā pusē no visiem audzējiem; Biežāk sastopami tikai ar vecumu saistīti paraksti [26, 27, 33]. Daudzas no šīm APOBEC{39}}izraisītām izmaiņām ir ļoti atkārtotas virzītāja mutācijas, kas ietekmē onkogēnus un audzēja nomācējus, un APOBEC3 var ietekmēt arī slimības gaitu, izmantojot nemutagēnus ceļus, piemēram, imūnmodulāciju audzēja mikrovidē.
1. tabula APOBEC3 pārmērīga ekspresija un korelācija ar mutāciju slogu vēža gadījumā

APOBEC3 var veicināt imūnsistēmas aktivētus vai imūnsupresētus fenotipus, kas var daļēji izskaidrot to atšķirīgo prognostisko nozīmi dažādos vēža veidos. Pamatojoties uz klīniskajām asociācijām un pirmsklīniskajiem pētījumiem, APOBEC3 varētu izmantot kā biomarķierus un mērķtiecīgi izmantot terapiju. Tādējādi APOBEC3-mediētās mutaģenēzes cēloņi un klīniskās sekas ir svarīgas izpētes jomas un šī pārskata uzmanības centrā.
APOBEC3 ekspresija vēža gadījumā
APOBEC3 ir izteikti zemā līmenī daudzos veselos audos, bet bieži vien ir pārmērīgi izteikti audzējos. Lielākajā daļā pētījumu ir izmantota uz RNS balstīta profilēšana, lai noteiktu APOBEC3 ekspresiju, un uz olbaltumvielām balstītas analīzes ir bijušas ierobežotākas (1. APOBEC3B parasti tiek ekspresēts augstākā līmenī nekā citi APOBEC3 ģimenes locekļi, un vairāku vēža veidu analīze atklāja APOBEC3B bagātināšanos astoņos audzēju veidos: urīnpūšļa, krūts, galvas un kakla, plaušu adenokarcinomas, plaušu plakanšūnu karcinomas, prostatas, skaidru šūnu nierēs, un dzemdes [34]. Augsta APOBEC3B ekspresija tika novērota arī dzemdes kakla un ādas vēža gadījumā, lai gan veseli audi nebija pieejami salīdzināšanai [34]. Līdzīgi ir ziņots par augstu APOBEC3B līmeni urīnpūšļa, žults ceļu, plaušu, kuņģa, barības vada, neiroendokrīno un olnīcu audzējos [35–43]. Citu APOBEC3 ekspresija var būt arī disregulēta vēža gadījumā. Piemēram, APOBEC3G ir konstatēts augstā līmenī resnās zarnas un aizkuņģa dziedzera audzējos [49, 50]. Krūts vēža gadījumā pētījumi atklāja APOBEC3A, APOBEC3B un APOBEC3H bagātināšanos [27, 48]. Augsta APOBEC3 ekspresija ir novērota arī vairāku hematoloģisku vēža gadījumā. Piemēram, APOBEC3A bagātināšana ir novērota leikēmijas gadījumā, un gan APOBEC3B, gan APOBEC3C ir konstatēti paaugstinātā līmenī primārās izsvīduma limfomas gadījumā [45, 52].

Cistanche tubulosa-Antitumor priekšrocības
APOBEC3A un APOBEC3B kā galvenie mutatori
APOBEC3 pārmērīga ekspresija, iespējams, veicina mutaģenēzi, jo vairākos pētījumos ir konstatēta korelācija starp APOBEC3 ekspresiju un parakstam raksturīgu mutāciju slogu (1. Vairāku audzēju veidu kombinētajā analīzē APOBEC3B ekspresija bija cieši saistīta ar lielāku APOBEC3-inducēto mutāciju slodzi; APOBEC3A, APOBEC3F un APOBEC3G uzrādīja līdzīgas, bet vājākas korelācijas [27]. Augsta APOBEC3B ekspresija bija saistīta arī ar vairāk APOBEC3- izraisītām mutācijām plaušu vēža gadījumā, savukārt gan APOBEC3A, gan APOBEC3B līmenis korelēja ar APOBEC3- izraisītām mutācijām krūts vēža gadījumā [22, 47, 53, 54]. Līdzīgas asociācijas ir novērotas urīnpūšļa vēža gadījumā, kam ir viens no augstākajiem APOBEC{19}}inducēto mutāciju slogu [1, 27, 34, 46]. Holangiokarcinomas gadījumā tikai APOBEC3A ekspresija bija saistīta ar APOBEC{25}}inducēto mutāciju slogu [43]. Šīs korelācijas liecina, ka gan APOBEC3A, gan APOBEC3B veicina mutaģenēzi, taču šo ģimenes locekļu relatīvā nozīme joprojām ir pretrunīga [47, 58]. Bieži tiek pieņemts, ka APOBEC3B ir galvenais mutators, ņemot vērā tā augstāko ekspresiju daudzos audzējos [22, 26, 34–36, 45, 48, 59]. Tomēr APOBEC3A ir lielāka fermentatīvā aktivitāte, kas var ļaut tai radīt vairāk mutāciju, neskatoties uz parasti zemāku audu ekspresiju [47, 60]. Attiecīgi, salīdzinot APOBEC3 knockout šūnu līnijas, atklājās, ka APOBEC3A deficītam ir vislielākā ietekme uz mutaģenēzi [58]. Šis rezultāts apstiprina agrākos atradumus raugā, kas vispirms atšķīra APOBEC3A un APOBEC3B izraisītas mutācijas un atklāja, ka pirmās ir vairāk sastopamas audzēja genomos [23]. Apstiprinot APOBEC3A kā dominējošo mutatoru, APOBEC3B dzimumšūnu dzēšana, kas ģenerē APOBEC3A kodējošā reģiona himēru, kas savienota ar APOBEC3B 5′ UTR, ir saistīta ar vairāk APOBEC izraisītām mutācijām dažos vēža veidos [61–64]. Citi APOBEC3 ģimenes locekļi, iespējams, izraisa mutācijas, jo in vitro analīze turpināja, kaut arī ievērojami samazinājās, 2. un 13. parakstu iegūšana, neskatoties uz to, ka tika izslēgti gan APOBEC3A, gan APOBEC3B [58]. APOBEC3H var veicināt šo atlikušo mutaģenēzi, īpaši vēža gadījumā ar APOBEC3H I haplotipu, kam ir spēcīga fermentatīvā aktivitāte un palielināta kodola lokalizācija [65]. APOBEC3G varētu būt arī mutagēns, jo tā ekspresija ir saistīta ar atšķirīgu mutācijas parakstu [30]. Tādējādi vairāki APOBEC3 var izraisīt mutācijas vēža gadījumā, un nozīmīgākie mutatori dažādos audzējos var atšķirties.
APOBEC3 mediētās mutaģenēzes eksogēni un endogēnie ierosinātāji
Vīrusu infekcija
APOBEC3 ir interferona stimulēti gēni, ko inducē ļoti dažādi vīrusi, tostarp poliomas vīrusi, parvovīrusi, herpesvīrusi un B hepatīta vīrusi [66]. Tādējādi daudziem ar vīrusu saistītiem vēža veidiem ir liels 2. un 13. mutācijas parakstu daudzums. Piemēram, dzemdes kakla vēzi vairāk nekā 95% gadījumu izraisa cilvēka papilomas vīruss (HPV), un tam ir daudz APOBEC{7}}inducētu mutāciju [67]. , 68]. APOBEC izraisītas mutācijas ir izplatītas arī galvas un kakla plakanšūnu karcinomas (HNSCC) gadījumā ar spēcīgu korelāciju starp HPV pozitivitāti un mutācijas 2. un 13. parakstu [69]. Vīrusu infekcija var arī veicināt APOBEC{14}}mediētu mutaģenēzi dažos vēža veidos, kas tradicionāli netiek uzskatīti par saistītiem ar vīrusu. Saskaņā ar hipotēzi "trāpīt un palaist", vīrusu infekcija var izraisīt APOBEC3 aktivitāti agrīnā audzēja ģenēzes stadijā, bet tiek izvadīta pirms audzēja noteikšanas [70]. Šī postulācija varētu attiekties uz dažiem urīnpūšļa vēža gadījumiem, jo anamnēzē BK poliomas vīrusa (BKPyV) pozitīvs urīns ir saistīts ar palielinātu urīnpūšļa vēža risku [71]. Tika arī pierādīts, ka BKPyV infekcija inducē APOBEC3 ekspresiju un deaminācijas aktivitāti normāla cilvēka urotēlija in vitro modelī [72]. Potenciālais BKPyV izraisītas urīnpūšļa kanceroģenēzes risks var būt īpaši augsts cilvēkiem ar novājinātu imūnsistēmu, īpaši orgānu transplantācijas saņēmējiem. Attiecīgi BKPyV virēmija vai citas ar poliomas vīrusu saistītas komplikācijas ir saistītas ar četras reizes lielāku urīnpūšļa vēža risku pēc nieres transplantācijas [73–77].
Dziļa urīnpūšļa audzēju genomu sekvencēšana no orgānu transplantācijas saņēmējiem ir arī atklājusi BKPyV integrāciju [78–80]. Lai gan noteiktas vīrusu infekcijas var veicināt APOBEC3-mediētu mutaģenēzi dažos tradicionāli ne-vīrusu vēža veidos, iespējams, ir svarīgi papildu faktori, ņemot vērā APOBEC3-inducēto mutāciju pastāvīgo iegūšanu vēlīnā audzēja evolūcijas posmā un, iespējams, pēc infekcijas izvadīšanas. [22, 56, 81, 82]. Šādi faktori, kas nav saistīti ar vīrusiem, var arī izskaidrot APOBEC{10}}izraisītu mutāciju izplatību vēža gadījumos, kuriem vīrusa etioloģija ir mazāk ticama.

cistanche priekšrocības vīriešiem - stiprina imūnsistēmu
Noklikšķiniet šeit, lai skatītu Cistanche Enhance Immunity produktus
【Jautājiet vairāk】 E-pasts:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
Iekaisums
Neskaitāmi faktori var izraisīt iekaisumu, kas var palielināt APOBEC3 ekspresiju, izmantojot NF-κB signālu pārraidi - galveno iekaisuma ceļu. Atbalstot šo hipotēzi, APOBEC3B promotorā ir konstatētas trīs NF-κB saistīšanās vietas, un p65/p50 un p65/c-Rel heterodimēri, kas ir daļa no kanoniskā NF-κB ceļa, ir izrādījušies svarīgi APOBEC3B transkripcijai [83]. . Nekanoniskā NF-κB signalizācija var arī regulēt APOBEC3 ekspresiju, jo APOBEC3B promotors satur RelB saistīšanās vietu. Vairāki zināmi APOBEC3 induktori, piemēram, LPS un IL-4, arī ir spēcīgi NF-κB aktivatori, kas vēl vairāk norāda uz NF-κB kā APOBEC3 transkripcijas virzītāju iekaisuma laikā [84]. NF-κB signalizācija var arī netieši palielināt APOBEC3 ekspresiju, izmantojot pro-iekaisuma mediatoru transkripciju. Piemēram, ir pierādīts, ka NF-κB mērķa gēns IL-6 inducē APOBEC3B ekspresiju hepatocelulārajā karcinomā, izmantojot JAK/STAT signālu [85, 86]. Tāpat tika atklāts, ka TNF- veicina APOBEC3A ekspresiju keratinocītos [87, 88]. Apstiprinot šos atklājumus, holangiokarcinomas un žultspūšļa vēža pētījums atklāja gan APOEBC3A, gan APOBEC3B regulējumu ar IL-6 un TNF iedarbību [43]. Turklāt IFN ir bijis iesaistīts kā APOBEC3B ekspresijas virzītājspēks urīnpūšļa audzējos un plaušu adenokarcinomā [46, 89]. Tādējādi NF-κB signalizācija — ar spēju darboties gan tieši caur APOBEC3 transkripciju, gan netieši caur citiem iekaisuma mediatoriem — tādējādi ir iespējamais APOBEC{44}}mediētās mutaģenēzes virzītājspēks vēža gadījumā (2. att.). Šī NF-κB APOBEC3-inducējošā loma var būt īpaši svarīga imunoloģiski "karstos" audzējos ar ļoti iekaisušu mikrovidi.
Zāļu iedarbība un replikācijas stress
Dažu zāļu iedarbība var izraisīt arī APOBEC{0}}mediētu mutaģenēzi, un ir pierādīts, ka tādas ķīmijterapijas kā bleomicīns, cisplatīns, etopozīds, 5-fluoruracils, gemcitabīns, hidroksiurīnviela, afidikolīns, kamptotecīns izraisa APOBEC3 ekspresiju vēža gadījumā. šūnu līnijas [1, 61, 90, 91]. NF-κB signalizācija, iespējams, ir starpnieks APOBEC3 indukcijā, reaģējot uz dažām no šīm zālēm, taču liela nozīme var būt arī replikācijas stresam un PI3K signalizācijai (2. att.) [1, 90, 92, 93]. Papildus APOBEC3 ekspresijas palielināšanai genotoksiskās zāles var vēl vairāk veicināt APOBEC{16}}mediētu mutaģenēzi, izraisot genoma bojājumus un tādējādi radot ssDNS substrātus (3. attēls). Pat ja nav genotoksisku zāļu, vēža šūnas var izjust APOBEC{18}}izraisošu replikācijas stresu uzkrāto DNS bojājumu un specifisku onkogēnu mutāciju dēļ. Piemēram, krūts vēža gadījumā ir pierādīts, ka PTEN samazināšanās un HER2 amplifikācija izraisa replikācijas stresu un palielina APOBEC3B aktivitāti in vitro [90]. Plaušu vēža gadījumā FHIT1 zudums — izplatīta ģenētiska izmaiņa, kas izraisa replikācijas stresu — bija saistīta ar lielāku APOBEC{23}}izraisītu mutāciju slodzi [53]. Šīs replikācijas stresu izraisošās mutācijas var būt īpaši spēcīgi APOBEC{26}}mediētās mutaģenēzes ierosinātāji, jo tās izraisa pastāvīgas izmaiņas šūnās atšķirībā no pārejošākas APOBEC3 indukcijas pēc vīrusu infekcijas vai zāļu iedarbības. Pozitīvas atgriezeniskās saites cilpā palielināta APOBEC3 ekspresija var saasināt replikācijas stresu papildu DNS bojājumu, palēninātu replikācijas dakšu un šūnu cikla apstāšanās dēļ [52, 97–99]. Replikācijas stresa kontekstā APOBEC3, jo īpaši APOBEC3B, var būt īpaši pakļauti kataegis, nevis difūzākiem mutāciju modeļiem. Attiecīgi ir pierādīts, ka APOBEC3B telomēru krīzes laikā izraisa katageis vēža šūnu līnijās [94]. APOBEC3B bija līdzīgi saistīts ar kataegis šūnu līnijās ar p53- deficītu, un visas vēža analīze atklāja, ka APOBEC3B ekspresija bija pozitīvi korelēta ar kataegis [31, 99].

cistanche tubulosa-uzlabo imūnsistēmu
Somatiskās un dzimumšūnu izmaiņas
Somatiskās mutācijas vairākos gēnos ir saistītas ar palielinātu APOBEC{0}}mediētu mutaģenēzi, taču visa genoma sekvencēšanas analīzes nav atklājušas atkārtotus somatiskus viena nukleotīda variantus APOBEC3 kodējošajos vai regulējošajos reģionos [100, 101]. Tāpēc ir maz ticamas somatiskās mutācijas, kas palielina APOBEC3 deaminācijas aktivitāti, tāpat kā mutācijas, kas maina APOBEC3 ekspresiju, palielinot promotora vai pastiprinātāja aktivitāti. Tomēr palielināta APOBEC3 ekspresija var rasties kopiju skaita palielināšanās dēļ vēža gadījumā. Lai gan novērotas tikai vienā vēža tipā, APOBEC3 kopiju skaita izmaiņas tika konstatētas ~ 30% plaušu audzēju [36, 102]. Šī ģenētiskā izmaiņa bija saistīta ar palielinātu APOBEC3B ekspresiju un lielāku APOBEC izraisītu mutāciju slodzi [36]. Šķiet, ka dīgļu līnijas varianti APOBEC3 gēna lokusā ir biežāk sastopami un var ietekmēt APOBEC3 ekspresiju un vēža risku. Piemēram, viena nukleotīda polimorfisms (SNP) rs1014971, kas atrodas augšpus APOBEC3 gēnu klastera, ir saistīts ar palielinātu APOBEC3B ekspresiju, APOBEC{21}}inducēto mutāciju bagātināšanu un lielāku urīnpūšļa vēža risku [61, 63, 103]. Krūts vēža gadījumā dzēšanas polimorfisms, kas ģenerē APOBEC3A/B himēru, ir saistīts ar paaugstinātu slimības risku, vairāk APOBEC{26}}inducētu mutāciju un sliktu audzēja diferenciāciju (negatīvas prognozes pazīme) [47, 61, 62, 64 , 104, 105]. Tas pats dzēšanas polimorfisms var veicināt APOBEC{33}}inducētu hipermutāciju akūtas limfoblastiskas leikēmijas gadījumā [62]. Plaušu vēža gadījumā sešu SNP kombinācija, kas nosaka APOBEC3H I haplotipu, ir saistīta ar paaugstinātu slimības risku [65] (2. Ģenētiskā variācija šajā haplotipā var vēl vairāk palielināt plaušu vēža risku [106]. Turklāt ir pierādīts, ka variants rs2267401 palielina žultspūšļa vēža un hepatocelulārās karcinomas risku, iespējams, palielinoties APOBEC3B ekspresijai, ko izraisa paaugstināta promotora aktivitāte un IL-6 reakcija [43, 86]. Turpretim tas pats SNP rs2267401 bija saistīts ar samazinātu holangiokarcinomas risku un zemāku APOBEC3B promotora aktivitāti šajā audzēja tipā, iespējams, transkripcijas represora TFAP2A pārmērīgas ekspresijas dēļ [43]. Vēl viens variants, rs12157810, ir saistīts arī ar zemāku holangiokarcinomas un žultspūšļa vēža risku, lai gan tika konstatēts, ka tas palielina APOBEC3A promotora aktivitāti [43]. Saskanīgi rezultāti tika novēroti nieru vēža gadījumā [108]. Vēl viens SNP rs139293 ir saistīts ar samazinātu plaušu vēža risku [107]. Šis variants, kas atrodas eksonā, rada potenciāli aktivitāti samazinošas aminoskābju izmaiņas APOBEC3H un var pazemināt APOEBC3H un APOBEC3C ekspresiju [107] (2. tabula).

2. att. APOBEC3 gēnu transkripcijas regulēšana. NF-κB signalizācija ir kopīgs ceļš endogēniem un eksogēniem APOBEC3 trigeriem. Lai izraisītu APOBEC3, NF-κB signalizācija darbojas tieši, izmantojot APOBEC3 transkripciju, un netieši, izmantojot citu iekaisuma mediatoru transkripciju. Galvenie iekaisuma mediatori ir interferoni, TNF- un IL-6, kas var vadīt APOBEC3 transkripciju, izmantojot NF-κB un JAK/STAT signālus. Turklāt replikācijas stress var aktivizēt NF-κB signalizāciju, izmantojot PI3K / Akt, lai veicinātu APOBEC3 ekspresiju
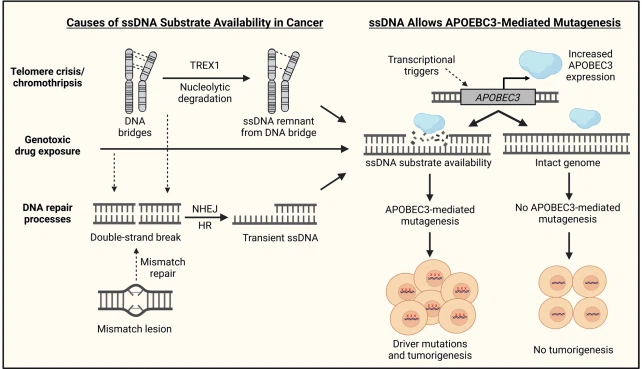
3. att. APOBEC3-mediētās mutaģenēzes divu faktoru modelis. Divu faktoru modelī APOBEC3-mediētajai mutaģenēzei ir nepieciešama gan APOBEC3 ekspresijas indukcija, gan ssDNS pieejamība. Tādi faktori kā zāļu iedarbība, telomēru krīze un DNS labošanas procesi var radīt ssDNS, savukārt transkripcijas izraisītāji var pārregulēt APOBEC3 ekspresiju [94–96]
Retrotransposona aktivitāte, telomēru krīze un DNS bojājumi
Vēža šūnām parasti ir nestabili genomi, kas var veicināt APOBEC{0}}mediētu mutaģenēzi, izmantojot vairākus atšķirīgus ceļus. Konkrēti, genoma nestabilitāte var veicināt retrotransposona aktivitāti un tādējādi izraisīt epizodiskus APOBEC3-mediētas mutaģenēzes uzliesmojumus [112]. Genoma nestabilitāte ir saistīta arī ar telomēru krīzi un hromotripsi, kas, kā pierādīts, ģenerē ssDNS pārtraukuma punktus, ko deaminē APOBEC3B [94] (3. att.). APOBEC3-mediētu mutaģenēzi var izraisīt APOBEC3 regulēšana DNS bojājumu izraisīta replikācijas stresa laikā un ar to saistītie neatbilstības labošanas procesi, piemēram, nehomologā gala savienošana (NHEJ) un homologā rekombinācija (HR), kas rada ssDNS starpproduktus [90] , 95, 96, 113–116] (3. att.). Tā kā APOBEC3 var deaminēt atpalikušo virkņu veidnes, ātri dalošās vēža šūnas var būt bieži pakļautas ssDNS, tādējādi veicinot APOBEC{17}} mediētu mutaģenēzi [14]. Šie endogēnie procesi vēža šūnās var veicināt nepārtrauktu APOBEC{19}}inducētu mutāciju iegūšanu vēlīnā audzēja evolūcijas posmā, nepakļaujoties eksogēniem trigeriem [81]. DNS bojājumu un ssDNS substrāta pieejamības nozīme var arī izskaidrot, kāpēc APOBEC3 daudzos veselos audos tiek ekspresēti zemā līmenī un parasti neizraisa ievērojamus audzēja genomam līdzīgus mutāciju modeļus. Veselos barības vada vai endometrija dziedzeru audos nav konstatētas nozīmīgas APOBEC3-inducētu mutāciju slodzes, lai gan zems šādu mutāciju līmenis ir konstatēts nevēža zarnu kriptu un bronhu epitēlija šūnu apakškopā [59, 117–120. ]. Tādējādi APOBEC3 aktivitātes divu faktoru modelis ir ticams daudzu vēža veidu gadījumā, jo gan paaugstināta APOBEC3 ekspresija, gan jau esošie DNS bojājumi ir nepieciešami APOBEC{32}}mediētajai mutaģenēzei (3. attēls).
Smēķēt?
Smēķēšana ir galvenais riska faktors vairākiem vēža veidiem ar augstu APOBEC{0}}izraisītu mutāciju slodzi. Piemēram, smēķēšana rada vairāk nekā 50% urīnpūšļa vēža riska un tiek lēsts, ka tā izraisa 80–90% plaušu audzēju [121, 122]. Smēķēšana ir visspēcīgāk saistīta ar mutācijas 4., 5. un 29. parakstu, taču vairākos pētījumos ir pārbaudīts, vai tabakas iedarbība ir saistīta arī ar APOBEC3- izraisīto 2. un 13. parakstu [24–26, 123, 124]. Tomēr rezultāti ir bijuši pretrunīgi. Plaušu adenokarcinomas analīzē 2. un 13. paraksts tika bagātināts ar smēķētāju audzējiem [123]. Urīnpūšļa vēža gadījumā paraksts 13 tika bagātināts ar audzējiem no bijušajiem smēķētājiem [125]. Tomēr atsevišķā tikai muskuļos invazīvo urīnpūšļa audzēju analīzē atklājās, ka 13. paraksts bija bagātināts nesmēķētājiem un negatīvi korelēja ar 5. parakstu [124]. Turklāt in vitro pētījumā ar normālu cilvēka urotēliju tika atklāts, ka benzo[a]pirēna – prokarcinogēna cigarešu dūmos – iedarbība neizraisīja 2. vai 13. parakstu. Tomēr šim pētījumam ir ierobežojumi, jo tajā tika izmantots tikai viens prokarcinogēns. tabakas dūmi ietver aptuveni 60 kancerogēnu [126]. Ja smēķēšana tomēr palielina APOBEC{29}}mediēto mutaģenēzi, efekts, visticamāk, ir saistīts ar vispārēju DNS bojājumu, kas palielina ssDNS substrāta pieejamību [123]. Lai gan tabakas nikotīna sastāvdaļa var izraisīt iekaisumu un NF-kB signālu pārraidi, nav pierādījumu, ka tabakas dūmi tieši palielina APOBEC3 ekspresiju. Vienā pētījumā par nesīkšūnu plaušu vēzi tika pārbaudīta šī hipotēze, taču netika atrasta nekāda saistība starp smēķēšanu un APOBEC3B mRNS ekspresiju [54]. Tomēr smēķēšanas kā izplatīta vēža riska faktora izplatība, kur plaši darbojas APOBEC{36}}mediētā mutaģenēze, var apgrūtināt smēķēšanas un APOBEC3 mijiedarbības noteikšanu.
2. tabula Dīgļu līnijas varianti, kas ietekmē APOBEC3 un vēža risku

2. tabula (turpinājums)

APOBEC3 ietekme caur mutagēniem un nemutagēniem ceļiem APOBEC3 izraisītām onkogēnām kodējošām mutācijām
APOBEC{0}}inducētās mutācijas ir visuresošas vēža gadījumā un var veicināt kanceroģenēzi, aktivizējot onkogēnus vai inaktivējot audzēja nomācējus (3. tabula). Piemēram, APOBEC3-inducētā FGFR3 S249C mutācija — visizplatītākā FGFR3 mutācija urīnpūšļa vēža gadījumā — izraisa kodētā augšanas faktora receptora konstitutīvu aktivāciju, lai veicinātu šūnu proliferāciju [127, 128]. Lai gan citos audzēju veidos tas retāk atkārtojas, S249C ir konstatēts arī plaušu, dzemdes kakla un galvas un kakla vēža gadījumā [129–132]. Papildus receptoru aktivizēšanai APOBEC{11}}inducētās mutācijas var ietekmēt pakārtotos signālu ceļus, radot ļoti onkogēnas mutācijas sinerģijas. Te APOBEC3-inducētā PIK3CA E545K mutācija, piemēram, izraisa augšanu veicinošā PI3K ceļa novirzes aktivāciju, un tā ir konstatēta urīnpūšļa, krūšu, dzemdes kakla, kolorektālo, barības vada, galvas un kakla un plaušu audzējos [39, 132–137]. Ļoti līdzīga PIK3CA E542K mutācija ir konstatēta urīnpūšļa, krūts, dzemdes kakla, kolorektālā, barības vada, galvas un kakla un plaušu vēža gadījumā [39, 132, 133, 135, 137–140]. APOBEC3-inducētas un citas onkogēnu aktivizējošas mutācijas var ļaut vēža šūnām nekontrolēti vairoties papildu mutāciju klātbūtnē audzēja supresoru gēnos, no kurām dažas rodas APOBEC3-mediētas mutaģenēzes rezultātā. Piemēram, inaktivējošā R505G FBXW7 mutācija ir attiecināma uz APOBEC3, un tā ir atklāta HNSCC, augšējā gremošanas trakta vēža, urīnceļu vēža un plaušu vēža gadījumā [132, 143]. Subklonālas APOBEC{36}}inducētas mutācijas ir novērotas arī audzēju nomācošos gēnos PTEN un TP53 urīnpūšļa, krūts, galvas un kakla un plaušu audzējos [148]. Citi mutācijas procesi var arī inaktivēt audzēja nomācējus, un augsta APOBEC3 aktivitāte var radīt selektīvu spiedienu, kas veicina šādas mutācijas. APOBEC3 rada lielu kopējo audzēja mutāciju slogu, tāpēc šūnas ar traucētu DNS bojājumu reakciju (DDR) audzēja nomācēju mutāciju dēļ, visticamāk, novērsīs apoptozi un turpinās proliferāciju. Attiecīgi TP53 mutācijas, kuras galvenokārt nav APOBEC{42}}inducētas, bija biežākas urīnpūšļa vēža, plaušu adenokarcinomu un B-šūnu limfomas šūnu līnijās ar lielu APOBEC{44}}inducēto mutāciju slodzi [46, 89 , 149]. Tāpat augsta APOBEC3B ekspresija ir saistīta ar vairāk p53 mutāciju krūts vēža un virsnieru garozas karcinomas gadījumā [22, 44]. Papildus atlases spiedienam šo tendenci var izraisīt augstāka APOBEC3 ekspresija p53-mutētos audzējos, jo p53 var nomākt APOBEC3B transkripciju caur p21 un DREAM proteīniem [150].
3. tabula Atkārtotas APOBEC{1}}izraisītas somatiskās mutācijas un kopiju skaita izmaiņas vēža gadījumā

Atkārtota APOBEC3 izraisīta nekodējoša mutācija
Latoriskie reģioni arī ir ļoti recidivējoši un var veicināt audzēja attīstību, modulējot ar vēzi saistītu gēnu ekspresiju (3. Piemēram, daudzi urīnpūšļa un krūts audzēji satur APOBEC3-inducētus "dvīņu mutāciju karstos punktus" PLEKHS1 un TBC1D12 promotoros, kas ir potenciāli onkogēni, kas saistīti ar invazīvu slimību un sliktu prognozi [33, 144, 147, 151, 152 ]. APOBEC3-inducētas ADGR6/GPR126 pastiprinātāja mutācijas, kas saistītas ar angioģenēzi, ir konstatētas arī urīnpūšļa vēža gadījumā [33, 145]. Citi gēni ar nekodējošām mutācijām, kas attiecināmas uz APOBEC3 urīnpūšļa vēža gadījumā, ir LEPROTL1 un, iespējams, audzēja nomācējs WDR74 [144, 153, 154]. Turklāt daudzām T-šūnu akūtām limfoblastiskām leikēmijām ir APOBEC{24}}inducēta mutācija augšpus onkogēna LMO1 transkripcijas sākuma vietas [146]. Vairākas šādas mutācijas tika konstatētas funkcionālas un tām ir potenciāla onkogēna loma krūts vēža gadījumā [155]. Tomēr nav atklāts, kas izraisa APOBEC3-mediētu mutaģenēzi nekodējošos starpgēnos un promotoru reģionos, taču tas, iespējams, notiek DNS replikācijas un transkripcijas iniciācijas laikā.
Papildus punktu mutāciju ģenerēšanai regulējošajos reģionos APOBEC3 var vēl vairāk traucēt gēnu ekspresiju, veicinot palielinātu onkogēnu kopiju skaitu (3. Piemēram, augstāka APOBEC3 ekspresija ir saistīta ar palielinātu vairāku Ras / MAPK regulējošo gēnu, piemēram, ATP2B4, MAPKAPK2 un USP15, kopiju skaita variāciju gliomā [51]. EGFR un CDK4 — abi zināmie onkogēni — amplifikācija ir novērota arī APOBEC{9}}augstas gliomas gadījumā [51]. Mehānismi, ar kuriem APOBEC3 atvieglo kopiju skaita izmaiņas, joprojām nav zināmi. Tomēr ir ticams, ka APOEBC3-inducētās kateegis veicina hromosomu nestabilitāti un divvirzienu pārtraukumus, radot iespējas kopiju skaita izmaiņām [156, 157].

Cistanche tubulosa-Antitumor priekšrocības
Audzēja evolūcija
Although some APOBEC3-induced mutations are likely important for initial tumor formation, many occur later in tumor evolution. Supporting this paradigm, episodic bursts of APOBEC3-mediated mutagenesis were observed during prolonged culture of numerous cancer cell lines [81, 112]. This repeated APOBEC3 activity can create a high overall tumor mutation burden and fuel subclone heterogeneity in a tumor context. Accordingly, APOBEC3s have been identified as primary drivers of subclonal mutations in bladder, breast, head neck, and lung cancers [48, 148]. In bladder cancer, over 45% of subclonal mutations in driver genes may be attributable to APOBEC3s [148]. Additionally, APOBEC3-induced mutation load has been strongly associated with tumor heterogeneity in metastatic thoracic cancers [89]. APOBEC3-induced tumor heterogeneity can promote resistance to cancer therapies. While the continued acquisition of signatures 2 and 13 is often part of natural tumor evolution, chemotherapy treatment may further fuel APOBEC3-mediated mutagenesis by triggering APOBEC3 expression and inducing DNA damage [1, 81, 90, 91]. Specific therapy resistance mutations can also arise due to APOBEC3 activity. For example, the APOEBC-induced MEK2 L46F mutation may confer resistance to BRAF inhibitors such as vemurafenib and dabrafenib in melanoma [82, 142]. In lung cancer, the potentially APOBEC3-induced C>T EGFR T790 mutācija var veicināt rezistenci pret EGFR inhibitoriem gefitinibu un erlotinibu [82, 141]. Tāpat dažas APOEBC3-inducētas mutācijas, kas novērotas recidivējošas refraktāras multiplās mielomas gadījumā, var veicināt terapijas rezistences iegūšanu [158]. Nemutagēni ceļi APOBEC{5}}inducētās mutācijas ir nozīmīgi audzēja ģenēzes virzītājspēki, taču APOBEC3 var arī ietekmēt vēzi, izmantojot nemutagēnus ceļus. Piemērojot šo ceļu nozīmi, hepatocelulārās karcinomas pētījums atklāja, ka katalītiski neaktīvā APOBEC3B pārmērīga ekspresija palielināja šūnu proliferāciju, šūnu migrāciju un šūnu invāziju in vitro [159]. K-Ras mutāciju klātbūtnē APOEBC3A var veicināt arī no STING atkarīgas metastāzes un hromosomu nestabilitāti, pamatojoties uz aizkuņģa dziedzera kanāla adenokarcinomas peles modeli [157]. Katalītiski neaktīvā APOBEC3B pārmērīga ekspresija ir saistīta arī ar biežāku "G1 aizbēgšanu", kas liecina, ka APOBEC3B veicina šūnu cikla disregulāciju [159]. Līdzīga APOBEC3B izraisīta šūnu cikla progresēšana ir novērota urīnpūšļa vēža gadījumā [159, 160]. APOBEC3s var arī kavēt šūnu nāvi, izmantojot vairākus mehānismus: tika pierādīts, ka APOBEC3G inhibē anoikis, aktivizējot Akt aizkuņģa dziedzera vēža gadījumā, un APOBEC3B var samazināt šūnu nāvi kuņģa vēža gadījumā, inhibējot PDCD2 funkciju un pazeminot ATM un Chk1/2 aktivitāti [38, 49]. Turklāt APOBEC3 var ietekmēt onkogēnu un audzēju nomācēju ekspresiju, izmantojot epiģenētiski saistītus mehānismus. Piemēram, ir pierādīts, ka APOBEC3B izraisa estrogēnu receptoru (ER) pārmērīgu ekspresiju krūts vēža gadījumā, izmantojot pārejošu hromatīna pārveidošanu [161]. Sniedzot papildu pierādījumus par APOBEC3-mediētu epiģenētisko regulējumu, augsta APOBEC3B ekspresija ir saistīta ar lielāku LINE1 metilēšanu (globālās DNS metilēšanas aizstājējs) barības vada vēža gadījumā [39].
Audzēja imūnās mikrovides modulācija
APOBEC3 var ietekmēt arī audzēja augšanu, izmantojot nemutagēnus ceļus, kas veido audzēja imūno mikrovidi (4. APOBEC3 ir imūnsupresīvi dažu vēža veidu gadījumā, un augstāka APOBEC3B ekspresija ir saistīta ar mazāku imūno šūnu infiltrāciju virsnieru garozas karcinomas un kuņģa vēža gadījumā [37, 162]. APOBEC3 ekspresija ir saistīta arī ar lielāku imūnsupresīvo mediatoru, piemēram, no mieloīdiem nomācošu šūnu (MDSC) un ar audzēju saistīto makrofāgu (TAM) infiltrāciju hepatocelulārās karcinomas peles modelī [163]. Citos vēža veidos ir novērots pretējs efekts, jo APOBEC3 veicina imūnsistēmas aktivāciju. Pan-vēža analīzē augsta APOBEC3B ekspresija bija saistīta ar paaugstinātu imūnsistēmas aktivāciju ādas melanomas un krūts vēža gadījumā [162]. Papildu pētījumi par krūts vēzi ir atklājuši līdzīgus rezultātus. Augsta APOBEC3B ekspresija ir saistīta ar vairāk audzēju piepūšošiem limfocītiem, un APOBEC3B indukcija izraisīja spēcīgu T šūnu mediētu imūnreakciju peles modelī [164, 165]. APOBEC3C-H līmenis korelēja arī ar lielāku CD8+ T šūnu skaitu audzēja mikrovidē, palielinātu T šūnu receptoru daudzveidību un lielāku citolītisko aktivitāti [48, 64]. Līdzīga imūnsistēmas aktivācija ir novērota urīnpūšļa vēža gadījumā, vairākos pētījumos atklājot pastiprinātus imūnsistēmas parakstus un interferona signālus APOBEC{26}}augsta līmeņa audzējos [35, 46, 160]. Plaušu vēža gadījumā T šūnu izraisīta imūnsistēmas aktivācija bija saistīta ar augstu APOBEC3B ekspresiju vai augstu APOBEC{32}}inducētu mutāciju slodzi [36, 166]. Olnīcu vēža gadījumā paaugstināta APOBEC3B un APOBEC3G ekspresija ir saistīta ar lielāku imūno šūnu infiltrāciju [41, 167]. Lai gan nav pašā audzējā, ir pierādīts, ka palielināta APOBEC3A ekspresija maina makrofāgu polarizāciju uz pro-iekaisumu veicinošu, imunitāti aktivizējošu stāvokli [168].
4. tabula APOBEC3 imūnmodulējošā iedarbība pēc vēža veida

APOBEC3 klīniskā un terapeitiskā nozīme vēža gadījumā
Saistība ar sliktu prognozi vairākiem vēža veidiem
Dažu vēža veidu imūnsupresija var sinerģēt ar APOBEC{0}}mediētu mutaģenēzi, ļaujot onkogēnām mutācijām uzkrāties un veicināt audzēju veidošanos, vienlaikus novēršot saimniekorganisma imūnreakciju. Saskaņā ar šo modeli pētījumos ar virsnieru garozas karcinomu un kuņģa vēzi, kas abi liecina par imūnsupresiju ar APOBEC3, ir konstatēts, ka augstāka APOBEC3B ekspresija ir saistīta ar īsāku dzīvildzi (4. un 5. tabula) [37, 38, 44]. Paaugstināta APOBEC3 ekspresija ir saistīta arī ar nelabvēlīgiem klīniskiem iznākumiem nazofaringeālās karcinomas, skaidras šūnu nieru karcinomas un neiroendokrīno audzēju gadījumā, lai gan maz ir zināms par APOBEC3-mediēto imūnsistēmu šajos vēža veidos (5. tabula) [55, 169]. . Augsta APOBEC3 ekspresija vai izraisīts mutāciju slogs var arī paredzēt nelabvēlīgus rezultātus krūts vēža gadījumā, lai gan dažos ziņojumos ir konstatēti pretrunīgi rezultāti (5. Tā kā APOBEC3s izraisa imūnsistēmas aktivāciju krūts vēža gadījumā, papildu faktoriem ir jāpārvar šī pastiprinātā imūnreakcija, lai veicinātu audzēja ģenēzi (. 4). Lielāka estrogēnu receptoru aktivācija (ER) ir iespējams mehānisms, jo ir pierādīts, ka APOBEC3B veicina ER pārmērīgu ekspresiju krūts vēža gadījumā [161]. Attiecīgi saistība starp augstu APOBEC3B ekspresiju un nelabvēlīgiem klīniskiem rezultātiem ir spēcīgāka ER+ slimībā (5. tabula).
5. tabula APOBEC3 ekspresijas un APOBEC3-inducēto mutāciju saistība ar klīniskiem rezultātiem pēc vēža veida

5. tabula (turpinājums)


4. attēls APOBEC{1}}inducēto faktoru ietekme uz prognozi dažādiem vēža veidiem ir atšķirīga. APOBEC3 var ietekmēt audzēja veidošanos, izmantojot mutagēnus un nemutagēnus ceļus, kam var būt pretēja ietekme uz slimības gaitu. Šo efektu relatīvais stiprums var noteikt APOBEC3 prognostisko nozīmi, izskaidrojot APOBEC3 atšķirīgo klīnisko ietekmi atkarībā no vēža veida (5. tabula). Tiek parādīti konkrētu vēža veidu piemēri.
APOBEC3 ir līdzīga kaitīga ietekme tradicionāli ārstētos plaušu vēža gadījumos. Ārpus imūnterapijas konteksta vairākos pētījumos ir atklāts, ka APOBEC3B ekspresija vai inducēta mutāciju slodze ir saistīta ar agresīvu slimību vai sliktu prognozi (5. Plaušu vēža gadījumā papildu faktori, piemēram, APOBEC3-inducētas mutācijas, kas veicina terapijas rezistenci, visticamāk, atsver APOBEC3-mediēto imūno aktivāciju, lai veicinātu sliktus klīniskos rezultātus [141] (4. attēls).
Saistība ar labvēlīgiem imūnterapijas un platīna terapijas rezultātiem
Plaušu vēža gadījumā APOBEC{0}}mediētā imūnsistēmas aktivācija ir saistīta ar uzlabotu reakciju uz imūnās kontrolpunkta blokādes terapiju (5. tabula). Līdzīgi rezultāti ir novēroti imūnterapijas reakcijai krūts, urīnpūšļa un plaušu vēža gadījumā, kas visi ir parādījuši imūnsistēmas aktivāciju ar APOBEC3 (4. un 5. tabula). Šajos vēža gadījumos APOBEC3-mediētā imūnsistēmas aktivācija, iespējams, sinerģē ar augstu APOBEC3-inducēto neoantigēna slodzi, lai veicinātu imūnterapijas reakciju (4. att.) [164, 187]. APOBEC3 ir saistīti arī ar uzlabotu reakciju uz imūnterapiju kuņģa vēža gadījumā, taču šis vēža veids paradoksālā kārtā ir parādījis imūnsupresiju ar APOBEC3 [37]. Lai gan pašreizējie dati ir nedaudz neskaidri, APOBEC3 var arī veicināt urīnpūšļa vēža izdzīvošanas uzlabošanos pat ar tradicionālo ķīmijterapiju (5. Urīnpūšļa vēzi bieži ārstē ar DNS alkilējošo līdzekli cisplatīnu, kam var būt pastiprināta aktivitāte APOBEC3 klātbūtnē. Mehāniski APOBEC3 var veicināt cisplatīna reakciju, deaminējot zāļu izraisītos ekstraspirālos citozīnus, un APOBEC3B var izraisīt turpmāku genotoksisku iedarbību ķīmijterapijas izraisītas neatbilstības novēršanas laikā [188]. Turklāt APOBEC3 var radīt lielu fona mutāciju slodzi, kas sensibilizē šūnas pret papildu cisplatīna izraisītiem DNS bojājumiem. Tomēr APOBEC3 klīniskais ieguvums urīnpūšļa vēža gadījumā var aprobežoties ar slimības vēlāku stadiju, jo augstāka APOBEC3B ekspresija var veicināt slimības progresēšanu no neinvazīvas uz muskuļu invazīvu slimību [1]. APOBEC3 ir līdzīgi saistīti ar uzlabotu klīnisko iznākumu olnīcu vēža gadījumā, ko ārstē kā urīnpūšļa vēzi, izmantojot uz platīnu balstītas terapijas cisplatīnu un karboplatīnu (5. tabula). Piemēram, augsta APOBEC3-inducēta mutāciju slodze bija saistīta ar uzlabotu bezprogresēšanas un vispārējo dzīvildzi pacientiem ar skaidru šūnu olnīcu karcinomu [186]. Augsta APOBEC3 ekspresija korelēja ar uzlabotu dzīvildzi augstas kvalitātes serozo olnīcu audzēju apakštipos [41, 42, 167]. Tāpat kā urīnpūšļa vēža gadījumā, šie ar APOBEC{42}}saistītie izdzīvošanas ieguvumi olnīcu vēža gadījumā, iespējams, izriet no imūnsistēmas aktivizēšanas un paaugstinātas reakcijas uz platīnu saturošām terapijām (4. att.).
APOBEC3 kā biomarķieri
APOBEC3 ekspresija un APOBEC3-izraisītā mutāciju slodze ir saistīta ar klīniskiem rezultātiem vairāku vēža veidu un ārstēšanas kontekstos, kas racionalizē to izmantošanu kā prognostiskos biomarķierus (5. tabula). Vairākos pētījumos par cisplatīnu/karboplatīnu ārstētiem vēža veidiem ir ziņots par saistību starp APOBEC3 un labvēlīgiem iznākumiem, tāpēc APOBEC3 ir pelnījuši turpmāku novērtējumu kā biomarķierus šai izplatītajai ķīmijterapijai [41, 46, 61, 167, 170, 186]. APOBEC3 var izmantot arī kā imūnterapijas biomarķierus, ņemot vērā esošos datus par plaušu, urīnpūšļa un krūts vēzi [37, 160, 166, 174, 180, 181]. Papildus šīm klīniskajām asociācijām vairāki pirmsklīniskie pētījumi ir apstiprinājuši APOBEC3 kā potenciālu uz platīnu balstītu terapiju un imūnterapijas biomarķierus (6. Turklāt APOBEC3 varētu būt īpaši auglīgi biomarķieri mērķtiecīgām terapijām (6. Augsta APOBEC3B ekspresija ir saistīta ar sliktu reakciju uz Raf inhibitoriem gliomas gadījumā, un noteiktas APOBEC{26}}inducētas mutācijas var paredzēt rezistenci pret Raf inhibitoriem un EGFR inhibitoriem attiecīgi multiplās mielomas un plaušu vēža gadījumā [82, 158]. ER+ krūts vēža gadījumā augsta APOBEC3B ekspresija var paredzēt rezistenci pret endokrīno terapiju tamoksifēnu [192]. Pamatojoties uz preklīniskajiem pētījumiem, APOBEC3 var arī paredzēt labvēlīgu reakciju uz mērķtiecīgu replikācijas kontrolpunktu un DDR inhibitoriem, iespējams, sintētisku ievainojamību dēļ, kas izraisa citotoksisku DNS bojājumu [52, 99, 157, 191]. Kopumā ir pārliecinoši pierādījumi tam, ka pacientu audzēju pārbaude attiecībā uz APOBEC3 ekspresiju vai izraisītu mutāciju slogu varētu vadīt terapijas lēmumus. Tomēr pastāv ievērojama atšķirība no laboratorijas līdz klīnikai, un būs svarīgi noteikt nozīmīgus parametrus, kas definē "APOBEC pozitivitāti". Šim nolūkam turpmākajos pētījumos būs jānovērtē APOEBC3 ekspresijas vai mutācijas parakstu rādītāji, kurus galu galā var izmantot klīniskajos pētījumos. Vērtēšanas un profilēšanas sistēmas attiecībā uz PD-L1/PD1 un kopējo audzēja mutāciju slogu var izmantot kā vadlīnijas [195–199].
APOBEC3 inhibīcija vēža terapijai
Tā kā APOBEC3 var veicināt audzēja veidošanos, izmantojot mutagēnus, nevis mutagēnus ceļus, varētu būt noderīgi inhibēt APOBEC3 specifiskos, bet, iespējams, daudzos onkogēnos apstākļos (6. tabula). Piemēram, APOBEC3 inhibitori potenciāli varētu novērst ne-muskuļu invazīva urīnpūšļa vēža progresēšanu par muskuļu invazīvu slimību, kurai ir lielāks APOBEC{6}}inducēto mutāciju slogs [1, 200]. APOBEC3 inhibitori varētu arī palēnināt no STING atkarīgās metastāzes, īpaši kombinācijā ar jauniem STING inhibitoriem [157, 201]. APOBEC3G inhibēšana varētu arī atbalstīt anoikis, jo ir pierādīts, ka APOBEC3 izjauc šo šūnu nāves veidu [49]. Turklāt APOBEC3 inhibitorus varētu izmantot īpaši vēža gadījumos, kur APOBEC3 prognozē sliktu prognozi, lai ierobežotu audzēja attīstību, subklonu neviendabīgumu un ķīmijterapijas rezistenci [82, 148]. APOBEC3 inhibitori pašlaik nav pieejami klīniskai lietošanai, taču jaunākie sasniegumi APOBEC3 enzīmu molekulāro struktūru atrisināšanā ir radījuši svarīgu pamatu šīs zāļu klases iespējamai attīstībai [202]. Ir pierādīts, ka vairāki savienojumi ar kateholu daļām inhibē APOBEC3G, un ķīmiskās modifikācijas atbalsta ierobežotāku APOBEC3A mērķēšanu [203]. Ir ziņots arī par nesen identificētu mazas molekulas inhibitoru, kas var mērķēt uz AID, APOBEC3A un APOBEC3B katalītiskajām kabatām, un tas var vadīt katram APOBEC enzīmam raksturīgu inhibitoru izstrādi [205]. Papildus mazo molekulu inhibitoriem citas potenciālās stratēģijas APOBEC3 aktivitātes samazināšanai ietver gēnu klusināšanas terapiju, ssDNS saturošus 2′-deoksizebularīna analogus un alternatīvus savienošanas modulatorus [204]. Pēdējā pieeja ir iespējama, jo dažas APOBEC3 izoformas nav mutagēnas, un ir pierādīts, ka SF3B1 inhibīcija maina ekspresiju uz nemutagēnu APOBEC3B izoformu, izraisot 5. eksona izlaišanu [1]. Turklāt ir pierādīts, ka replikācijas stresa mazināšana, izmantojot nukleozīdu papildināšanu un chk1 inhibīciju, samazina APOBEC3B ekspresiju in vitro [90].
6. tabula APOBEC3 biomarķieris un terapeitiskais potenciāls

6. tabula (turpinājums)

APOBEC3 aktivizēšana vēža terapijai
Lai gan APOBEC3 inhibēšana var būt noderīga daudzu vēža veidu gadījumā, šķietami pretintuitīvā stratēģija APOBEC3 aktivitātes palielināšanai noteiktos kontekstos var piedāvāt unikālu terapeitisku iespēju. Piemēram, mērķtiecīga APOEBC3 pārmērīga ekspresija var būt izdevīga ar imūnterapijas līdzekļiem. Atbalstot šo pieeju, ir pierādīts, ka APOBEC3B indukcija palielina reakciju uz imūnās kontrolpunkta blokādes terapiju melanomas un krūts vēža peļu modeļos [164, 187]. Šī APOBEC3-izraisītā sensibilizācija var notikt, izmantojot vairākus sinerģiskus ceļus (5. att.). Pirmkārt, APOBEC3 var radīt lielu kopējo audzēja mutāciju slogu, izraisot neoepitopu veidošanos un imūnsistēmas aktivāciju dažos audzēju veidos [187]. Otrkārt, APOBEC{10}}mediētā PD-L1 ekspresijas palielināšanās var arī uzlabot imūnterapijas reakciju [64, 171, 189]. Mehāniski APOBEC3 var veicināt PD-L1 ekspresiju, izmantojot DNS bojājumus, kas aktivizē JNK/c-JUN signalizāciju [190]. Sinerģija starp APOBEC3 un IFN- var vēl vairāk palielināt PD-L1 ekspresiju vēža šūnās un papildus uzlabot sensibilizāciju pret imūnterapiju [206, 207]. Tā kā APOBEC3 izraisa augstu DNS bojājumu līmeni, to mērķtiecīga pārmērīga ekspresija vēža šūnās var būt arī citotoksiska [208]. APOBEC3A aktivizēšana var īpaši izraisīt apoptozi in vitro, jo tai ir visaugstākā deaminācijas aktivitāte starp APOBEC3 [43, 108]. Turklāt mērķtiecīga APOBEC3 pārmērīga ekspresija var būt īpaši citotoksiska audzējiem ar pavājinātu uracila glikozilāzes funkciju vai pamata vietas sensora HCES zudumu — mutācijām, kas radītu sintētisku ievainojamību [209, 210]. APOBEC{36}}aktivizējošās terapijas var ietekmēt arī genotoksisku zāļu lietošanu. Piemēram, APOBEC3 induktori varētu sagatavot audzējus, lai reaģētu uz platīna bāzes ķīmijterapiju un DDR inhibitoriem. Kā koncepcijas pierādījumu in vitro krūts vēža pētījums atklāja, ka APOBEC3 inducēšana šūnu līnijās ar zemu sākotnējo ekspresiju ievērojami palielināja reakciju uz cisplatīnu [188]. Tika arī pierādīts, ka APOBEC3 pārmērīga ekspresija palielina reakciju uz mērķtiecīgiem ATR un Chk1/2 inhibitoriem akūtas mieloleikozes un osteosarkomas šūnu līnijās [52, 191]. Līdzīgi, APOBEC3B pārmērīga ekspresija sensibilizēja p53-deficīta šūnas pret CHEK1/2, WEE1 un PARP inhibīciju [99]. Paaugstināta jutība pret PARP inhibitoriem tika novērota arī ar APOBEC3A regulēšanu aizkuņģa dziedzera vēža šūnās [157]. Neskatoties uz terapeitisko potenciālu dažos kontekstos, APOBEC3 indukcija var neveicināt imūnterapijas reakciju visos vēža veidos, īpaši audzējos, kur augstāka APOBEC3 ekspresija ir saistīta ar imūnsupresiju (4. APOBEC{57}}pastiprinošās zāles arī ir jāizpēta piesardzīgi, ņemot vērā jaunu draiveru mutāciju risku, palielinātu audzēju neviendabīgumu un ķīmijterapijas rezistenci. Tomēr APOBEC3 aktivitātes aktivizēšana un kavēšana ir daudzsološas pieejas, kas varētu radīt jaunas ārstēšanas iespējas rītdienas klīniskajai ainavai.

5. att. APOBEC3 aktivizēšana, lai pastiprinātu reakciju uz imūnterapiju. APOBEC3 aktivitātes palielināšana varētu palielināt imūnterapijas reakciju, veidojot neoepitopu, palielinot PD-L1 ekspresiju un imūnsistēmas aktivāciju, kā tas ir pierādīts pētījumos, izmantojot peles modeļus.
Secinājumi
APOBEC3 ir galvenie mutagēnie vēža izraisītāji, un APOBEC3A un APOBEC3B, iespējams, ir nozīmīgākie mutatori starp APOBEC3 virsģimeni. APOBEC3A un APOBEC3B ir pārmērīgi izteikti daudzos vēža veidos, un to ekspresija korelē ar lielāku APOBEC{6}}izraisītu mutāciju slodzi. Tomēr atlikušās deaminācijas aktivitātes noteikšana pēc abu ģimenes locekļu izslēgšanas liecina, ka arī citi APOBEC3 ir aktīvi mutatori. Uzlabota izpratne par to, kā katrs APOBEC3 veicina vēzi, vēl vairāk noskaidros audzēja etioloģiju un var kļūt terapeitiski nozīmīga, lai mērķētu uz APOBEC3.

6. attēls APOBEC{1}}mediētās mutaģenēzes cēloņi, sekas un klīniskie aspekti vēža gadījumā. Dažādi eksogēni un endogēni faktori var izraisīt APOBEC3, kas pēc tam var ietekmēt vēža augšanu, izmantojot mutagēnus un nemutagēnus ceļus. Šie APOBEC{4}}mediētie efekti var ietekmēt klīniskos rezultātus un būt nozīmīgi gan pašreizējā, gan turpmākajā terapeitiskajā vidē.
Plašāka izpratne par faktoriem, kas izraisa APOBEC{0}}mediētu mutaģenēzi, varētu arī uzlabot vēža profilakses stratēģijas. Pašlaik zināmie APOBEC3 ekspresijas izraisītāji ir vīrusu infekcija, iekaisums un noteiktas genotoksiskas zāles, lai gan palielināta ekspresija viena pati var neizraisīt augstu mutaģenēzes līmeni (6. attēls). Divu faktoru modelī ssDNS, kas var rasties no genotoksisku zāļu iedarbības, genoma nestabilitātes utt., rada APOBEC3 galvenos mutācijas substrātus un atvieglo mutaģenēzi. Lai gan mutaģenēze ir galvenā APOBEC3 lomai vēža ārstēšanā, APOBEC3 var veicināt arī audzēja veidošanos, izmantojot nemutagēnus ceļus, piemēram, šūnu cikla modulāciju, epiģenētisko regulējumu, STING atkarīgās metastāzes un šūnu nāves inhibīciju (6. attēls). Turklāt APOBEC3 var modulēt audzēja imūno mikrovidi, un iedarbība atšķiras atkarībā no vēža veida. APOBEC3 ir saistīti ar imūnsistēmas aktivāciju krūts, plaušu un urīnpūšļa vēža gadījumā, savukārt APOBEC{12}}mediēta imūnsupresija ir novērota aknu vēža, kuņģa vēža un virsnieru garozas karcinomas gadījumā. APOBEC3 imūnmodulējošā iedarbība, iespējams, ietekmē slimības gaitu, taču APOBEC{15}mediētā imūnsistēmas aktivācija ne vienmēr uzlabo klīniskos rezultātus, jo citiem faktoriem, piemēram, vadītāja mutācijām un šūnu nāves kavēšanai, var būt pretēja ietekme. APOBEC3-mediētā imūnsistēmas aktivācija, palielināta neoepitopu slodze un augstāka PD-L1 ekspresija var sinerģēt, lai pastiprinātu reakciju uz imūnterapiju (6. attēls). APOBEC3s var arī atvieglot reakciju uz platīnu saturošām terapijām. Vairākas klīniskās asociācijas, kā arī pirmsklīniskie pētījumi liecina, ka APOBEC3 varētu izmantot kā biomarķierus pašlaik pieejamām imūnterapijām un ķīmijterapijām, savukārt jaunas APOBEC3 aktivācijas stratēģijas varētu stimulēt noteiktus audzējus, lai palielinātu terapeitisko reakciju (6. att.).

Citanche tubulosa priekšrocības- stiprināt imūnsistēmu
Turpretim APOBEC3 inhibēšana var palēnināt audzēja attīstību, samazināt subklonu neviendabīgumu un novērst terapijas rezistenci dažos vēža veidos un kontekstā ar konkrētiem ārstēšanas veidiem. APOBEC3 tiek neregulēti daudzos un lielai daļai cilvēku audzēju, tāpēc pētījumiem šajās jomās ir liels potenciāls un tie varētu radīt jaunas ārstēšanas iespējas daudziem vēža veidiem.
Atsauces
1. Rouf Bandday A, Onabajo OO, Lin SHY, Obajemu A, Vargas JM, Delviks Frankenberry KA u.c. Mērķtiecīga APOBEC3B dabiskā savienojuma plastiskums ierobežo tā ekspresiju un mutagēno aktivitāti. Commun Biol.
2. 2021;4(1):386. Ebrahimi D, Richards CM, Carpenter MA, Wang J, Ikeda T, Becker JT u.c. Ģenētiskais un mehāniskais pamats APOBEC3H alternatīvai splicēšanai, retrovīrusu ierobežošanai un HIV-1 proteāzes pretdarbībai. Nat Commun.
3. 2018;9(1):4137. Harari A, Ooms M, Mulder LCF, Simon V. Polimorfismi un savienojuma varianti ietekmē cilvēka APOBEC3H pretretrovīrusu aktivitāti. Dž Virols. 2009;83(1):295–303.
4. Lassen KG, Wissing S, Lobritz MA, Santiago M, Greene WC. Divu APOBEC3F savienojuma variantu identificēšana ar HIV-1 pretvīrusu aktivitāti un kontrastējošu jutību pret Vif*. J Biol Chem. 2010;285(38):29326–35.
5. Salter JD, Bennett RP, Smith HC. APOBEC proteīnu saime: to vieno struktūra, atšķirīgas funkcijas. Trends Biochem Sci. 2016;41(7):578–94.
6. Chaudhuri J, Evans T, Kumar R, DiMenna L. Aktivācijas izraisītas citidīna deamināzes (AID) bioloģiskā funkcija. Biomed J. 2014;37(5):269.
7. Chen SH, Habib G, Yang CY, Gu ZW, Lee BR, Weng SA u.c. Apolipoproteīns B-48 ir ziņojuma RNS produkts ar orgānam specifisku kadrā esošu stopkodonu. Zinātne. 1987;238(4825):363–6.
8. Powell LM, Wallis SC, Pease RJ, Edwards YH, Knott TJ, Scott J. Jauns audu specifiskās RNS apstrādes veids ražo apolipoproteīnu-B48 zarnās. Šūna. 1987;50(6):831–40.
9. Hirano K, Min J, Funahashi T, Baunoch DA, Davidson NO. Cilvēka aerobā-1 gēna raksturojums: ekspresija kuņģa-zarnu trakta audos, ko nosaka alternatīva savienošana ar jauna saīsināta peptīda ražošanu. J Lipid Res. 1997;38(5):847–59.
10. Hariss RS, Dudlijs JP. APOBEC un vīrusu ierobežošana. Virusoloģija. 2015;479–480:131–45.
11. Silvas T, Šifers, CA. APOBEC3: DNS rediģējošās cilvēka citidīna deamināzes. Protein Sci. 2019. gads. https://doi.org/10.1002/pro.3670.
12. Yu Q, König R, Pillai S, Chiles K, Kearney M, Palmer S u.c. APOBEC3G vienas virknes specifika nosaka HIV genoma mīnus virknes deamināciju. Nat Struct Mol Biol. 2004;11(5):435–42.
13. Chan K, Sterling JF, Roberts SA, Bhagwat AS, Resnick MA, Gordenin DA. Bāzes bojājumi vienas virknes DNS ir pamatā in vivo hipermutācijai, ko izraisa visuresošs vides aģents. PLoS Genet. 2012;8(12):e1003149.
14. Hoopes JI, Cortez LM, Mertz TM, Malc EP, Mieczkowski PA, Roberts SA. APOBEC3A un APOBEC3B DNS replikācijas laikā deaminē atpalikušo virknes veidni. Cell Rep. 2016;14(6):1273–82.
15. Lada AG, Kliver SF, Dhar A, Polev DE, Masharsky AE, Rogozin IB u.c. Transkripcijas koaktivatora Sub1 pārtraukšana izraisa APOBEC izraisīto klasteru mutāciju atkārtotu sadalījumu genoma mērogā aktīvos rauga gēnos. PLoS Genet. 2015;11(5):e1005217.
16. Seplyarskiy VB, Soldatov RA, Popadin KY, Antonarakis SE, Bazykin GA, Nikolaev SI. APOBEC izraisītās mutācijas cilvēka vēža gadījumā replikācijas laikā ir stipri bagātinātas atpalikušajā DNS virknē. Genome Res. 2016;26(2):174–82.
17. Buisson R, Langenbucher A, Bowen D, Kwan EE, Benes CH, Zou L u.c. Pasažieru karstā punkta mutācijas vēzī, ko izraisa APOBEC3A un mezomēroga genoma iezīmes. Zinātne. 2019; 364:6447.
18. McCann JL, Cristini A, Law EK, Lee SY, Tellier M, Carpenter MA u.c. R-cilpas homeostāze un vēža mutaģenēze, ko veicina DNS citozīna deamināze APOBEC3B. bioRxiv [internets]. 2021;2021.08.30.458235. Pieejams no: http://biorxiv.org/content/ early/2021/08/30/2021.08.30.458235.abstract.
19. Holtz CM, Sadler HA, Mansky LM. APOBEC3G citozīna deaminācijas karstos punktus nosaka gan secības konteksts, gan vienas virknes DNS sekundārā struktūra. Nucleic Acids Res. 2013;41(12):6139–48.
20. Hariss RS. APOBEC3B katalizētās mutaģenēzes molekulārais mehānisms un klīniskā ietekme krūts vēža gadījumā. Breast Cancer Res. 2015;17(1):8.
21. Refsland EW, Harris RS. Retroelementu ierobežošanas faktoru APOBEC3 saime. Berlīne: Springer; 2013. lpp. 1.–27.
22. Burns MB, Lackey L, Carpenter MA, Rathore A, Land AM, Leonard B u.c. APOBEC3B ir fermentatīvs mutāciju avots krūts vēža gadījumā. Daba. 2013;494(7437):366–70.
23. Chan K, Roberts SA, Klimczak LJ, Sterling JF, Saini N, Malc EP u.c. APOBEC3A hipermutācijas paraksts ir atšķirams no APOBEC3B fona mutaģenēzes paraksta cilvēka vēža gadījumā. Nats Ženē. 2015;47(9):1067–72.
24.KOSMISKAIS. 2022. gads.
25. Alexandrov LB, Kim J, Haradhvala NJ, Huang MN, Tian Ng AW, Wu Y u.c. Cilvēka vēža mutāciju parakstu repertuārs. Daba. 2020;578(7793):94–101.
26. Aleksandrovs LB, Nik-Zainal S, Wedge DC, Aparicio SAJR, Behjati S, Biankin A u.c. Cilvēka vēža mutācijas procesu paraksti. Daba. 2013;500(7463):415–21.
27. Roberts SA, Lawrence MS, Klimczak LJ, Grimm SA, Fargo D, Stojanov P u.c. APOBEC citidīna deamināzes mutaģenēzes modelis ir plaši izplatīts cilvēka vēža gadījumā. Nats Ženē. 2013;45(9):970–6.
28. Zou J, Wang C, Ma X, Wang E, Peng G. APOBEC3B, cilvēka vēža mutaģenēzes molekulārais virzītājspēks. Šūnu Biosci. 2017;7(1):29.
29. Teilors BJ, Niks Zaināls S, Vu YL, Stebbings LA, Raine K, Campbell PJ u.c. DNS deamināzes izraisa ar pārtraukumiem saistītus mutāciju dušas, kas ietver APOBEC3B un 3A krūts vēža kataegis. Elife. 2013;16:2.
30. Liu W, Newhall KP, Khani F, Barlow L, Nguyen D, Gu L u.c. Citidīna deamināze APOBEC3G veicina vēža mutaģenēzi un klonu attīstību urīnpūšļa vēža gadījumā. Cancer Res. 2022; 26:2651.
31. Aaltonen LA, Abascal F, Abeshouse A, Aburatani H, Adams DJ, Agrawal N u.c. Visu genomu vēža analīze. Daba. 2020;578(7793):82–93.
32. Bergstrom EN, Luebeck J, Petljak M, Khandekar A, Barnes M, Zhang T u.c. Vēža grupēto mutāciju kartēšana atklāj cDNS APOBEC3 mutaģenēzi. Daba. 2022;602(7897):510–7.
33. Langenbucher A, Bowen D, Sakhtemani R, Bournique E, Wise JF, Zou L u.c. Paplašināts APOBEC3A mutācijas paraksts vēža gadījumā. Nat Commun. 2021;12(1):1602.
34. Burns MB, Temiz NA, Harris RS. Pierādījumi par APOBEC3B mutaģenēzi vairāku cilvēku vēža gadījumos. Nats Ženē. 2013;45(9):977–83.
35. Kim H, Kim O, Lee MA, Lee JY, Hong SH, Ha US u.c. APOBEC3B ekspresijas prognostiskā ietekme metastātiskā urotēlija karcinomā un tās saistība ar audzēju infiltrējošām citotoksiskām T šūnām. Curr Oncol. 2021;28(3):1652–62.
36. Vans S, Dzja M, He Z, Liu XS. APOBEC3B un APOBEC mutācijas paraksts kā potenciālie paredzamie marķieri imūnterapijas reakcijai nesīkšūnu plaušu vēža gadījumā. Onkogēns. 2018;37(29):3924–36.
37. Xia S, Gu Y, Zhang H, Fei Y, Cao Y, Fang H u.c. Imūnsistēmas inaktivācija ar APOBEC3B bagātināšanu prognozē reakciju uz ķīmijterapiju un izdzīvošanu kuņģa vēža gadījumā. Onkoimunoloģija. 2021. gads. https://doi.org/10. 1080/2162402X.2021.1975386.
38. Zhang J, Wei W, Jin HC, Ying RC, Zhu AK, Zhang FJ. APOBEC3B loma kuņģa vēzī. Int J Clin Exp Pathol. 2015;8(5):5089–96.
39. Kosumi K, Baba Y, Ishimoto T, Harada K, Nakamura K, Ohuchi M u.c. APOBEC3B ir barības vada plakanšūnu karcinomas molekulāro izmaiņu enzīmu avots. Med Oncol. 2016;33(3):26.
40. Feng C, Zheng Q, Yang Y, Xu M, Lian Y, Huang J u.c. APOBEC3B augsta ekspresija gastroenteropankreātiskajos neiroendokrīnos audzējos un saistība ar limfas metastāzēm. Appl Immunohistochem Mol Morphol. 2019;27(8):599–605.
41. Rüder U, Denkert C, Alisa Kunze C, Jank P. APOBEC3B proteīna ekspresija un mRNS analīzes pacientiem ar augstas pakāpes serozu olnīcu karcinomu. Histol Histopathol. 2019;34:405–17.
42. Du Y, Tao X, Wu J, Yu H, Yu Y, Zhao H. APOBEC3B augšupregulācija neatkarīgi prognozē olnīcu vēža prognozi: kohortas pētījums. Cancer Cell Int. 2018;18(1):78.
43. Liu W, Ji H, Zhao J, Song J, Zheng S, Chen L u.c. Transkripcijas represijas un apoptoze ietekmē ietekmi
44. Gara SK, Tyagi MV, Patel DT, Gaskins K, Lack J, Liu Y u.c. GATA3 un APOBEC3B ir prognostiski marķieri virsnieru garozas karcinomas gadījumā, un APOBEC3B tieši transkripcijas veidā regulē GATA3. Oncotarget. 2020;11(36):3354–70.
45. Wagener R, Alexandrov LB, Montesinos-Rongen M, Schlesner M, Haake A, Drexler HG u.c. Mutācijas parakstu analīze B-šūnu limfomas šūnu līniju eksomās liecina, ka APOBEC3 ģimenes locekļi ir iesaistīti primārās efūzijas limfomas patoģenēzē. Leikēmija. 2015;29(7):1612–5.
46. Glaser AP, Fantini D, Wang Y, Yu Y, Rimar KJ, Podojil JR u.c. APOBEC mediētā mutaģenēze urotēlija karcinomā ir saistīta ar uzlabotu izdzīvošanu, mutācijām DNS bojājumu reakcijas gēnos un imūnreakciju. Oncotarget. 2018;9(4):4537–48.
47. Cortez LM, Brown AL, Dennis MA, Collins CD, Brown AJ, Mitchell D u.c. APOBEC3A ir ievērojama citidīna deamināze krūts vēža gadījumā. PLoS Genet. 2019;15(12):e1008545.
48. Asaoka M, Patnaik SK, Ishikawa T, Takabe K. Dažādiem APOBEC3 DNS mutatoru ģimenes locekļiem ir pretējas asociācijas ar krūts vēža ainavu. Am J Cancer Res. 2021;11:5111.
49. Wu J, Pan TH, Xu S, Jia LT, Zhu LL, Mao JS u.c. Vīrusa izraisītais proteīns APOBEC3G inhibē anoikis, aktivizējot Akt kināzi aizkuņģa dziedzera vēža šūnās. Sci Rep. 2015;5(1):12230. 50. Ding Q, Chang CJ, Xie X, Xia W, Yang JY, Wang SC u.c. APOBEC3G veicina aknu metastāzes kolorektālā vēža ortotopiskā peles modelī un prognozē cilvēka aknu metastāzes. J Clin izmeklēšana. 2011;121(11):4526–36.
51. Luo C, Wang S, Liao W, Zhang S, Xu N, Xie W u.c. APOBEC3 ģimenes regulēšana ir saistīta ar sliktu prognozi un ietekmē ārstēšanas reakciju uz Raf inhibitoriem zemas pakāpes gliomas gadījumā. Int J Mol Sci. 2021;22(19):10390.
52. Green AM, Budagyan K, Hayer KE, Reed MA, Savani MR, Wertheim GB u.c. Citozīna deamināze APOBEC3A sensibilizē leikēmijas šūnas pret DNS replikācijas kontrolpunkta kavēšanu. Cancer Res. 2017;77(17):4579–88.
53. Waters CE, Saldivar JC, Amin ZA, Schrock MS, Huebner K. FHIT zudumu izraisīts DNS bojājums rada optimālus APOBEC substrātus: ieskats APOBEC mediētā mutaģenēzē. Oncotarget. 2015;6(5):3409–19.
54. Sasaki H, Suzuki A, Tatematsu T, Shitara M, Hikosaka Y, Okuda K u.c. APOBEC3B gēna pārmērīga ekspresija nesīkšūnu plaušu vēža gadījumā. Biomed Rep. 2014;2(3):392–5.
55. Feng C, Zhang Y, Huang J, Zheng Q, Yang Y, Xu B. APOBEC3B un PD-L1/PD-1 prognostiskā nozīme nazofaringeālās karcinomas gadījumā. Appl Immunohistochem Mol Morphol. 2021;29(3):239–44.
56. Leonards B, Harts SN, Burns MB, Carpenter MA, Temiz NA, Rathore A u.c. APOBEC3B regulēšana un genoma mutāciju modeļi serozā olnīcu karcinomā. Cancer Res. 2013;73(24):7222–31.
57. Heller M, Prigge ES, Kaczorowski A, von Knebel Doeberitz M, Hohen Fellner M, Duensing S. APOBEC3A ekspresija dzimumlocekļa plakanšūnu karcinomā. Patobioloģija. 2018;85(3):169–78.
58. Petljak M, Dananberg A, Chu K, Bergstrom EN, Striepen J, von Morgen P, et al. APOBEC3 mutaģenēzes mehānismi cilvēka vēža šūnās. Daba. 2022;607(7920):799–807.
59. Petljak M, Maciejowski J. Ar APOBEC saistīto mutāciju molekulārā izcelsme vēža gadījumā. DNS remonts (Amst). 2020;94:102905.
60. Carpenter MA, Li M, Rathore A, Lackey L, Law EK, Land AM u.c. Metilcitozīns un normāla citozīna deaminācija ar svešā DNS restrikcijas enzīma APOBEC3A palīdzību. J Biol Chem. 2012;287(41):34801–8.
61. Middlebrooks CD, Bandy AR, Matsuda K, Udquim KI, Onabajo OO, Paquin A u.c. Dzimumlīnijas variantu saistība APOBEC3 reģionā ar vēža risku un bagātināšana ar APOBEC paraksta mutācijām audzējos. Nats Ženē. 2016;48(11):1330–8.
62. Nik-Zainal S, Wedge DC, Alexandrov LB, Petljak M, Butler AP, Bolli N u.c. APOBEC3A un APOBEC3B dzimumšūnu kopiju skaita polimorfisma saistība ar iespējamo APOBEC atkarīgo mutāciju slogu krūts vēža gadījumā. Nats Ženē. 2014;46(5):487–91.
63. Matsuda K, Takahashi A, Middlebrooks CD, Obara W, Nasu Y, Inoue K u.c. Genoma mēroga asociācijas pētījums identificēja SNP uz 15q24, kas saistīts ar urīnpūšļa vēža risku Japānas populācijā. Hum Mol Genet. 2015;24(4):1177–84.
64. Kim Y, Sun DS, Yoon J, Ko YH, Won HS, Kim JS. APOBEC3A un 3B ekspresijas klīniskā ietekme pacientiem ar krūts vēzi. PLoS ONE. 2020;15(3):e0230261. 65. Starrett GJ, Luengas EM, McCann JL, Ebrahimi D, Temiz NA, Love RP u.c. DNS citozīna deamināzes APOBEC3H I haplotips, iespējams, veicina krūts un plaušu vēža mutaģenēzi. Nat Commun. 2016;7(1):12918.
66. Stavrou S, Ross SR. APOBEC3 proteīni vīrusu imunitātē. J Immunol. 2015;195(10):4565–70.
67. Bosch FX, Lorincz A, Munoz N, Meijer CJLM, Shah K. Cēloņsakarība starp cilvēka papilomas vīrusu un dzemdes kakla vēzi. Dž Klins Patols. 2002;55(4):244–65.
68. Revathidevi S, Murugan AK, Nakaoka H, Inoue I, Munirajan AK. APOBEC: molekulārais virzītājspēks dzemdes kakla vēža patoģenēzē. Cancer Lett. 2021;496:104–16.
69. Riva G, Albano C, Gugliesi F, Pasquero S, Pacheco SFC, Pecorari G u.c. HPV satiekas ar APOBEC: jauni spēlētāji galvas un kakla vēža ārstēšanā. Int J Mol Sci. 2021;22(3):1402.
