Minerālorganisko nanodaļiņu noteikšana un raksturošana cilvēka nierēs
Feb 22, 2022
Tsui-Yin Wong1,2,*, Cheng-Yeu Wu1,2,3,* un citi
Ārpusdzemdes pārkaļķošanās ir saistīta ar dažādām cilvēku slimībām, tostarp aterosklerozi, vēzi,hroniskanieresslimība, uncukura diabētsmellitus. Lai gan pārkaļķotos asinsvados ir konstatētas minerālu nanodaļiņas, šo daļiņu būtība un loma cilvēka organismā joprojām nav skaidra. Šeit mēs pirmo reizi parādām, ka cilvēksnieresaudi, kas iegūti no beigu stadijashroniskanieresslimībavai nieru vēža pacienti satur apaļas, daudzslāņu minerālu daļiņas ar garumu 50 līdz 1500 nm, turpretim veselām kontrolēm daļiņas nav novērotas. Minerālu daļiņas atrodas galvenokārt ārpusšūnu matricā, kas ieskauj vītņotos kanāliņus, Henles savākšanas kanālus un cilpas, kā arī kanāliņus norobežojošo šūnu citoplazmā, un tās sastāv no polikristāliskā kalcija fosfāta, kas līdzīgs minerālam, kas atrodams kaulos un ārpusdzemdes pārkaļķojumos. Thenieresminerālu nanodaļiņas satur vairākus seruma proteīnus, kas kavē ārpusdzemdes kalcifikāciju ķermeņa šķidrumos, tostarp albumīnu, fetuīnu-A un apolipoproteīnu A1. Tā kā minerālu-organiskās nanodaļiņas ir atrodamas ne tikai pārkaļķotās nogulsnēs, bet arī vietās, kur nav mikroskopisku pārkaļķojumu, mūsu novērojumi liecina, ka nanodaļiņas var būt kalcifikācijas un nieru akmeņu priekšteči cilvēkiem.
Kontaktpersona:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791

Ārpusdzemdes pārkaļķošanās ir saistīta ar aterosklerozi, vēzi,hroniskanieresslimība, un cukura diabēts1–3. Jaunākie pētījumi liecina, ka aterosklerozes unhroniskanieresslimībapacientiem ar asinsvadu pārkaļķošanās pazīmēm ir paaugstināts saslimstības un mirstības risks, kas liecina, ka ārpusdzemdes pārkaļķošanās ir kaitīga cilvēka veselībai1,3. Nevēlama pārkaļķošanās tiek novērota arī novecojošiem indivīdiem, un lielākajai daļai cilvēku, kas vecāki par 60 gadiem, ir asinsvadu pārkaļķošanās pazīmes4. Šo iemeslu dēļ svarīgi mērķi ir ārpusdzemdes kalcifikāciju izraisošo faktoru atšifrēšana un efektīvas ārstēšanas izstrāde.
Ārpusdzemdes kalcifikāciju var definēt kā nelīdzsvarotību starp inhibitoriem un kalcifikācijas induktoriem organismā. Kalcifikācijas inhibitori ietver seruma olbaltumvielas, piemēram, albumīnu, fetuīnu-A, osteopontīnu un matricas GLA proteīnu, kā arī mazus savienojumus, piemēram, pirofosfātu, turpretim hiperfosfatēmija un iekaisums ir galvenie kalcifikācijas izraisītāji5–7. Jaunākie pētījumi liecina, ka pārkaļķošanās induktori aktivizē šūnu procesu, kas ir līdzīgs kaulu veidošanās procesam asinsvadu pārkaļķošanās laikā7,8. Matricas pūslīši, kas ir līdzīgi tiem, kas izraisa mineralizāciju jaunattīstības kaulos, ir konstatēti arī pārkaļķotos mīkstos audos7–9. Šīs matricas pūslīšus, iespējams, atbrīvo asinsvadu gludās muskulatūras šūnas, kas diferencējas osteoblastiem līdzīgās šūnās, kas izraisa kalcifikāciju7.
Mīkstajos audos ir konstatētas minerālu nanodaļiņas (NP), kurām ir ārpusdzemdes kalcifikācijas pazīmes. Price et al. atklāja, ka ar bisfosfonāta etidronātu vai D vitamīna vitamīnu ārstēto žurku serumā ir minerālvielu-olbaltumvielu kompleksi, kas satur kalcifikācijas inhibitorus fetuīnu-A un matricas GLA proteīnu10,11. Tāpat Jahnen-Dechent et al. novēroja, ka fetuīnu A saturošus minerālu kompleksus, ko sauca par kalciproteīna daļiņām (CPP), var noteikt ascītiskajā šķidrumā pacientiem ar kalcifikējošu peritonītu12. Nesenais pētījums, ko veica Bertazzo et al. parādīja minerālu NP klātbūtni gan aterosklerozes, gan reimatiskā drudža pacientu aortas vārstuļos un koronārajās artērijās13. Lai gan pētījumi par minerālu daļiņu veidošanos parasti ir vērsti uz cilvēka sirds un asinsvadu sistēmu, joprojām nav skaidrs, vai daļiņas var atrasties citos audos un vai šīm vienībām ir nozīme veselībā vai slimībās.
Iepriekš mēs novērojām, ka minerāli-organiskie NPS spontāni veidojas cilvēku un dzīvnieku ķermeņa šķidrumos 14–28. Šie minerālu NP sākotnēji tika aprakstīti kā nanobaktērijas (NB), un tika uzskatīts, ka tās ir ne tikai mazākās šūnas uz zemes29, bet arī iespējamais daudzu slimību, tostarp Alcheimera slimības, aterosklerozes, vēža, pārnēsāšanas cēlonis.nieresakmensveidošanās, policistiskanieresslimība, un prostatīts30–32. Tomēr mūsu rezultāti ir parādījuši, ka NB patiesībā ir nedzīvi minerālu NP, kas atdarina parastās baktērijas to morfoloģijas, augšanas, proliferācijas un subkultūras ziņā15, 18, 22. Vēl jāizpēta iespēja, ka cilvēka audos var atrasties tā sauktajām NB līdzīgām minerālu daļiņām un vai šīm daļiņām ir nozīme slimībās.
Šajā pētījumā mēs izstrādājām nanomateriālu pieeju, lai atklātu un analizētu minerālu-organisko NP slimā cilvēkā.nieresaudus. Mēs parādām, ka nieru audi no beigu stadijas hroniskas nieru slimības un nieru vēža slimniekiem satur daudzslāņu minerālu NP, kas ir līdzīgi biomimētiskajām minerālu daļiņām, kas spontāni izgulsnējas ķermeņa šķidrumos in vitro . Mūsu rezultāti atklāj kritisku ieskatu par šo minerālu-organisko daļiņu bioķīmisko sastāvu, veidošanās mehānismu un bioloģisko funkciju, un tie atklāj ārpusdzemdes pārkaļķošanās mehānismus un slimības ierosināšanu cilvēka organismā.
Rezultāti
Mēs pārbaudījām nieru audus, kas ķirurģiski izņemti pacientiem ar hronisku nieru slimību beigu stadijā (n=2) vai nieru vēzi (n=18; skatīt 1. tabulu; nieru vēža paraugiem mēs koncentrējāmies uz ne - audu vēža daļa). Kā veselas kontroles mēs pētījām nieru biopsijas, kas iegūtas no pacientiem ar traumu vai hematomu, bet kuriem iepriekš nebija patoloģisku nieru darbību (n=2; 1. tabula).
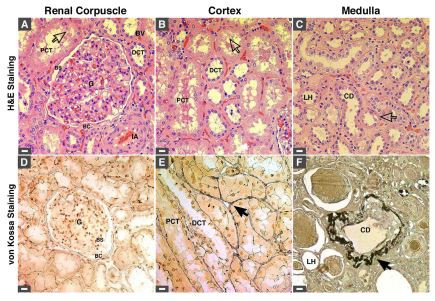
Veselu indivīdu nieru audiem bija normālas histoloģiskas pazīmes, un pēc fon Kossa krāsošanas netika novērota ārpusdzemdes pārkaļķošanās (1.A, B att.). No otras puses, nieru audos, kas iegūti no slimiem indivīdiem un krāsoti ar hematoksilīnu un eozīnu (H&E), tika konstatēti audu bojājumi (2.A–C. attēls, kas norādīts ar bultiņām), un 80 procentos pārbaudīto slimo audu bija mineralizēti nogulsnes, kā atklāts. ar fon Kossa krāsošanu (1. C. – T. att., 2. E., F. att., pārkaļķošanās ir redzama kā melns materiāls, kas apzīmēts ar melnām bultiņām; skatīt arī 1. tabulu). Pārkaļķojušies nogulsnes tika pamanītas garozā un smadzenēs, tostarp ārpusšūnu telpā, kas ieskauj distālos vītņotos kanāliņus, proksimālās vītņotās kanāliņos, Henles savākšanas vadus un cilpas, kā arī šūnu citoplazmu, kas iezīmē kanāliņus un kanālus (1. C–T att. 2E, F). Nieres asinsķermenī pārkaļķošanās netika konstatēta (2.D att.).

Lai pārbaudītu minerālu nogulsnes, mēs sagatavojām īpaši plānas nieru sekcijas novērošanai ar transmisijas elektronu mikroskopiju (TEM). Paraugos, kas satur mikroskopiskas minerālu nogulsnes, minerālu daļiņas vai granulas tika konstatētas nieru epitēlija šūnu citoplazmā, ekstracelulārajā matricā zem bazālās membrānas un proksimālo un distālo vītņotu kanāliņu lūmenā (3.A, B att., daļiņas ir palielinātas). paneļos A1–A4 un B1–B4). Minerālu NP tika novēroti arī šūnās, kas klāj Henles cilpas un savākšanas kanālus (3. C, D att., palielināts paneļos C1, C2 un D1). Dažas daļiņas tika atrastas nieru šūnu intracelulārajos pūslīšos (3.A attēls, A1 un A2 paneļi). Šeit izmantotā elektronu mikroskopijas pieeja ļāva arī vizualizēt minerālu daļiņu iekšpusi; dažās daļiņās bija elektronu blīvi gredzeni, kas mijas ar viegliem, elektronu caurlaidīgiem slāņiem (3.A att., A3 un A4 paneļi, 3.C att., panelis C1). Vairākus asinsvadus, piemēram, vasa recta rentes (nieres taisnās artērijas), mūs ieskauj liels skaits minerālu NP (3. D attēls, panelis D1). Tādējādi minerālu NP tika atrasti dažādās vietās visos cilvēka nieru audos, kam bija ārpusdzemdes pārkaļķošanās pazīmes, turpretim veselajās kontrolēs netika atrastas daļiņas.
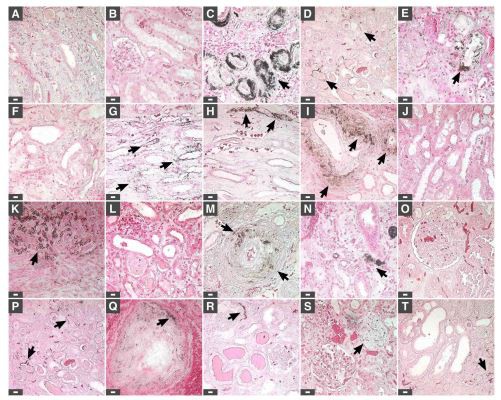
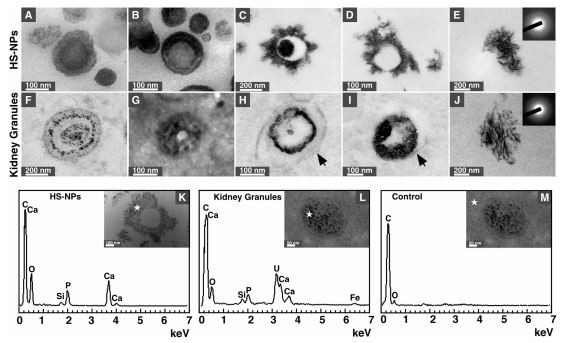
Nieru audos atrastās minerālu daļiņas, šķiet, ir ļoti līdzīgas minerālorganiskajiem NP, kas aprakstīti mūsu iepriekšējos pētījumos spontāni veidojoties ķermeņa šķidrumos 15, 17 (un kurus mēs esam nosaukuši par bioniem 24). Lai pārbaudītu šo iespēju, mēs sagatavojām minerālu organiskos NP (vai bionus), izmantojot nokrišņu metodi, kā mēs iepriekš aprakstījām . Šī metode sastāv no izgulsnēšanas jonu, piemēram, kalcija un fosfāta, pievienošanas šūnu kultivēšanas barotnei (Dulbecco modificētajai ērgļa barotnei vai DMEM), kas satur ķermeņa šķidrumu, piemēram, cilvēka serumu (HS), kam seko inkubācija šūnu kultūras apstākļos (skatīt metodes). Šādā veidā iegūtās daļiņas (HS-NPS) bija vai nu sfēriskas, vai elipsoidālas, un tām bija gluda vai kristāliska minerālu virsma (4A–E att.), kas ir līdzīga iepriekš aprakstītajām daļiņām ķermeņa šķidrumos22,23, kā arī cilvēka ascītā12 un pārkaļķojušās artērijas13. Minerālu daļiņas bija ļoti līdzīgas minerālu NP vai granulām, kas novērotas nieru audos pēc to vispārējās morfoloģijas, daudzslāņu struktūras un virsmas īpašībām (4. att. F-J). Arī HS iegūto daļiņu un nieru granulu izmērs bija salīdzināms, diametrā no 50 līdz 1500 nm (4.A-E, F-J att.). Kā minēts iepriekš, dažas nieru granulas ieskauj lipīdu membrāna, kas, iespējams, attēlo intracelulāras kravas vezikulas vai ārpusšūnu membrānas pūslīšus (4H, I att., membrānas ir apzīmētas ar bultiņām); šādas membrānas struktūras nebija HS-NP paraugos, kas sagatavoti in vitro (4. A-E att.). Šie novērojumi liecina, ka nieru granulas ir līdzīgas mineralo-organiskajiem NP, kas samontēti serumā.
Izmantojot atlasīto laukuma elektronu difrakcijas analīzi, mēs novērojām, ka in vitro sagatavoto HS-NP minerālā fāze sastāvēja no polikristāliska nanomateriāla (4. E att., ielikts; ievērojiet vājos koncentriskos gredzenus). Līdzīgi rezultāti tika iegūti nieru granulām (4.J att., ielaidums) un kauliem un ārpusdzemdes pārkaļķojumiem, kā aprakstīts iepriekšējos pētījumos33,35.
Mēs pētījām HS-NP un nieru granulu ķīmisko sastāvu, izmantojot enerģiju izkliedējošu rentgena spektroskopiju (EDX). HS-NP uzrādīja galvenos oglekļa (C), kalcija (Ca), skābekļa (O) un fosfora (P) pīķus (4K att.), kas atbilst kalcija fosfāta minerāla klātbūtnei. Zems silīcija (Si) maksimums tika novērots arī HS-NP (4K att.), kas, iespējams, pārstāv nelielu daļiņu sastāvdaļu. Nieru granulās bija arī oglekļa, kalcija, skābekļa un fosfora maksimumi, kas liecina par kalcija fosfāta minerālu, kā arī papildu silīcija un dzelzs (Fe) pīķi (4. att.). Urāna pīķi (U) tika attiecināti uz uranilacetātu, ko parauga sagatavošanas laikā izmantoja kā kontrastējošu reaģentu (urāna klātbūtne dažos minerālu daļiņu paraugos, piemēram, nieru granulās, un tā trūkums kontroles audos 4M attēlā var būt saistīts ar augstu urāna afinitāte pret fosfātu, kā ziņots iepriekš35). Nieru audu kontroles EDX spektros, kas ieskauj daļiņas, bija oglekļa un skābekļa maksimumi (4M attēls), kas liecina, ka kalcijs un fosfors tika atrasti galvenokārt minerālu daļiņās.
Kalcija: fosfora (Ca:P) attiecība HS-NP un nieru granulās mainījās no 0,65 līdz 1,18. Šīs attiecības atšķiras no teorētiskās vērtības 1, 67, kas novērotas stehiometriskajam hidroksiapatītam, bet joprojām ir robežās, kas iepriekš tika novērotas kalcija fosfāta un apatīta kristāliem, kas novēroti dažādās kristalizācijas pakāpēs15. Kopā šie atklājumi apstiprina, ka nieru granulas sastāv no kalcija fosfāta NP.
Ir konstatēts, ka dažādi proteīni organismā sistēmiski kavē ārpusdzemdes kalcifikāciju36,37. Turklāt tiek uzskatīts, ka proteīna korona, kas atrodas uz sintētisko NP virsmas, nosaka daļiņu bioloģisko sadalījumu un ietekmi uz šūnām in vivo 38, 39. No otras puses, cilvēka nieru audos atrodamo mineraloorganisko NP olbaltumvielu sastāvs joprojām ir nepilnīgi saprotams. Iepriekš mēs noskaidrojām, ka albumīns, fetuīns-A un apolipoproteīns-A1 (apo-A1) ir galvenie proteīni, kas mijiedarbojas ar ķermeņa šķidrumos veidotajiem mineralo-organiskajiem NP 17, 20. Šeit mēs izmantojām imūnzelta marķējumu, lai pārbaudītu šo proteīnu klātbūtni un ultrastrukturālo atrašanās vietu nieru granulās.
Mēs izmantojām poliklonālās antivielas pret cilvēka seruma albumīnu (HSA), cilvēka seruma fetuīnu-A (HSF), cilvēka apo-1A un visu HS, lai pārbaudītu seruma proteīnu klātbūtni HS-NP un nieru granulās. Poliklonālo antivielu (sagatavotas, kā aprakstīts iepriekš25) specifika tika pārbaudīta, izmantojot Western blotēšanu (5. att.). Katra no poliklonālajām antivielām pozitīvi reaģēja ar in vitro sagatavotajiem HS-NP, kā arī ar cilvēka nieru audos atrastajām minerālu granulām (6.A, B att., paneļi A1–A3 un B1–B3; melni punkti). Antivielas reaģēja galvenokārt ar elektronu blīvajiem slāņiem vai HS-NP un nieru granulu tumšo kodolu (6.A, B att.), norādot, ka šajos tumšajos apgabalos var būt augstāks olbaltumvielu līmenis, salīdzinot ar elektronu caurlaidības zonām. Negatīvās kontroles, kas veiktas bez primārās antivielas, neizraisīja reakciju (6.A, B att., A4 un B4 paneļi, kontrole). Mēs secinājām, ka nieru granulas pārstāv mineralo-organiskos NP, kas ir līdzīgi HS-NP, pamatojoties ne tikai uz to morfoloģiju un minerālu sastāvu, bet arī uz to saistīšanos ar galvenajiem kalcifikācijas inhibitoriem, kas atrodas serumā.
Tālāk tika izmantota imunofluorescences mikroskopija, lai apstiprinātu HSA un HSF saturošu minerālu granulu klātbūtni slimās cilvēka nierēs. Izmantojot šo paņēmienu, cilvēka nieru audi parādīja
pozitīvs krāsojums abām olbaltumvielām dažādās jomās, tostarp intersticiumā, kas ieskauj nieru kanāliņus, kā arī kanāliņu iezīmējošo šūnu citoplazmā (7.A att., A1 un A2 paneļi). Šajos apgabalos tika pamanīti arī proteīnu agregāti, kas satur gan albumīnu, gan fetuīnu-A, lai gan mazākos daudzumos, salīdzinot ar atsevišķu proteīnu krāsojumu (7.A attēls un panelis A3, apvienota krāsošana dzeltenā krāsā). Konkrēti, mēs pamanījām, ka ar imunofluorescenci konstatētā proteīna krāsošanās cieši pārklājās ar ārpusdzemdes pārkaļķošanās modeli, kas novērots, izmantojot fon Kossa krāsošanu (7.A, B att., kalcifikācija ir redzama kā melns materiāls, kas norādīts ar bultiņām B). Šie rezultāti sniedz papildu atbalstu mineralo-organisko daļiņu klātbūtnei pārbaudītajos cilvēka nieru audos.

Diskusija
Lai gan ir panākts progress mūsu izpratnē par sintētisko NP un cilvēka šūnu mijiedarbību, mēs zinām daudz mazāk par minerālorganisko NP, kas spontāni veidojas ķermeņa šķidrumos, ietekmi. Mūsu iepriekšējie pētījumi ir parādījuši, ka šīs daļiņas veidojas bioloģiskajos šķidrumos, kad kalcija un fosfāta koncentrācija pārsniedz piesātinājumu15,16. Mēs arī novērojām, ka šīs daļiņas internalizē imūnās šūnas, bet tikai lielas daļiņas izraisa iekaisuma imūnreakcijas23. Tomēr šo daļiņu izplatība cilvēka audos un tas, vai tām ir kāda fizioloģiska vai patoloģiska loma organismā, līdz šim nav pētīta.
Šajā pētījumā mēs pirmo reizi atklājām minerālorganiskos NP cilvēku pacientu nierēs, kuri cieš no beigu stadijas nieru slimības vai nieru vēža. Konstatētie mineraloorganiskie NP satur vāji kristalizētu kalcija fosfātu, kas līdzīgs kaulu minerālam, kā arī albumīnu, fetuīnu-A un apo-A1, kas darbojas kā sistēmiski kalcifikācijas inhibitori ķermeņa šķidrumos. Mūsu rezultāti saskan ar iepriekšējiem ziņojumiem, kuros aprakstīta minerālu-olbaltumvielu kompleksu klātbūtne asinsvadu audos un ķermeņa šķidrumos 12, 13, 34, 40. Tā kā daļiņas, kuras mēs novērojām, tika atrastas vietās, kur nav mikroskopisku pārkaļķošanos, mūsu novērojumi liecina, ka daļiņas var būt ārpusdzemdes pārkaļķošanās priekšteči cilvēka audos. Ņemot vērā iespēju, ka minerālorganiskie NP var pakāpeniski palielināties un labvēlīgos apstākļos pāriet no daļiņām uz plēvi, kā aprakstīts mūsu iepriekšējos pētījumos 15, 18, šeit sniegtie novērojumi liecina, ka minerālu prekursori var izraisīt lielāku veidošanos. minerālu nogulsnes in vivo, piemēram, Rendāla plāksne un nierakmeņi.

Mūsu novērojumi, ka minerālu ārpusdzemdes pārkaļķošanās un mineralo-organiskie NP ir atrodami dažādās nieru anatomiskajās struktūrās, atbilst iepriekšējiem ārpusdzemdes pārkaļķošanās atklājumiem šajā orgānā41. Evan et al. novērojumi norādīja, ka mineralizācija nierēs pacientiem ar nefrolitiāzi var sākties un notikt galvenokārt Henles cilpu intersticiālajos audos40,42. Šie autori novēroja, ka minerālu nogulsnes, kas veidojas šajā apgabalā, var izvirzīties no urotēlija bazālās puses un izraisīt nierakmeņu veidošanos. Mūsu novērojumi liecina, ka papildus Henles cilpām citās nieru zonās var būt minerālu NP, kas galu galā var attīstīties, veidojot lielas minerālu nogulsnes cilvēka nierēs. Mēs arī pētām iespēju, ka minerālu NP, kas veidojas asinsritē, var pārvietoties nieru audos un izraisīt ārpusdzemdes kalcifikāciju un akmeņu veidošanos nierēs.
Vairākas šajā pētījumā atklātās nieru granulas ir atrodamas intracelulārajās vai ekstracelulārajās pūslīšos (4H, I att.), un tās ir līdzīgas matricas pūslīšiem, kas, kā pierādīts, izraisa kalcifikāciju kaulos un zobos7,8. Nesen mēs novērojām, ka pūslīši, kas izolēti no cilvēka un dzīvnieku seruma, in vitro inducē minerālu NP un mikroskopisku nogulšņu veidošanos25. Schlieper et al.34 arī novēroja, ka artērijās atrodamās minerālu daļiņas ir saistītas ar membrānu struktūrām, un ierosināja, ka matricas pūslīši vai apoptotiskie ķermeņi var būt minerālu daļiņu kodoli šajos audos. Līdzīgi, Khan et al. ziņoja, ka kalcija fosfāta nogulsnes, kas konstatētas cilvēku ar idiopātiskiem nierakmeņiem, nierēs ir saistītas ar kolagēna šķiedrām un matricas pūslīšiem9. Šie rezultāti liecina, ka nieru audos konstatētie mineralo-organiskie NP var veidoties, izmantojot mehānismu, kas ietver membrānas pūslīšus, kas ir analoga situācijai, kas redzama aterosklerozes artērijās 7, 8. No otras puses, nesen veikts pētījums parādīja, ka ārpusdzemdes pārkaļķošanās, kas konstatēta sieviešu krūšu artērijās, nebija saistīta ar osteogēniem vai apoptotiskiem šūnu marķieriem43, kas liecina, ka kalcifikācijas mehānisms var būt specifisks iesaistītajam orgānam vai bioloģiskajam kontekstam. Turklāt minerālorganiskie NP, piemēram, šeit aprakstītie, cilvēka nieru audi var veidoties arī tāpēc, ka netiek uzturēta jonu (piemēram, kalcija un fosfāta) un kalcifikācijas inhibitoru (piemēram, albumīna, fetuīna-A un apo) fizioloģiskā koncentrācija. -A1) cilvēka ķermeņa šķidrumos.
Mūsu rezultāti liecina, ka minerālu-organisko NP elektronu blīvais slānis un kodols var saturēt augstāku olbaltumvielu un organisko molekulu līmeni, salīdzinot ar daļiņu elektronu caurlaidības zonām (6.A, B att.). Šķiet, ka šie elektronu blīvie slāņi ir mineralizēti, kā redzams šī materiāla kristāliskajā dabā saskaņā ar TEM (sk. 4. A-J att.). Citi autori, tostarp Ryall41 un Evan et al.44, ir ierosinājuši, ka elektronu caurlaidīgais slānis var attēlot minerālus, bet elektronu blīvie slāņi var atbilst organiskajām molekulām. Šīs interpretācijas vismaz daļēji var būt saistītas ar veidu, kādā paraugi tika apstrādāti un pārbaudīti katrā pētījumā, kā arī izmantoto sākuma audu raksturs.
Papildus tam, ka minerālvielas-organiskās daļiņas ir iesaistītas ārpusdzemdes kalcifikācijā, tās var izraisīt iekaisumu nieru audos. Mēs nesen parādījām, ka, lai gan mineraloorganiskie NP nespēj izraisīt cilvēka makrofāgu pro-iekaisuma interleikīna -1 sekrēciju, minerālu agregāti, kas lielāki par 1 μm, to spēj izdarīt23. Ir pierādīts, ka interleikīna -1 izdalīšanās, reaģējot uz kristāliskiem materiāliem, ir atkarīga no intracelulāro molekulāro kompleksu aktivizēšanas, ko sauc par iekaisumiem45–47. Turklāt minerālu daļiņas tika atklātas nierēs, kurās bija audzēji, un tagad ir labi zināma saistība starp vēzi un iekaisumu48. Joprojām ir jāizpēta iespēja, ka agregētas minerālu daļiņas var aktivizēt iekaisumu un veicināt iekaisuma un vēža attīstību nierēs vai citos audos.
Papildus ārpusdzemdes pārkaļķošanai šeit aprakstītās minerālu granulas var piedalīties citos slimības procesos. Piemēram, mēs jau iepriekš esam ierosinājuši, ka minerālvielu NP var saistīties ar dažādiem ķermeņa šķidrumos esošajiem proteīniem un noārdīt šīs organiskās molekulas no ķermeņa šķidrumiem 20, 26. No otras puses, cilvēka ķermenis normālos apstākļos var novērst minerālvielu NP veidošanos un uzkrāšanos, paļaujoties uz kalcifikācijas inhibitoru un retikuloendoteliālās sistēmas (ti, makrofāgu) klātbūtni. Tādējādi minerālvielu NP var uzkrāties tikai tad, kad tiek traucēta sistēmiskā vai lokālā kalcija homeostāze un ja cilvēka organismā ir bojāti aizsardzības mehānismi.
Mēs ierosinām, ka šeit izstrādāto nanomateriālu pieeju var izmantot, lai pētītu mineralo-organisko NP veidošanos dzīvnieku un cilvēku audos. Piemēram, antivielas, kas radītas pret kalcifikācijas inhibitoru proteīniem, piemēram, albumīnu, fetuīnu-A un apo-A1, var izmantot kombinācijā ar minerālu analīzi, lai noteiktu un raksturotu mineraloorganisko NP veidošanos dzīvnieku modeļu audos. Rezultātus, kas iegūti, izmantojot šo pieeju, var izmantot klīniskiem mērījumiem, kas veikti cilvēka ķermeņa šķidrumos, lai identificētu bioloģiskos parametrus, kas atspoguļo minerālu daļiņu veidošanās stāvokli un ārpusdzemdes pārkaļķošanos organismā. Mēs sagaidām, ka šīs zināšanas var novest pie jaunu terapeitisku stratēģiju izstrādes, lai novērstu un ārstētu cilvēku slimības un apstākļus, kas saistīti ar ārpusdzemdes kalcifikāciju.
Metodes
Nieru audi.Cilvēka audu izmantošanu un šajā pētījumā veiktos eksperimentus apstiprināja Chang Gung Memorial Hospital Institucionālā pārskata padome; metodes un eksperimenti tika veikti saskaņā ar apstiprinātajām vadlīnijām. No pacientiem tika saņemta rakstiska informēta piekrišana. Kontroles veseli nieru audi tika iegūti no traumu un hematomas pacientu biopsijām, kuriem anamnēzē nebija nieru slimības (n=2); nieru audi tika iegūti arī no nieru vēža pacientiem (n=20) un no nieru slimības beigu stadijas pacientiem (n=2), kuriem transplantācijas operācijas laikā tika izņemtas nieres vai veikta biopsija (1. tabula). Nieru vēža audiem šajā pētījumā tika izdalīta un analizēta audu daļa, kas nav vēzis.

Histoloģiskā analīze.Nieru audi tika uzstādīti uz parafīna blokiem. Bloki tika sadalīti un audu šķēles tika karsētas uz karstās plāksnes 70 grādu temperatūrā 30 minūtes, lai noņemtu parafīnu. Sekcijas tika iegremdētas svaigā ksilola šķīdumā trīs reizes 15 minūtes, lai pilnībā noņemtu atlikušo parafīnu. Sekcijas tika rehidrētas ar 95 procentiem, 80 procentiem un 70 procentiem etanola katru reizi 5 minūtes. Rehidrētos paraugus 5 minūtes mazgāja ar divreiz destilētu ūdeni (ddH2O). Šūnu kodoli tika iekrāsoti ar hematoksilīnu 8 minūtes. Krāsvielu no paraugiem noņēma ar siltu ūdeni 10 minūtes. Nieru paraugi tika izskaloti ddH2O un 10 reizes iemērkti 95 procentu etanolā. Ar etanolu apstrādātos paraugus 1 minūti iekrāsoja ar eozīnu Y. Paraugi tika dehidrēti ar 95% un 100% etanolu katru reizi 10 minūtes, kam sekoja dehidratācijas posms ksilolā 10 minūtes. Galīgie dehidrētie nieru paraugi tika uzstādīti uz stikla priekšmetstikliņiem ar 50% glicerīna un novēroti gaismas mikroskopā, kas aprīkots ar digitālo kameru.

Deparafinēti un rehidrēti paraugi tika sagatavoti, kā aprakstīts H&E krāsošanai. Rehidrētās sekcijas tika iekrāsotas ar sudraba nitrātu (5 procenti), kam sekoja UV gaismas iedarbība 20 minūtes. Šķīdumu 15 minūtes mazgāja ar ddH2O. Sekcijas tika iekrāsotas ar nātrija tiosulfātu (5 procenti) 5 minūtes, kam sekoja mazgāšana ar ddH2O 15 minūtes. Sekcijas tika iekrāsotas ar kodolātri sarkanu (Sigma-Aldrich, Sentluisa, MI) 5 minūtes. Krāsotie paraugi tika dehidrēti secīgi ar 95% un 100% etanolu 10 minūtes, pirms dehidratācijas ksilolā 10 minūtes. Nieru paraugi tika uzstādīti uz stikla priekšmetstikliņiem un pārbaudīti, kā aprakstīts iepriekš.
Elektronu mikroskopija un EDX analīze.Nieru paraugi tika sagriezti mazos gabaliņos, kas bija mazāki par 1 mm, izmantojot LGPS sadalīšanas mikroskopu (Olympus, Tokija, Japāna). Audi tika fiksēti ar 2,5% glutaraldehīda un 1% paraformaldehīda 0,1 M kakodilāta buferšķīdumā 4 grādu temperatūrā nakti. Fiksētie paraugi tika mazgāti trīs reizes ar 0,1 M kakodilāta buferšķīdumu 8 procentiem saharozes (pH 7,2) uz ledus 10 minūtes. Mazgātos audus 2 stundas uz ledus inkubēja ar fosfātu buferētā fizioloģiskā šķīdumā (PBS; 137 mM NaCl, 2,7 mM KCl, 10 mM Na2HPO4), kas satur 1 procentu osmija tetroksīda un 1,5 procentus kālija ferocianīda. Audus trīs reizes mazgāja ar ddH2O uz ledus 10 minūtes. Mazgātos audus 1 stundu krāsoja uz ledus ar 1% uranilacetātu ddH2O, pēc tam trīs reizes mazgājot ar ddH2O uz ledus. Nieru audi tika dehidrēti ar 30, 50, 70, 80 un 90 procentiem etanola katru reizi 10 minūtes, izņemot gadījumus, kad etanols sasniedza 70 procentus, un tādā gadījumā paraugus uz nakti uzglabāja 4 grādu temperatūrā. Audus 15 minūtes iekrāsoja ar 1% fosfotungstīnskābi 95% etanolā, pēc tam 5 minūtes dehidratēja ar 95% etanolu. Paraugi tika iegremdēti propilēna oksīdā 40, 57, 67 un 100 procentu temperatūrā etanolā katru reizi 10 minūtes, kam sekoja vēl viena iegremdēšana 100 procentu propilēna oksīdā 5 minūtes. Nieru audi tika infiltrēti ar 50, 70 un 100 procentiem Eponate 812 (Ted Pella, Redding, CA) katru reizi 1 stundu. Eponāta 812-iegultie nieru paraugi tika sagatavoti, divreiz inkubējot 100 procentu eponātā. Iegultos paraugus nakti inkubēja krāsnī 60 grādos, lai nodrošinātu sveķu polimerizāciju.
Mazgātas HS-NP granulas, kas iegūtas, kā norādīts iepriekš, tika fiksētas ar glutaraldehīdu (2,5 procenti) un paraformaldehīdu (1 procents) ddH2O 4 stundas 4 grādu temperatūrā. Fiksētās granulas tika mazgātas ar ddH2O trīs reizes 10 minūtes katru reizi. Granulas tika dehidrētas ar secīgām inkubācijām 30, 50, 70, 80, 90, 95 un 100 procentu etanolā katru reizi 10 minūtes, izņemot gadījumus, kad etanols sasniedza 70 procentus, kurā granulas tika uzglabātas 4 grādu temperatūrā nakti. Citi etanola šķīdumi tika saskarē ar granulām tikai 10 minūtes. Dehidrētas granulas tika infiltrētas ar LR balto iegulšanas vidi (Electron Microscopy Sciences, Hatfield, PA), izmantojot dažādas etanola un LR barotnes attiecības (3: 1, 1: 1 un 1: 3) katra 30 minūtes. Granulas tika infiltrētas ar svaigu LR barotni (100 procenti) nakti pirms polimerizācijas. Granulas, kas infiltrētas ar LR barotni, tika inkubētas krāsnī 60 grādu temperatūrā 2 dienas, lai nodrošinātu sveķu polimerizāciju. Nieru un HS-NP bloki tika sadalīti, lai iegūtu šķēles ar biezumu 70–100 nm, izmantojot Reichert Ultracut S mikrotomu (Leica, Wetzlar, Vācija). Audu sekcijas tika iekrāsotas ar 4% uranilacetātu pirms vizualizācijas JEM 1230 transmisijas elektronu mikroskopā (JEOL, Tokija, Japāna), kas darbojās ar 100 kV. Elektronu difrakcijas modeļi tika iegūti, izmantojot to pašu sistēmu. Niķeļa režģi tika izmantoti kā atbalsts.
EDX analīzei plānās nieru audu daļas tika iekrāsotas ar uranilacetātu un mazgātas ar ddH2O, kā norādīts iepriekš, kam sekoja žāvēšana elektroniskā eksikatora skapī. Paraugi tika novēroti augstas izšķirtspējas JEM 2100 transmisijas elektronu mikroskopā (JEOL), kas darbojās ar 120 kV spriegumu. EDX spektri tika iegūti trīs eksemplāros, izmantojot INCA Energy EDS sistēmu (Oxford Instruments, Abingdon, UK). Plānas HS-NP daļas tika novērotas bez krāsošanas.
Minerālorganisko NP sagatavošana.Visi sākuma šķīdumi tika noregulēti līdz pH 7,4 un pirms lietošanas sterilizēti, filtrējot caur 0,2 μm membrānām. HS tika iegūts no veseliem brīvprātīgajiem, izmantojot parasto venipunktūras tehniku. Cilvēka bioloģisko šķidrumu izmantošanu šajā pētījumā apstiprināja Linko Chang Gung memoriālās slimnīcas Institucionālā pārskata padome, un no brīvprātīgajiem tika saņemta rakstiska informēta piekrišana. HS-NP tika sagatavoti, pievienojot katru 3 mM CaCl2 un Na2HPO4 DMEM (Gibco, Carlsbad, CA), kas satur 10 procentus HS, kam sekoja inkubācija vienu nedēļu šūnu kultūras apstākļos (37 grādi, 5 procenti CO2, mitrināts gaiss). Daļiņas tika granulētas, centrifugējot pie 16, 000 × g 15 minūtes 4 grādos un divas reizes nomazgātas ar HEPES buferšķīdumu (20 mM HEPES, 1 mM CaCl2, 2 mM Na2HPO4, 150 mM NaCl), izmantojot to pašu centrifugēšanas procedūru.
SDS-PAGE un Western blotēšana.SDS-PAGE un Western blot analīze tika veikta būtībā tāpat kā iepriekš15. Īsumā, 0.2 ug (5.A,D. att.) vai 1,2 ug (5.B ,C. att.) HS olbaltumvielas, 47 ug (5.A, B,D att.) vai 590ug HS-NP proteīnu (5. C att.), 0,1 ug HSA (5.A–D. att.) un 0,6 ug (5.A, C, D att.) vai {{23} },15 ug HSF (5.B att.) tika izšķīdināti 5 reizes "iekraušanas buferšķīdumā" (0,313 M Tris-HCl pH 6,8, 10 procenti SDS, 0,05 procenti bromfenolzilā, 50 procenti glicerīna, 12,5 procenti - merkaptoetanols) līdz galīgajai koncentrācijai 1x, pirms karsēšanas 95 grādos 5 minūtes un atdalīšanas denaturēšanas un reducēšanas apstākļos ar 10% SDS-PAGE, izmantojot mini-gēla sistēmu (Hoefer, Holliston, MA). NP kontrole (izmantota 5.A–D att. 1. joslā) sastāvēja no minerālu NP, kas sagatavoti, pievienojot DMEM 3 mM CaCl2 un Na2HPO4 (galīgais tilpums 1 ml), kam sekoja inkubācija vienu dienu šūnu kultūras apstākļos; daļiņas tika granulētas, centrifugējot pie 16,000 × g 15 minūtes, divas reizes nomazgātas ar HEPES buferšķīdumu un atkārtoti suspendētas 50 ul HEPES buferšķīduma. 20 ul atkārtoti suspendētu daļiņu alikvota daļa tika apstrādāta SDS-PAGE, kā norādīts iepriekš. PVDF membrānas tika bloķētas 1 stundu 5% (w/v) attaukotā pienā istabas temperatūrā. Primārās antivielas, kas ražotas uzņēmumā, kā aprakstīts iepriekš25, tika izmantotas atšķaidījumā 1:1, 000 (-apo-A1 un -HS-NP), 1:3, 000 (-HSF) , vai 1:6,000 (-HSA). Ar kazu anti-trušu mārrutku peroksidāzi konjugētā sekundārā antiviela tika izmantota, pamatojoties uz ražotāja sniegtajiem norādījumiem (Millipore, Billerica, MA). Bloti tika atklāti, izmantojot pastiprinātu ķīmijluminiscenci (Amersham Biosciences, Amersham, Apvienotā Karaliste) un autoradiogrāfiskās plēves.
Imūnzelta marķēšana.Paraugi tika sagatavoti TEM novērošanai. HS-NP bloki tika sadalīti šķēlēs, kuru biezums bija mazāks par 70 nm. Paraugu sekcijas uz režģiem tika bloķētas ar 1 procentu zivju želatīnu (Sigma) 0,1 M HEPES buferšķīdumā (pH 8,0) 25 minūtes. Režģi tika inkubēti ar šādām primārajām antivielām: -HSA, 1:30; -HSF, 1:50; -apo-A1, 1:30; -HS-NP, 1:60. Negatīvā kontrole nesaturēja primāro antivielu (1 procents zivju želatīna HEPES buferšķīdumā). Inkubētās sekcijas 15 minūtes skaloja ar HEPES buferšķīdumu. Izskalotās sekcijas tika bloķētas ar 1 procentu zivju želatīnu HEPES buferšķīdumā 20 minūtes. Paraugi tika apstrādāti ar sekundāro 5-nm-zelta konjugātu kazas anti-trušu IgG 1 stundu. Paraugus 10 minūtes mazgāja ar HEPES buferšķīdumu, pirms 10 minūtes mazgāja ar ddH2O. TEM novērojumi tika veikti, kā minēts iepriekš.
Fluorescences mikroskopija.Histoloģiskie nieru audu priekšmetstikliņi, kas sagatavoti, kā norādīts iepriekš, tika bloķēti ar 1 procentu liellopu seruma albumīna 1 stundu istabas temperatūrā. Priekšmetstikliņus inkubēja ar primārajām poliklonālajām antivielām atšķaidījumā 1:4, 000. Pēc mazgāšanas paraugi tika inkubēti ar sekundārajām antivielām kazas anti-trušu FITC (492/520nm) un kazas anti-trušu-TRITC (550/570nm) (Jackson Immuno Research, West Grove, PA) 1:100. 1h. Kompleksi tika mazgāti ar PBST 15 minūtes. Fluorescējošais traips 4′,6-diamidino-2-fenilindols (DAPI) tika izmantots ar 10 ug/ml 15 minūtes. Ar DAPI iekrāsotos paraugus dehidrēja ar 95 un 100% etanolu 10 minūtes, kam sekoja dehidratācija ksilolā vēl 10 minūtes. Dehidrēti nieru paraugi tika uzstādīti ar Vectashield fluorescences H-1000 montāžas barotni (Vector Laboratories, Burlingame, CA) un tika novēroti konfokālā mikroskopā (LSM510 Meta; Zeiss, Oberkochen, Vācija), kas aprīkots ar Spot Flex kameru.

Cistanche tubulosa novērš nieru slimību, noklikšķiniet šeit, lai iegūtu paraugu
Atsauces
1. Giachelli, CM Ārpusdzemdes kalcifikācija: stingru faktu apkopošana par mīksto audu mineralizāciju. Am J Pathol 154, 671–675 (1999).
2. Abedin, M., Tintut, Y. & Demer, LL Asinsvadu kalcifikācija: mehānismi un klīniskās sekas. Arterioscler Thromb Vasc Biol 24, 1161–1170 (2004).
3. Alexopoulos, N. & Raggi, P. Calcification in aterosclerosis. Nat Rev Cardiol 6, 681–688 (2009).
4. Allison, MA, Criqui, MH & Wright, CM Sistēmiskas kalcificētas aterosklerozes modeļi un riska faktori. Arterioscler Thromb Vasc Biol 24, 331–336 (2004).
5. Ketelers, M. et al. Kalcija regulējošo proteīnu trūkumi dialīzes pacientiem: jauna sirds un asinsvadu kalcifikācijas koncepcija urēmijas gadījumā. Kidney Int Suppl 84, S84–87 (2003).
6. Kapustin, A. & Shanahan, CM Asinsvadu pārkaļķošanās mērķa noteikšana: cietā mērķa mīkstināšana. Curr Opin Pharmacol 9, 84–89 (2009).
7. Kapustin, AN & Shanahan, CM Asinsvadu gludo muskuļu šūnu matricas pūslīšu kalcija regulēšana. Trends Cardiovasc Med 22, 133–137 (2012).
8. Doherty, TM et al. Kalcifikācija aterosklerozes gadījumā: kaulu bioloģija un hronisks iekaisums artēriju krustcelēs. Proc Natl Acad Sci USA 100, 11201–11206 (2003).
9. Khan, SR, Rodriguez, DE, Gower, LB & Monga, M. Randall plāksnīšu asociācija ar kolagēna šķiedrām un membrānas pūslīšiem. J Urol 187, 1094–1100 (2012).
10. Price, PA, Nguyen, TM & Williamson, MK Seruma fetuīna-minerālu kompleksa bioķīmiskais raksturojums. J Biol Chem 278, 22153-22160 (2003).
11. Price, PA, Williamson, MK, Nguyen, TM & Than, TN Fetuīna-minerālu kompleksa līmenis serumā korelē ar artēriju kalcifikāciju žurkām. J Biol Chem 279, 1594-1600 (2004).
12. Heiss, A. et al. Fetuīna-A un skābo seruma proteīnu hierarhiskā loma kalcija fosfāta daļiņu veidošanā un stabilizācijā. J Biol Chem 283, 14815–14825 (2008).
13. Bertazzo, S. et al. Nanoanalītiskā elektronu mikroskopija atklāj fundamentālu ieskatu cilvēka sirds un asinsvadu audu kalcifikācijā. Nat Mater 12, 576–583 (2013).
14. Martel, J. & Young, JD Apgalvotās nanobaktērijas cilvēka asinīs kā kalcija karbonāta nanodaļiņas. Proc Natl Acad Sci USA 105, 5549–5554 (2008).
15. Young, JD et al. Iespējamās nanobaktērijas ir normālas kalcija homeostāzes fizioloģiskas paliekas un kultūras blakusprodukti. Plos One 4, e4417 (2009).
16. Young, JD et al. Kalcija un apatīta granulāciju raksturojums serumā kā pleomorfiski minerālproteīnu kompleksi un kā iespējamo nanobaktēriju prekursori. Plos One 4, e5421 (2009).
17. Wu, CY, Martel, J., Young, D. & Young, JD. Fetuīna-A/albumīna minerālu kompleksi, kas atgādina kalcija granulas serumā un iespējamās nanobaktērijas: dubultās kavēšanas-sēšanas koncepcijas demonstrēšana. Plos One 4, e8058 (2009).
18. Young, JD & Martel, J. The rise and fall of nanobacteria. Sci Am 302, 52–59 (2010).
19. Martel, J., Wu, CY & Young, JD. Gamma starojuma apstarotā seruma, ko izmanto kā barotāju kultūrā, kritisks novērtējums un iespējamo nanobaktēriju un pārkaļķojošo nanodaļiņu demonstrēšana. Plos One 5, e10343 (2010).
20. Martel, J. et al. Visaptveroša minerālu nanodaļiņu proteomiskā analīze, kas iegūta no cilvēka ķermeņa šķidrumiem un analizēta ar šķidruma hromatogrāfijas-tandēma masas spektrometriju. Anal Biochem 418, 111–125 (2011).
