Pirmā daļa Sērūdeņraža loma nieru fizioloģijā un slimību stāvokļos
Jun 13, 2023
Abstrakts
Sērūdeņradis (H2S), endogēns gāzveida signālu raidītājs, ir guvis atzinību tā fizioloģiskās iedarbības dēļ. Šajā pārskatā mūsu mērķis ir apkopot un apspriest esošos pētījumus par H2S lomu nieru funkcijās un nieru slimībās, kā arī pamatā esošos mehānismus. H2S galvenokārt ražo četri ceļi, un nieres ir galvenie orgāni, kas ražo H2S. Iepriekšējie pētījumi ir parādījuši, ka H2S var ietekmēt vairākus signalizācijas ceļus, izmantojot sulfhidratāciju. Nieru fizioloģijā H2S veicina nieru izdalīšanos, regulē renīna izdalīšanos un palielina ATP veidošanos kā skābekļa sensoru. H2S ir iesaistīts arī nieru slimību attīstībā. H2S ir saistīts ar nieru išēmiju/reperfūziju un cisplatīna un sepses izraisītu nieru slimību. Hronisku nieru slimību, īpaši diabētiskās nefropātijas, hipertensīvās nefropātijas un obstruktīvas nieru slimības gadījumā H2S mazina slimības progresēšanu, regulējot oksidatīvo stresu, iekaisumu un renīna-angiotenzīna-aldosterona sistēmu. Neskatoties uz eksperimentālo pētījumu uzkrātajiem pierādījumiem, kas liecina par H2S donoru iespējamo lomu nieru slimību ārstēšanā, šiem rezultātiem ir nepieciešama turpmāka klīniskā tulkošana. Tāpēc izpratnes paplašināšana par H2S var ne tikai veicināt mūsu turpmāku izpratni par nieru fizioloģiju, bet arī likt pamatu H2S pārveidošanai par konkrētu nieru slimību mērķi.
Atslēgvārdi
Ūdeņraža sulfīds; sulfhidrācija; nieru fizioloģija; akūts nieru bojājums; hroniska nieru slimība.

Noklikšķiniet šeit, lai iegūtuCistanche priekšrocības
Ievads
Sērūdeņradis (H2S) ir toksiska, bezkrāsaina gāze ar puvušu olu smaržu. Tas pastāv dabā, un to var atrast dabasgāzē, vulkāniskajās emisijās un naftā [1]. 1989. gadā Warenycia un Goodwin [2] pirmo reizi pierādīja, ka cilvēka organismā ir H2S, kas galvenokārt pastāv smadzenēs, un norādīja, ka smadzeņu stumbrs ir jutīgāks pret eksogēnu H2S nekā citas smadzeņu daļas. H fizioloģiskā funkcija2S tikai nesen tika pakāpeniski atzīts. Augsta H koncentrācija2S var izraisīt pilnīgu šūnu elpošanas inhibīciju, mitohondriju membrānas potenciāla depolarizāciju un superoksīda veidošanos [3]. Zems H līmenis2S var regulēt homeostatiskos mehānismus, piemēram, asinsspiediena (BP) kontroli un apoptozi, un piedalīties patoloģiskos mehānismos, tostarp oksidatīvajā stresā (OS) un iekaisumā [4, 5]. Nierēs H2S ir aktīvi iesaistīts nieru regulēšanā, un H2S ražošanas traucējumi ir saistīti ar daudzu nieru slimību rašanos un attīstību [6]. Lai gan eksogēnā H2Ir pierādīts, ka S spēlē galveno lomu dažādu nieru bojājumu dzīvnieku modeļu mazināšanā, tā specifiskais molekulārais mehānisms nav zināms.
Šajā pārskatā mēs vispirms aprakstām H2S paaudze un funkcijas. Tālāk mēs iepazīstinām ar H lomu2S nieru fizioloģijā. Turklāt mēs apspriežam H2S kā saistītu faktoru nieru slimību rašanās un progresēšanā un atklāj dažus mehānismus. Visbeidzot, mēs apkopojam H pielietojumu2S donori un inhibitori preklīniskajā darbā un loģiski novērtē H terapeitisko potenciālu2S nieru slimībās.

Cistanche tubulosa
H2S paaudze un funkcijas
Lai gan sākotnēji tika uzskatīts tikai par toksisku gāzi, H2S tagad ir atzīta par gāzveida signālu molekulu, kas savā ziņā ir līdzīga slāpekļa oksīdam (NO) un oglekļa monoksīdam (CO) [7]. Atšķirībā no NO un CO, H2S ir skābs, kas ļauj tam izšķīst ūdenī. Turklāt tāpēc, ka H2S ir ļoti lipofīls, tas var brīvi izplatīties uz visu šūnu tipu šūnu membrānām [8]. Fermenti, kas ir atbildīgi par endogēno H veidošanos2S ietver cistationīna-b-sintāzi (CBS), cistationīna-c-liāzi (CSE) un mitohondriju 3-merkaptopiruvāta sērtransferāzi (3-MST) [9]. Gan CBS, gan CSE ražo endogēno H2S citozolā, savukārt 3–MST ražo endogēno H2S mitohondrijās [4,10]. Endogēno H2S ražo četros galvenajos veidos. Pirmajā mehānismā L-homocisteīns un serīns ražo L-cistationīnu CBS iedarbībā; pēc tam CSE L-cistationīns tiek pārveidots par L-cisteīnu. Visbeidzot, H2S veidojas procesā, ko citoplazmā mediē CBS un CSE [6]. Otrajā mehānismā CSE reaģē ar L-homocisteīnu, veidojot H2S, a-ketobutirātu un L-homolantionīnu [4]. Trešajā mehānismā cisteīna aminotransferāze pārvērš L-cisteīnu par 3-merkaptopiruvātu (3-MP), ko pēc tam izmanto 3-MST H2S ražošanai mitohondrijās [11]. Pēdējā mehānismā D-aminoskābes oksidāze veicina D-cisteīna pārveidošanu par 3-MP, un pēc tam H2S tiek ražots 3-MST iedarbībā. Ir vērts atzīmēt, ka nākamajam solim 3–MP ir jāimportē mitohondrijās. Nierēs galvenais substrāts H2S ražošanai ir D-cisteīns, un H2S no D-cisteīna ir daudz vairāk nekā no L-cisteīna [12] (1. attēls).
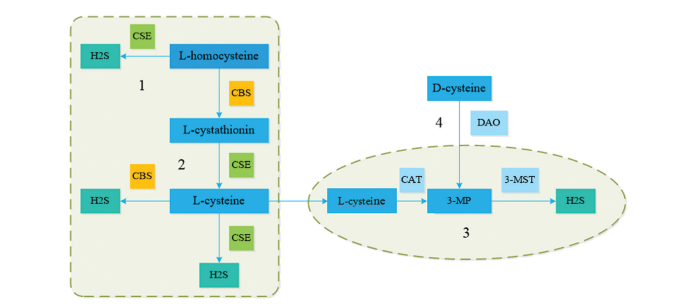
1. attēls. H2S endogēnā sintēze četros veidos. (A) CSE katalizē L-homocisteīna reakciju, lai izraisītu H2S veidošanos. (B) CBS reaģē ar L-homocisteīnu, palielinot L-cistationīna veidošanos, kas pēc tam tiek pārveidots par L-cisteīnu, izmantojot CSE, kas tālāk ražo H2S. (C) CAT L-cisteīns tiek pārveidots par 3MP, un 3-MST katalizē 3MP reakciju, lai izraisītu H2S veidošanos mitohondrijās. (D) DAO reaģē ar D-cisteīnu, veidojot 3MP, kas pēc tam nonāk mitohondrijās un kalpo kā substrāts H2S ražošanai. CBS (cistationīna b-sintāze); CSE (cistationīna c-liāze); CAT (cisteīna aminotransferāze); 3MP (3-merkaptopiruvāts); DAO (D-aminoskābes oksidāze); 3–MST (3–merkaptopiruvāta sērtransferāze).
Kā H2S veic bioloģiskās funkcijas? Jaunākie pētījumi ir snieguši atbildes. H2S var regulēt dažādus signalizācijas ceļus, kas ietekmē šūnu metabolismu. H2S ir iesaistīts signālu pārraidē pa signalizācijas ceļiem caur sulfhidrāciju, kura laikā tas reaģē ar dažādu mērķa proteīnu cisteīna atlikumiem, veidojot persulfīda saites. Sulfhidrācijas reaktivitāti nosaka cisteīna atlieku skābes disociācijas konstantes [13]. Mustafa et al. [14] atklāja, ka aptuveni 10–25 procentus aknu proteīnu var aktivizēt ar S-sulfhidrāciju, piemēram, aktīnu, tubulīnu un gliceraldehīda-3-fosfāta dehidrogenāzi. S-sulfhidrācija ir būtiska aknu proteīnu funkcijām; piemēram, tas uzlabo gliceraldehīda-3-fosfāta dehidrogenāzes aktivitāti un aktīna polimerizāciju. H2S ir no endotēlija iegūts hiperpolarizējošais faktors, kas var izraisīt asinsvadu endotēlija un gludo muskuļu šūnu hiperpolarizāciju un vazodilatāciju. Šo vazodilatāciju galvenokārt panāk, aktivizējot pret ATP jutīgos, vidējas un mazas vadītspējas kālija kanālus, un vissvarīgākais kanālu aktivācijas solis ir S-sulfhidrācija [15]. H2S piedalās iekaisuma reakcijās kā kurjermolekula, un sulfhidrācijas pakārtotā ietekme ietekmē kodolfaktoru jB (NF–jB). NF-jB ir galvenā loma iekaisuma reakcijā šūnās. Nil Kantha et al. [5] atklāja, ka audzēja nekrozes faktors-a (TNF-a) var stimulēt CSE transkripciju, lai radītu H2S. H2S sulfhidrē p65 Cys38, uzlabojot tā saistīšanos ar koaktivatora ribosomu proteīnu S3, tādējādi regulējot NF-jB kodolfunkcijas. Pelēm ar CSE deficītu p65 nevar pašhidratēt, kā rezultātā samazinās NF-jB mērķa gēna aktivitāte. Proteīna tirozīna fosfatāze-1B atrodas endoplazmatiskā retikuluma (ER) citoplazmas virsmā un ir saistīta ar ER stresa signalizāciju. H2S izraisīta proteīna tirozīna fosfatāzes-1B sulfhidrācija piedalās ER stresa reakcijā [16]. P66Shc ir mitohondriju redokssignalizācijas augšējais aktivators. Reaģējot uz OS, p66Shc tiek aktivizēts, izmantojot proteīnkināzes C-bII mediētu fosforilāciju pie Ser36. Xie et al. [17] atklāja, ka H2S samazina p66Shc fosforilēšanos, izmantojot Cys59 atlieku sulfhidratāciju, tādējādi samazinot reaktīvo skābekļa sugu (ROS) mitohondriju veidošanos un panākot antioksidantu iedarbību. Kodolfaktors — ar eritroīdu 2 saistītais faktors 2 (Nrf2) ir galvenais antioksidantu atbildes regulators. Parasti Nrf2 ir visuresošs un ātri noārdās proteasomā, iedarbojoties ar Kelch līdzīgu ECH saistītā proteīna 1 (Keap1). Ir ziņots, ka nātrija sulfīds (NaHS) ir S-sulfhidril Keap1 pie Cys151 un veicina Nrf2 kodola translokāciju [18].

Cistanche piedeva
H2S veidošanās nierēs un tās loma nieru fizioloģijā
1. H2S veidošanās nierēs
Dažos pētījumos ir atklāts, ka trīs enzīmi, kas ražo endogēno H2S, ir ļoti izteikti noteiktos audos, piemēram, nierēs [19]. CBS, CSE un 3–MST var noteikt nieru proksimālajās kanāliņos. CSE galvenokārt izpaužas arī nieru glomerulos, intersticiālajās un interlobulārajās artērijās [19,20]. Normālos apstākļos CSE proteīns tiek ekspresēts visaugstākajā līmenī nierēs, sasniedzot 20 reizes lielāku līmeni nekā CBS. Sprague-Dawley žurku nieru audos ir visi trīs H2S ražojošie enzīmi, un CSE mRNS tiek ekspresēta daudz biežāk nekā 3MST un CBS mRNS [4]. Tāpēc CSE ir vadošā loma H2S ražošanā [21,22]. CBS un CSE sinerģiski ražo H2S, un šie divi enzīmi var kopīgi palielināt endogēnā H2S veidošanos nierēs [23].
Nierēs ir identificēti trīs tradicionālie H2S sintezēšanas ceļi (ietver CSE, CBS un 3-MST kopā ar cisteīna aminotransferāzi), kā aprakstīts sadaļā "H2S ģenerēšana un funkcijas". Tāpēc mēs koncentrējāmies uz ceturto H2S paaudzes ceļu, proti, DAO/3 – MST ceļu [24]. Šajā ceļā D-cisteīns tiek pārveidots par 3-MP ar peroksisomu izvietotu DAO. Pateicoties metabolītu apmaiņai starp peroksisomām un mitohondrijiem, 3–MP tiek importēts mitohondrijās un katalizēts H2S ar 3–MST [24] (1. attēls). Shibuya et al. parādīja, ka nieru lizāts var ražot 60 reizes vairāk H2S, ja D-cisteīns tiek izmantots kā substrāts, nekā tad, ja lieto L-cisteīnu [12]. Unikālā DAO / 3 – MST ceļa atklāšana nierēs un smadzenēs var nozīmēt 3–MST mediētas H2S veidošanās nozīmīgu lomu šajos orgānos. Šo iespēju ir vērts izpētīt sīkāk.
2. H2S nieru fizioloģijā
2.1. H2S ietekme uz nieru ekskrēcijas funkciju
H2S ir svarīga loma nieru ekskrēcijā. Xia et al. atklāja, ka gan CBS, gan CSE var ražot H2S nierēs un, ja kāds no enzīmiem tiek inhibēts, otra ekspresija palielinās, lai to kompensētu. Viņi arī atklāja, ka anestēzētām Sprague-Dawley žurkām NaHS infūzija nieru artērijā var palielināt nieru asins plūsmu un glomerulārās filtrācijas ātrumu (GFR). Filtrācijas ātruma palielināšanās dēļ šie autori spekulēja, ka H2S loma vazodilatējošajos asinsvados bija lielāka preglomerulārajās arteriolās nekā postglomerulārajās arteriolās. H2S var arī inhibēt Na-K-2Cl kotransporteru Henles cilpas augšupejošajā daļā un Na-K ATPāzes enzīmu, potenciāli palielinot nātrija un kālija izdalīšanos no urīna. Tāpēc H2S piedalās gan asinsvadu, gan kanāliņu darbībā nierēs [23].

Cistanche tabletes
2.2. H2S kā skābekļa sensors
H2S var darboties kā skābekļa (O2) sensors, lai atjaunotu O2 līdzsvaru. Šī parādība ir apstiprināta dažādos O2 uztverošos audos, piemēram, karotīdo ķermenī, virsnieru smadzenēs un citos ķīmiski uztverošajos audos, kā arī gludajos muskuļos sistēmiski. un elpceļi un elpceļi [25]. H2S metabolisms ir ļoti atkarīgs no O2 koncentrācijas [25]. Fizioloģiskos apstākļos pO2 ir samazināts nieru smadzenēs, un H2S oksidācija negatīvi korelē ar pO2 mitohondrijās, tāpēc H2S aktivitāte medulā, visticamāk, ir augstāka nekā nieru garozā [4]. H2S, kas uzkrājas palielinātā daudzumā nieru medulās hipoksijas apstākļos, var atjaunot O2 piegādi, palielinot medulāro asins plūsmu [26]. Turklāt pētījumi ir parādījuši, ka pietiekama skābekļa apstākļos CBS un CSE līmenis mitohondrijās ir zems. Kad rodas hipoksija, palielinās CBS un CSE koncentrācija, kas palielina H2S veidošanos [27, 28]. H2S kalpoja kā elektronu donors un palielina ATP ražošanu [27]. Hipoksija ir vissvarīgākais riska faktors daudzu nieru slimību patoģenēzei un progresēšanai. Endogēns H2S deficīts var vēl vairāk veicināt traucētu medulāro oksigenāciju un saasināt nieru slimību rašanos un attīstību [26]. Tomēr konkrētais mehānisms joprojām ir neskaidrs un ir jāturpina pētīt.
2.3. H2S modulē renīna izdalīšanos
H2S vājina renīna-angiotenzīna-aldosterona sistēmas (RAAS) patoloģisko signālu pārraidi, lai saglabātu nieru darbību. RAAS ir humorāla regulēšanas sistēma, kas sastāv no hormoniem un atbilstošiem enzīmiem, kas regulē ūdens un nātrija izdalīšanos. Renīna izdalīšanās no jukstaglomerulārajām šūnām nosaka renovaskulārās hipertensijas rašanos un attīstību, procedūru koriģē ar intracelulāro 30–50 –ciklisko adenozīna monofosfātu (cAMP). Ir ziņots, ka H2S samazina cAMP, inhibējot adenilāta ciklāzes aktivitāti, tādējādi regulējot renīna izdalīšanos un kontrolējot BP [29, 30]. Ar renīnu bagāto nieru šūnu primārajās kultūrās NaHS ievērojami samazina intracelulārā cAMP līmeni un samazina renīna aktivitāti. Ir konstatēts, ka Dāla žurku modelī augsta sāls izraisītas hipertensijas gadījumā ārstēšana ar H2S inhibē RAAS sistēmas aktivāciju nierēs un regulē BP [31]. H2S arī regulē BP, izmantojot angiotenzīnu konvertējošo enzīmu, kas pieder RAAS sistēmai. Cilvēka endotēlija šūnās H2S var tieši ietekmēt cinku angiotenzīnu konvertējošā enzīma aktīvajā centrā [32].

Standartizēta Cistanche
Īsāk sakot, H2S ir galvenā loma nieru fizioloģijā; tomēr ir nepieciešama turpmāka izpēte, lai noteiktu konkrētos iesaistītos mehānismus.
Atsauces
[1] Rodrigues C, Percival SS. Glutationa, ķiploku atvasinājumu un sērūdeņraža imūnmodulējošā iedarbība. Uzturvielas. 2019;11(2):295.
[2] Warenycia MW, Goodwin LR, Benishin CG u.c. Akūta saindēšanās ar sērūdeņradi. Smadzeņu stumbra selektīvās sulfīda uzņemšanas demonstrēšana, mērot smadzeņu sulfīda līmeni. Biochem Pharmacol. 1989;38(6):973–981.
[3] Wedmann R, Bertlein S, Macinkovic I u.c. Darbs ar "H2S": fakti un šķietami artefakti. Slāpekļa oksīds. 2014; 41:85–96.
[4] Koning AM, Frenay AR, Leuvenink HG u.c. Sērūdeņradis nieru fizioloģijā, slimībās un transplantācijā – nieru aizsardzības smarža. Slāpekļa oksīds. 2015;46:37–49.
[5] Sen N, Pols BD, Gadalla MM u.c. Ar sērūdeņradi saistītā NF-jB sulfhidrācija veicina tā antiapopotiskās darbības. Mol Cell. 2012;45(1):13–24.
[6] Feliers D, Lee HJ, Kasinath BS. Sērūdeņradis nieru fizioloģijā un slimībās. Antioksīda redoksa signāls. 2016;25(13):720–731.
[7] Wen YD, Wang H, Zhu YZ. Sērūdeņraža zāļu izstrāde sirds un asinsvadu slimībām. Oxid Med Cell Longev. 2018;2018:4010395.
[8] Mathai JC, Missner A, K€ ugler P, et al. Sērūdeņraža transportēšanai uz membrānu nav nepieciešams veicinātājs. Proc Natl Acad Sci USA. 2009;106(39): 16633–16638.
[9] Yetik-Anacak G, Sevin G, Ozzayım O u.c. Sērūdeņradis: jauns mehānisms asinsvadu aizsardzībai ar resveratrolu oksidatīvā stresa apstākļos peles aortā. Vascul Pharmacol. 2016;87:76–82.
[10] Ngowi EE, Sarfraz M, Afzal A u.c. Sērūdeņraža donoru loma parastās nieru slimībās. Front Pharmacol. 2020;11:564281.
[11] Modis K, Coletta C, Erdelyi K u.c. Intramitohondriju sērūdeņraža ražošana, ko veic 3- merkaptopiruvāta sērtransferāze, uztur mitohondriju elektronu plūsmu un atbalsta šūnu bioenerģētiku. Faseb J. 2013;27(2):601–611.
[12] Shibuya N, Koike S, Tanaka M u.c. Jauns ceļš sērūdeņraža ražošanai no D-cisteīna zīdītāju šūnās. Nat Commun. 2013; 4:1366.
[13] Pols BD, Snyder SH. H2S signalizācija, izmantojot proteīnu sulfhidratāciju un tālāk. Nat Rev Mol Cell Biol. 2012;13(8):499–507.
[14] Mustafa AK, Gadalla MM, Sen N u.c. H2S signāli caur proteīna S-sulfhidrāciju. Zinātniskais signāls. 2009. gads; 2(96):ra72.
[15] Mustafa AK, Sikka G, Gazi SK u.c. Sērūdeņradis kā no endotēlija iegūts hiperpolarizējošais faktors sulfhidrē kālija kanālus. Circ Res. 2011; 109(11): 1259–1268.
[16] Krishnan N, Fu C, Pappin DJ u.c. H2S izraisīta fosfatāzes PTP1B sulfhidrācija un tās loma endoplazmatiskā retikuluma stresa reakcijā. Zinātniskais signāls. 2011;4(203):ra86.
[17] Xie ZZ, Shi MM, Xie L u.c. P66Shc sulfātēšana pie cisteīna59 mediē sērūdeņraža antioksidantu iedarbību. Antioksīda redoksa signāls. 2014; 21(18): 2531–2542.
[18] Yang G, Zhao K, Ju Y u.c. Sērūdeņradis aizsargā pret šūnu novecošanos, izmantojot Keap1 S-sulfhidrāciju un Nrf2 aktivizēšanu. Antioksīda redoksa signāls. 2013;18(15):1906–1919.
[19] Kamoun P. Endogēnā sērūdeņraža ražošana zīdītājiem. Aminoskābes. 2004;26(3):243–254.
[20] Zhang S, Pan C, Zhou F u.c. Sērūdeņradis ir potenciāls terapeitiskais mērķis fibrozes gadījumā. Oxid Med Cell Longev. 2015;2015:593407.
[21] Kabil O, Vitvitsky V, Xie P u.c. Transsulfurācijas enzīmu kvantitatīvā nozīme H2S ražošanā peles audos. Antioksīda redoksa signāls. 2011;15(2):363–372.
[22] Sun HJ, Wu ZY, Cao L u.c. Sērūdeņradis: nesenie panākumi un perspektīvas diabētiskās nefropātijas ārstēšanā. Molekulas. 2019;24(15):2857.
[23] Xia M, Chen L, Muh RW u.c. Sērūdeņraža, jaunas gāzveida bioaktīvas vielas, ražošana un darbība nierēs. J Pharmacol Exp Ther. 2009;329(3):1056–1062.
[24] Cao X, Bian JS. Sērūdeņraža loma nieru sistēmā. Front Pharmacol. 2016; 7:385. [25] Olsons KR. Sērūdeņradis kā skābekļa sensors. Antioksīda redoksa signāls. 2015;22(5):377–397.
[26] Bełtowski J. Hipoksija nieru smadzenēs: ietekme uz sērūdeņraža signalizāciju. J Pharmacol Exp Ther. 2010;334(2):358–363.
[27] Teng H, Wu B, Zhao K u.c. Skābeklijutīga cistationīna b-sintāzes mitohondriju uzkrāšanās, ko mediē Lon proteāze. Proc Natl Acad Sci USA. 2013;110(31):12679–12684.
[28] Fu M, Zhang W, Wu L u.c. Sērūdeņraža (H2S) metabolisms mitohondrijās un tā regulējošā loma enerģijas ražošanā. Proc Natl Acad Sci USA. 2012. gads; 109(8):2943–2948.
[29] Lu M, Liu YH, Goh HS u.c. Sērūdeņradis inhibē plazmas renīna aktivitāti. J Am Soc Nephrol. 2010; 21(6): 993–1002.
[30] Liu YH, Lu M, Xie ZZ u.c. Sērūdeņradis novērš sirds mazspējas attīstību, kavējot renīna izdalīšanos no tuklajām šūnām ar izoproterenolu ārstētām žurkām. Antioksīda redoksa signāls. 2014;20(5):759–769.
[31] Huang P, Chen S, Wang Y u.c. Zemāk regulētais CBS / H2S ceļš ir iesaistīts augsta sāls izraisītā hipertensijā Dāla žurkām. Slāpekļa oksīds. 2015;46: 192–203.
[32] Laggner H, Hermann M, Esterbauer H u.c. Jaunais gāzveida vazorelaksants sērūdeņradis inhibē endotēlija šūnu angiotenzīnu konvertējošā enzīma aktivitāti. J Hipertensija. 2007;25(10):2100–2104.
Jianan Feng, Xiangxue Lu, Han Li un Shixiang Wang
Nefroloģijas nodaļa, Pekinas Chao-Yang slimnīca, Capital Medical University, Pekina, Ķīna






