Otrā daļa Endotēlija šūnu disfunkcija un paaugstināts kardiovaskulārais risks pacientiem ar hronisku nieru slimību
Jun 07, 2023
PALIELINĀTA ENDOTĒLIĀLO ŠŪNU DISFUNKCIJA HNS
Endotēlija šūnu disfunkcija HNS kontekstā ir plaši pētīta gan pētījumos ar dzīvniekiem, gan pacientiem (1. Kopumā šie pētījumi atklāja samazinātu no endotēlija atkarīgu vazodilatāciju, endotēlija glikokaliksa bojājumus, palielinātu endotēlija caurlaidību, kā arī palielinātas proinflammatoriskās un protrombotiskās īpašības. Līdztekus makrovaskulāro endotēlija šūnu disfunkcijai CKD ir saistīta ar mikrovaskulāru disfunkciju un retināšanu. Turklāt HNS pacientiem arvien biežāk novēro mediālu kalcifikāciju, kas ir saistīta ar palielinātu artēriju stīvumu.77,78 Apvienojumā ar asinsvadu sieniņas un imūnsistēmas novecošanas īpašībām79 šīs patofizioloģiskās izmaiņas ir pamatā priekšstatam par HNS kā artēriju stīvumu. pastiprināta asinsvadu novecošanās.80
1. Ieskats no pētījumiem par dzīvniekiem
CKD dzīvnieku modeļi ir snieguši mums daudz vērtīgu ieskatu par CKD izraisītu endotēlija šūnu disfunkciju, jo tie ļauj in vivo novērtēt endotēlija (šūnu) funkciju. Ir pierādīts, ka HNS indukcija žurkām samazina no endotēlija atkarīgu relaksāciju,81 palielina krūšu aortas endotēlija caurlaidību82 un palielina mikrovaskulāro caurlaidību, kas bija saistīta ar endotēlija virsmas slāņa zudumu žurku modelī. 5/6-nefrektomizētām žurkām tika atklāti plaši glikokaliksa bojājumi, par ko liecina samazināts aortas glikokaliksa biezums un paaugstināts glikokaliksa komponenta sindekāna-1 līmenis plazmā. .84 Turklāt HNS peļu modeļos endotēlija šūnu disfunkcija ir pierādīta makro un mikrovaskulārā līmenī, ko ilustrē ievērojams glikokaliksa biezuma un blīvuma samazinājums, glikokaliksa komponentu pastiprināta ekspresija, samazināta endotēlija atkarīgā relaksācija, reaģējot uz acetilholīnu. aortas gredzeni un palielināta ICAM-1 un VCAM-1 endotēlija ekspresija.85–87 Turklāt, izmantojot preglomerulāro artēriju mikrodatortomogrāfijas attēlveidošanu, Ēlings et al47 parādīja, ka nieru disfunkcija izraisīja asinsvadu samazināšanos. diametrs un asinsvadu atzarojums, kā arī asinsvadu līkuma palielināšanās 3 progresējošas nieru slimības un nieru fibrozes peļu modeļos. Kombinācijā ar apolipoproteīna E deficīta fonu HNS indukcija turklāt izraisīja lielāku aplikuma slogu, kas norāda uz augstāku aterosklerozes risku HNS.85
2. Pacientu pētījumu ieskati
2.1. Samazināta no makrovaskulārā endotēlija atkarīga vazodilatācija HNS
Runājot par perifērās mikrovaskulārās sistēmas funkcionālajām reakcijām, kā novērtēts ar mutes un nagu sērgu, vairāki pētījumi ir parādījuši, ka HNS pacientiem ir būtiski endotēlija atkarīgās vazodilatācijas traucējumi,62–64, kas palielinās, palielinoties HNS smagumam,64,88 neatkarīgi prognozē kardiovaskulāro iznākumu64 un korelē ar kreisā kambara hipertrofiju.65 Arī no endotēlija neatkarīga vazodilatācija, ko mēra ar pleca mutes un nagu sērgu analīzi pēc nitroglicerīna injekcijas, bija ievērojami samazināta pacientiem ar progresējošu HNS, bet ne pacientiem ar koronāro artēriju slimību un veselīgu nieru darbību, un asinsvadu pārkaļķošanās tika ieteikta kā potenciālais pamatā esošais mehānisms.89 Turklāt vairāki pētījumi parādīja, ka, progresējot HNS, palielinās artēriju stīvums,67,68,70, lai gan citi nevarēja apstiprināt korelāciju starp PWV un nieru darbību pēc kovariātu pielāgošanas (tostarp, bet ne tikai, vecums, dzimums , blakusslimības un medikamentu lietošana).69

Noklikšķiniet šeit, lai uzzinātu par Cistanche ietekmi uz nierēm
2.2 MVD un retināšana CKD gadījumā
HNS ir saistīta gan ar perifērās, gan koronārās mikrovaskulārās sistēmas pastiprinātu disfunkciju, un, HNS progresējot, strukturālais un funkcionālais kapilāru blīvums samazinās. vidēji 32 procenti 49; to jau varēja novērot HNS3-4, un to pavadīja pastiprināta endotēlija-mezenhimālā pāreja un miokarda fibroze.49,91 Lai gan HNS pacientiem bieži ir blakusslimības, kas spēcīgi veicina MVD attīstību (piemēram, hipertensija un diabēts), HNS izraisīta MVD jeb urēmiskā angiopātija pārsniedz šos faktorus, un rezultātā radusies mikrovaskulāra disfunkcija vēl vairāk pastiprina HNS progresēšanu. Pierādījumi ir iegūti no HNS dzīvnieku modeļiem, kā arī no HNS pacientu pētījumiem, kuros tika pierādīts, ka HNS izraisīta mikrovaskulāra retināšana notiek neviendabīgi, kā rezultātā veidojas lielas asinsvadu zonas.48,49
Vēnu un pirkstu pletismogrāfijas mērījumi liecināja par traucētu endotēlija atkarīgu vazodilatācijas reakciju no dialīzes atkarīgā CKD, 61, 66, lai gan Wang et al92 nenovēroja korelāciju starp aprēķināto GFR un reaktīvās hiperēmijas indeksu, ko mēra ar perifēro artēriju tonometriju. Koncentrējoties uz koronāro mikrovaskulāru disfunkciju, nesen veiktā sistemātiskā pārskatā ar metaanalīzi tika norādīts, ka HNS pacientiem ir ievērojami zemāka koronārās plūsmas rezerve, salīdzinot ar pacientiem, kuriem nav HNS.59 Tāpat kā vispārējā populācijā, samazināta koronārās plūsmas rezerve, kas liecina par koronāro mikrovaskulāro disfunkciju. prognozēt kardiovaskulāro risku pacientiem ar HNS, pat pēc pielāgošanas tradicionālajiem kardiovaskulārajiem riska faktoriem.60,93 Nieru funkcijas atjaunošana pēc nieres transplantācijas daļēji uzlaboja mikrovaskulāro funkciju, kas novērtēta ar sublingvālās mikrocirkulācijas un koronārās plūsmas rezerves analīzi, kas liecina, ka zināmā mērā mikrovaskulāras izmaiņas HNS ir atgriezeniskas.94,95
2.3. Endotēlija glikokaliksa bojājumi HNS
Pacientiem ar HNS serumā ir konstatēts paaugstināts glikokaliksa komponentu sindekāna-1 un hialuronāna līmenis kombinācijā ar paaugstinātu hialuronidāzes aktivitāti, un augstākais līmenis novērots HNS pacientiem, kuriem tiek veikta dialīze.71,84,96 Līdz ar to līnija, cilvēka endotēlija šūnu ārstēšana in vitro ar urēmisko serumu no pediatriskiem HNS pacientiem vai pieaugušajiem hemodialīzes pacientiem izraisīja glikokaliksa augstuma samazināšanos un endotēlija šūnu stīvumu.97 Glikokaliksa bojājumi tika apstiprināti HNS pacientu dermas biopsijās, kurās smaga krāsojuma samazināšanās ar ulex europaeus aglutinīnu-1 (lektīnu saistoši glikoproteīni un glikolipīdi) tika novērota biopsijās, kas iegūtas no nedialīzes atkarīgiem HNS pacientiem, kā arī hemodialīzes pacientiem.98 Perfūzijas robežzonas mērījumi, kā indikators glikokaliksa biezums, pētījumos ir mazāk konsekventi. Kamēr Vlahu et al96 novēroja perfūzijas robežas apgabala un perfūzijas diametra palielināšanos, Liew et al71 neatklāja būtiskas atšķirības perfūzijas robežapgabalā. Trīs mēnešus pēc nieres transplantācijas endotēlija glikokaliksa marķieri uzlabojās, jo samazinājās perfūzijas robežzona un pazeminājās sindekāna-1, sVCAM-1 un vWF līmenis serumā, salīdzinot ar līmeni pirms transplantācijas.99 Hialuronāna līmenis serumā saglabājās. nemainīgs.99

Cistanche ekstrakta kapsulas
2.4. Šķīstošie endotēlija veselības biomarķieri HNS
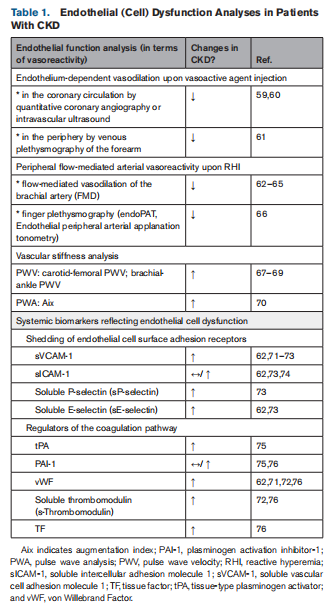
Sistēmiskie biomarķieri ir izmantoti, lai sniegtu ieskatu endotēlija šūnu disfunkcijas apjomā pacientiem ar paaugstinātu kardiovaskulāro risku (1. tabula). Disfunkcionāls endotēlijs parasti ražo mazāk NO, samazinoties eNOS ražošanai vai aktivitātei, taču īsais NO pussabrukšanas periods apgrūtina nolasīšanu, lai precīzi novērtētu endotēlija šūnu funkciju. Alternatīvi sistēmiski biomarķieri, kas izmantoti, pētot endotēlija šūnu disfunkciju, ietver sasmalcinātas iekaisuma izraisītu šūnu virsmas adhēzijas receptoru formas (piemēram, VCAM-1, ICAM-1 šķīstošās formas, P-selektīns un E- selektīns, un pēdējais tiek uzskatīts par visselektīvāko endotēlija šūnām).100 Tā kā endotēlijam ir svarīga hemostāzes regulējoša loma, bieži vien kvantitatīvi nosaka arī trombocītu aktivācijā un koagulācijā iesaistītās molekulas, lai novērtētu potenciāli disfunkcionāla endotēlija trombotiskās atbildes. Tas ietver vWF, šķīstošā trombomodulīna, tPA (audu tipa plazminogēna aktivatora) un PAI-1 (plazminogēna aktivācijas inhibitors-1; fibrinolīzes inhibitors) sistēmisku līmeni.100 101 Tomēr jāatzīmē, ka lielākā daļa no šiem sistēmiskajiem biomarķieriem nav specifiski iekaisušam vai bojātam endotēlijam un sniedz tikai netiešu ieskatu iespējamā endotēlija šūnu disfunkcijā.
Īpaši no dialīzes atkarīgiem pacientiem HNS stadijā 3-5, asimetriskā dimetilarginīna (eNOS inhibitora), L-arginīna (NO prekursora), sVCAM-1, sE-selektīna, sP līmenis plazmā un serumā. -selektīns, s-trombomodulīns, tPA, uPA (urokināzes tipa plazminogēna aktivators), TF un vWF bija paaugstināts (1. tabula). kā HNS smaguma marķieri.62,71 Pat viegli nieru darbības traucējumi ir neatkarīgi saistīti ar vWF un sVCAM-1 līmeni plazmā kā endotēlija aktivācijas marķieriem.74 HNS ietekme uz PAI sistēmisko līmeni{18 }} un sICAM-1 ir mazāk skaidri, svārstās no nemainīga62,74,76 līdz paaugstinātam līmenim HNS pacientiem, kuriem netiek veikta dialīze.73,75
MEHĀNISKI IESKATI ENDOTĒLIĀLO ŠŪNU DISFUNKCIJĀ CKD
Ir konstatēts, ka patofizioloģisko procesu daudzveidība veicina endotēlija šūnu disfunkciju HNS. Tie ietver hronisku zemas pakāpes iekaisumu, paaugstinātu oksidatīvo stresu, urēmisko toksīnu uzkrāšanos un ar to saistītās proteīnu un lipoproteīnu daļiņu pēctranslācijas modifikācijas, kā arī metabolisko acidozi un augstu simpātisku aktivāciju (3. līdz 5. attēls). Turklāt pacientiem ar CKD ir progresējošas asinsvadu novecošanās pazīmes, un viņiem ir asinsvadu pārkaļķošanās. Nākamajos punktos tiek apspriesta katra no šiem dažādajiem faktoriem mijiedarbība ar endotēlija šūnu disfunkciju CKD gadījumā. Tradicionālo kardiovaskulāro riska faktoru, piemēram, hipertensijas un cukura diabēta, kā biežas hroniskas nieru slimības un cēloņu ietekme netiek apspriesta.

Cistanche tubulosa
Hronisks zemas pakāpes iekaisums
Bojātajās nierēs neatrisināts zemas pakāpes iekaisums izraisa rezidentu nieru šūnas, lai ražotu proinflammatoriskus citokīnus un kemokīnus un izraisītu ECM nogulsnēšanos, kas veicina tubulointersticiālu fibrozi. Tādējādi hronisks zemas pakāpes iekaisums ir nozīmīgs HNS progresēšanas virzītājspēks.60 Turklāt samazināta nieru filtrācijas funkcija HNS izraisa sistēmisku urēmisku vidi, kas izraisa sistēmisku, hronisku zemas pakāpes iekaisumu, mainot HNS ekspresiju un izdalīšanos. proinflammatoriskie mediatori, piemēram, citokīni, asinīs.103 Zemas pakāpes iekaisuma pazīmes HNS ir paaugstināts sistēmiskais proinflammatorisko citokīnu līmenis IL-1, IL-6, TNF (audzēja nekrozes faktors)- , un hs-CRP (augstas jutības C-reaktīvais proteīns), kas uzkrājas asinīs palielinātas izdalīšanās, kā arī samazināta nieru klīrensa dēļ.104,105
Sistēmiski proinflammatoriskie biomarķieri ir saistīti ar HNS progresēšanu106, kā arī ar kardiovaskulāro risku pacientiem ar HNS.107 Piemēram, hs-CRP līmenis serumā var paredzēt kardiovaskulārus notikumus pacientiem ar HNS,108109 ar koriģētu kardiovaskulārās mirstības riska risku 1,94. vidējais novērošanas ilgums 10 gadi HNS3-4 pacientiem ar augstu CRP (lielāks par vai vienāds ar 3 mg/l), salīdzinot ar zemu CRP (<3 mg/L).109 Also, systemic levels of IL-6 correlated with a poor outcome in CKD, and both IL-6 and TNF-α could predict all-cause mortality in CKD5D patients after adjustment for age, sex, diabetes, smoking, baseline kidney function, protein-energy wasting as well as other inflammation biomarkers as hsCRP (high-sensitivity C-reactive protein).104,107 On the other hand, also the antiinflammatory IL-10 is upregulated in patients with CKD through increased secretion by uremic monocytes and reduced kidney clearance, with IL-10 counteracting the activated inflammatory response.104 Increased IL-10 levels were found to be positively correlated with cardiovascular events in CKD patients at follow-up, with increased IL-10 levels interpreted as an increased compensatory effect in an overall proinflammatory state in CKD patients.110
Antivielu izraisītā IL-1 blokāde CANTOS pētījumā (Kanakinumaba pretiekaisuma trombozes rezultātu pētījums) samazināja nopietnu nevēlamu kardiovaskulāru notikumu rašanos pacientiem ar vidēji smagu HNS (CKD3a) vidēji 3,7 gadu novērošanas laikā. .111 IL-6 bloķēšana 24 nedēļas pacientiem ar HNS3-5D un atlikušo iekaisuma risku RESCUE pētījumā ievērojami samazināja hs-CRP kā sistēmiskā iekaisuma marķieri, izmantojot ZEUS pētījumu (Zlitivekimab Cardiovascular Outcomes Study). ) pašlaik novērtē iespējamo ieguvumu kardiovaskulāro iznākumu ārstēšanā HNS{12}} pacientiem ar augstu atlikušā iekaisuma risku.112

Cistanche tabletes un sausais Cistanche
Hronisks iekaisums, kā arī iepriekš minētie citokīni ir saistīti ar endotēlija iekaisumu un endotēlija šūnu disfunkciju. Piemēram, ir zināms, ka IL-6 izraisa CRP veidošanos, gan IL-6113, gan CRP114 samazina endotēlija veidošanos un/vai eNOS aktivizēšanu un tādējādi NO kā būtisku molekulu asinsvadu veselības uzturēšanā. IL-6 arī aktīvi bojā endotēlija barjeru un palielina endotēlija caurlaidību, samazinot adherēnu savienojuma proteīna VE-kadherīna endotēlija ekspresiju caur transsignalizācijas ceļu115, kā arī ciešā savienojuma proteīna ZO{{7} savienojuma lokalizāciju. } caur STAT3 fosforilāciju.116 TNF samazināja no endotēlija atkarīgo vazodilatāciju peles aortā, palielinot superoksīda veidošanos, aktivējot NADPH oksidāzes117, un gan palielinātais TNF-, gan samazinātais NO var būt cēloņsakarība ar endotēlija apoptozi novecojušu žurku artērijās118.
Papildus paaugstinātam citokīnu līmenim pacientiem ar CKD ir paaugstināts ar bīstamību saistītu molekulāro raksturlielumu molekulu, piemēram, HMGB1, S100 proteīnu un uzlaboto glikācijas galaproduktu (AGE) līmenis, kas izraisa proinflammatoriskas reakcijas, salīdzinot ar RAGE (progresīva glikācijas galaprodukta receptoru), TLR. , un NLRP3 iekaisuma aktivācija. 119 120 Turklāt neitrofilu ekstracelulārie slazdi, ko ražo aktivēti neitrofīli, izraisa endotēlija iekaisumu un pastiprina TF ekspresiju un aktivitāti, tādējādi veicinot koagulāciju.121 Citi hroniska iekaisuma stāvokļa veicinātāji HNS ir zarnu trakta disbioze (toksīnu un disbioze79). sīkāk apspriests tālāk).
Zemas pakāpes iekaisuma stāvoklis tiek novērots ne tikai HNS, bet arī citu hronisku slimību gadījumā, kā arī novecojot, un tāpēc to sauc par iekaisumu.79 Kopumā zemas pakāpes iekaisums izraisa endotēlija šūnu disfunkciju, kā arī oksidatīvo stresu, kas savukārt pastiprina iekaisuma stāvokli, kā tālāk apspriests.
ATSAUCES
59. Jain V, Gupta K, Bhatia K, Rajapreyar I, Singh A, Zhou W, Klein A, Nanda NC, Prabhu SD, Bajaj NS. Koronārās plūsmas anomālijas hroniskas nieru slimības gadījumā: sistemātisks pārskats un metaanalīze. Ehokardiogr. 2022; 39:1382–1390. doi: 10.1111/echo.15445
60. Charytan DM, Skali H, Shah NR, Veeranna V, Cheezum MK, Taqueti VR, Kato T, Bibbo CR, Hainer J, Dorbala S u.c. Koronārās plūsmas rezerve prognozē sirds un asinsvadu nāves risku neatkarīgi no hroniskas nieru slimības stadijas. Kidney Int. 2018;93:501–509. doi 10.1016/j.kint.2017.07.025
61. Annuk M, Lind L, Linde T, Fellström B. Impaired endothelium-dependent vazodilatation in renāla mazspēja cilvēkiem. Nephrol Dial transplantācija. 2001;16:302–306. doi: 10.1093/ndt/16.2.302
62. Chen J, Hamm LL, Mohler ER, Hudaihed A, Arora R, Chen CS, Liu Y, Browne G, Mills KT, Kleinpeter MA u.c. Vairāku endotēlija disfunkcijas biomarķieru savstarpējā saistība ar hronisku nieru slimību. PLoS One. 2015;10:e0132047. doi: 10.1371/journal.pone.0132047
63. Kruger A, Stewart J, Sahityani R, O-Riordan E, Thompson C, Adler S, Garrick R, Vallance P, Goligorsky MS. Endotēlija disfunkcijas lāzera Doplera plūsmas noteikšana pacientiem beigu stadijas nieru slimībām: korelācija ar kardiovaskulāro risku. Kidney Int. 2006;70:157–164. doi: 10.1038/sj.ki.5001511
64. Yilmaz MI, Stenvinkel P, Sonmez A, Saglam M, Yaman H, Kilic S, Eyileten T, Caglar K, Oguz Y, Vural A u.c. Asinsvadu veselība, sistēmisks iekaisums un progresējoša nieru darbības samazināšanās; klīniskie noteicošie faktori un ietekme uz kardiovaskulārajiem rezultātiem. Nephrol Dial transplantācija. 2011;26:3537–3543. doi: 10.1093/ndt/gfr081
65. Poulikakos D, Ross L, Recio-Mayoral A, Cole D, Andoh J, Chitalia N, Sharma R, Kaski JC, Banerjee D. Kreisā kambara hipertrofija un endotēlija disfunkcija hroniskas nieru slimības gadījumā. Eur Sirds J Sirds un asinsvadu attēlveidošana. 2014;15:56–61. doi: 10.1093/ehjci/jet120
66. Hirata Y, Sugiyama S, Yamamoto E, Matsuzawa Y, Akiyama E, Kusaka H, Fujisue K, Kurokawa H, Matsubara J, Sugamura K u.c. Endotēlija funkcija un kardiovaskulāri notikumi hroniskas nieru slimības gadījumā. Int J Cardiol. 2014; 173:481–486. doi: 10.1016/j.ijcard.2014.03.085
67. Briet M, Bozec E, Laurent S, Fassot C, London GM, Jacquot C, Froissart M, Houillier P, Boutouyrie P. Artēriju stīvums un paplašināšanās vieglas vai vidēji smagas hroniskas nieru slimības gadījumā. Kidney Int. 2006; 69:350–357. doi: 10.1038/sj.ki.5000047
68. Yoon HE, Shin DI, J KD, Koh ES, Hwang HS, Chung S, Shin SJ. Brachialankle pulsa viļņa ātrums paredz nieru funkcijas un kardiovaskulāro notikumu samazināšanos hroniskas nieru slimības sākuma stadijā. Int. J Med Sci. 2013; 10:1430–1436. doi: 10.7150/ijms.6645
69. Kim CS, Kim HY, Kang YU, Choi JS, Bae EH, Ma SK, Kim SW. Pulsa viļņa ātruma un pulsa spiediena saistība ar nieru darbības samazināšanos. J Clin hipertensija (Grīnviča). 2014;16:372–377. doi 10.1111/jch.12302
70. Weber T, Ammer M, Gündüz D, Bruckenberger P, Eber B, Wallner M. Palielināto arteriālo viļņu refleksiju asociācija ar nieru funkcijas samazināšanos hroniskas nieru slimības 3. un 4. stadijā. Am J Hipertenss. 2011; 24:762–769. doi 10.1038/ajh.2011.45
71. Liew H, Roberts MA, Pope A, McMahon LP. Endotēlija glikokaliksa bojājumi nieru slimības gadījumā korelē ar urēmiskiem toksīniem un endotēlija disfunkciju. BMC Nephrol. 2021; 22:21. doi: 10,1186/s12882-020-02219-4
72. Jacobson SH, Egberg N, Hylander B, Lundahl J. Korelācija starp šķīstošiem endotēlija disfunkcijas marķieriem pacientiem ar nieru mazspēju. Esmu J. Nefrols. 2002;22:42–47. doi: 10.1159/000046673
73. Bonomini M, Reale M, Santarelli P, Stuard S, Settefrati N, Albertazzi A. Šķīstošo adhēzijas molekulu līmenis serumā hroniskas nieru mazspējas un dialīzes pacientiem. Nefrons. 1998;79:399–407. doi: 10.1159/000045084
74. Stam F, van Guldener C, Becker A, Dekker JM, Heine RJ, Bouter LM, Stehouwer CDA. Endotēlija disfunkcija veicina ar nieru darbību saistītu kardiovaskulāro mirstību populācijā ar vieglu nieru mazspēju: Hoorn pētījums. J Am Soc Nephrol. 2006;17:537–545. doi: 10.1681/ASN.2005080834
75. Kaminski TW, Pawlak K, Karbowska M, Mysliwiec M, Grzegorzewski W, Kuna J, Pawlak D. Asociācija starp urēmisko toksīnu-antranilskābi un fibrinolītiskās sistēmas aktivitāti predialīzes pacientiem dažādos hroniskas nieru slimības posmos. Int Urol Nephrol. 2018;50:127–135. doi: 10,1007/s11255-017-1729-1
76. Mezzano D, Tagle R, Panes O, Pérez M, Downey P, Muñoz B, Aranda E, Barja P, Thambo S, González F u.c. Endotēlija šūnu marķieri hroniskā urēmijā: saistība ar hemostatiskiem defektiem un nieru mazspējas smagumu. Thromb Res. 1997;88:6. doi: 10,1016/s0049-3848(97)00280-6
77. Guerin AP, London GM, Marchais SJ, Metivier F. Artēriju stīvums un asinsvadu kalcifikācijas beigu stadijas nieru slimībās. Nephrol Dial transplantācija. 2000;15:1014–1021. doi: 10.1093/ndt/15.7.1014
78. Holmar J, de la Puente-Secades S, Floege J, Noels H, Jankowski J, Orth-Alampour S. Urēmiskie toksīni, kas ietekmē sirds un asinsvadu kalcifikāciju: sistemātisks pārskats. Šūnas. 2020; 9:2428. doi: 10,3390/cells9112428
79. Kooman JP, Dekker MJ, Usvyat LA, Kotanko P, van der Sande FM, Schalkwijk CG, Shiels PG, Stenvinkel P. Iekaisums un priekšlaicīga novecošana progresējošas hroniskas nieru slimības gadījumā. Am J Physiol Renal Physiol. 2017;313:F938–F950. doi: 10.1152/ajprenal.00256.2017
80. Dai L, Qureshi AR, Witasp A, Lindholm B, Stenvinkel P. Agrīna asinsvadu novecošanās un šūnu novecošanās hroniskas nieru slimības gadījumā. Comput Struct Biotechnol J. 2019;17:721–729. doi 10.1016/j.csbj.2019.06.015
81. Wu-Wong JR, Kawai M, Chen Y, Wessale JL, Huang CJ, Wu MT, Nakane M. Diviem jauniem D vitamīna receptoru modulatoriem ar līdzīgām struktūrām ir atšķirīga hiperkalciēmijas iedarbība 5/6 nefrektomizētām urēmiskām žurkām. Esmu J. Nefrols. 2013;37:310–319. doi: 10.1159/000348755
82. Vila Cuenca M, Ferrantelli E, Meinster E, Pouw SM, Kovacevic I, de Menezes R, Niessen HW, Beelen RJ, Hordijk PL, Vervloet MG. D vitamīns mazina endotēlija disfunkciju urēmiskām žurkām un uztur cilvēka endotēlija stabilitāti. J Am Heart asoc. 2018;7:e008776. doi: 10.1161/JAHA.118.008776
83. Salmon AHJ, Ferguson JK, Burford JL, Gevorgyan H, Nakano D, Harper SJ, Bates DO, Peti-Peterdi J. Endotēlija glikokaliksa zudums saista albuminūriju un asinsvadu disfunkciju. J Am Soc Nephrol. 2012; 23:1339–1350. doi: 10.1681/ASN.2012010017
84. Padberg JS, Wiesinger A, di Marco GS, Reuter S, Grabner A, Kentrup D, Lukasz A, Oberleithner H, Pavenstadt H, Brand M u.c. Endotēlija glikokaliksa bojājumi hroniskas nieru slimības gadījumā. Ateroskleroze. 2014;234:335– 343. doi: 10.1016/j.ateroskleroze.2014.03.016
85. Six I, Gross P, Rémond MC, Chillon JM, Poirot S, Drueke TB, Massy ZA. Indoksilsulfāta kaitīgā ietekme uz asinsvadiem un perorāla adsorbenta AST atcelšana-120. Ateroskleroze. 2015; 243:248–256. doi: 10.1016/j.ateroskleroze.2015.09.019
86. Verkaik M, Juni RP, van Loon EPM, van Poelgeest EM, Kwekkeboom RFJ, Gam Z, Richards WG, Ter Wee PM, Hoenderop JG, Eringa EC u.c.; NIGRAM konsorcijs. FGF23 pasliktina perifēro mikrovaskulāro funkciju nieru mazspējas gadījumā. Am J Physiol Heart Circ Physiol. 2018;315:H1414–H1424. doi: 10.1152/ajpheart.00272.2018
87. Ermert K, Buhl EM, Klinkhammer BM, Floege J, Boor P. Endotēlija glikokaliksa samazināšana uz peritubulārajiem kapilāriem hroniskas nieru slimības gadījumā. Esmu J Pathol. 2023; 193:138–147. doi: 10.1016/j.ajpath.2022.11.003
88. Theodorakopoulou MP, Schoina M, Sarafidis P. Endotēlija un mikrovaskulārās funkcijas novērtējums CKD: vecākas un jaunākas metodes, saistītie riska faktori un attiecības ar rezultātiem. Esmu J. Nefrols. 2020;51:931–949. doi: 10.1159/000512263
89. Kopel T, Kaufman JS, Hamburg N, Sampalis JS, Vita JA, Dember LM. No endotēlija atkarīga un neatkarīga asinsvadu funkcija progresējošas hroniskas nieru slimības gadījumā. Clin J Am Soc Nephrol. 2017; 12:1588–1594. doi: 10.2215/CJN.12811216
90. Schoina M, Loutradis C, Memmos E, Dimitroulas T, Pagkopoulou E, Doumas M, Karagiannis A, Garyfallos A, Papagianni A, Sarafidis P. Mikrocirkulācijas funkcija pasliktinās ar progresējošām hroniskas nieru slimības stadijām neatkarīgi no arteriālās stīvuma un aterosklerozes. Hypertens Res. 2021; 44:179–187. doi: 10,1038/s 41440-020-0525-g
91. Charytan DM, Padera R, Helfand AM, Zeisberg M, Xu X, Liu X, Himmelfarb J, Cinelli A, Kalluri R, Zeisberg EM. Palielināta cirkulējošās angioģenēzes un slāpekļa oksīda inhibitoru koncentrācija pacientiem ar hronisku nieru slimību izraisa endotēlija pāreju uz mezenhimālu un miokarda fibrozi. Int J Cardiol. 2014; 176:99–109. doi: 10.1016/j.ijcard.2014.06.062
92. Wang L, Huang X, He W, Liu W, Yang J. Digitālā mikrovaskulārā reaktivitāte nesamazinās ar nieru darbības traucējumiem hroniskas nieru slimības gadījumā. BMC Nephrol. 2019; 20:288. doi: 10,1186/s12882-019-1484-x
93. Nakanishi K, Fukuda S, Shimada K, Miyazaki C, Otsuka K, Kawarabayashi T, Watanabe H, Yoshikawa J, Yoshiyama M. Prognostic value of coronary flow reserve on long-term kardiovaskulārie rezultāti pacientiem ar hronisku nieru slimību. Esmu J Cardiol. 2013; 112:928–932. doi: 10.1016/j.amjcard.2013.05.025
94. Caliskan Y, Oflaz H, Demirturk M, Yazici H, Turkmen A, Cimen A, Elitok A, Yildiz A. Koronārās plūsmas rezerves disfunkcija hemodialīzes un nieru transplantācijas pacientiem. Klina transplantācija. 2008; 22:785–793. doi: 10.1111/j.{7}}.2008.00879.x
95. Yeh YC, Chao A, Lee CY, Lee CT, Yeh CC, Liu CM, Tsai MK. Novērošanas pētījums par mikrocirkulāciju dialīzes pacientiem un nieru transplantācijas saņēmējiem. Eur J Clin Invest. 2017;47:630–637. doi 10.1111/eci.12784
96. Vlahu CA, Lemkes BA, Struijk DG, Koopman MG, Krediet RT, Vink H. Endotēlija glikokaliksa bojājumi dialīzes pacientiem. J Am Soc Nephrol. 2012;23:1900–1908. doi: 10.1681/ASN.2011121181
97. Fels B, Beyer A, Cazana-Perez V, Giraldez T, Navarro-Gonzalez JF, Alvarez de la Rosa D, Schaefer F, Bayazit AK, Obrycki L, Ranchin B u.c. Hroniskas nieru slimības ietekmi uz endotēlija glikokaliksa nanomehāniku ietekmē mineralokortikoīdu receptori. Int J Mol Sci. 2022;23:10659. doi: 10.3390/ijms231810659
98. Koch J, Hijmans RS, Ossa Builes M, Dam WA, Pol RA, Bakker SJL, Pas HH, Franssen CFM, van den Born J. Tiešie pierādījumi par endotēlija disfunkciju un glikokaliksa zudumu dermas biopsijās pacientiem ar hronisku nieru slimību un to saistība ar tilpuma pārslodzes marķieriem. Front Cell Dev Biol. 2021;9:733015. doi: 10.3389/fcell.2021.733015
99. Liew H, Roberts MA, McMahon LP. Endotēlija glikokaliksa marķieri uzlabojas pēc nieres transplantācijas. Kidney Blood Press Res. 2021;46:581–587. doi: 10.1159/000517317
100. Deanfield J, Halcox JP, Rabelink TJ. Endotēlija funkcija un disfunkcija: testēšana un klīniskā nozīme. Aprite. 2007;115:1285–1295. doi: 10.1161/CIRCULATIONAHA.106.652859
101. Martins FA, Mērfijs RP, Cummins PM. Trombomodulīns un asinsvadu endotēlijs: ieskats funkcionālajos, regulējošajos un terapeitiskajos aspektos. Am J Physiol Heart Circ Physiol. 2013;304:H1585–H1597. doi: 10.1152/ajpheart.00096.2013
102. Chen J, Hamm LL, Mohler ER, Hudaihed A, Arora R, Chen CS, Liu Y, Browne G, Mills KT, Kleinpeter MA u.c. Vairāku endotēlija disfunkcijas biomarķieru savstarpējā saistība ar hronisku nieru slimību. PLoS One. 2015;10:e0132047. doi: 10.1371/journal.pone.0132047
103. Mihai S, Codrici E, Popescu ID, Enciu AM, Albulescu L, Necula LG, Mambet C, Anton G, Tanase C. Ar iekaisumu saistīti mehānismi hroniskas nieru slimības prognozēšanā, progresēšanā un iznākumā. J Immunol Res. 2018;2018:2180373. doi: 10.1155/2018/2180373
104. Stenvinkel P, Keteler M, Johnson RJ, Lindholm B, Pecoits-Filho R, Riella M, Heimbürger O, Cederholm T, Girndt M. Il-10, IL-6 un TNF-alpha: galvenie faktori izmainītajā urēmijas citokīnu tīklā -- labs, slikts un neglīts. Kidney Int. 2005; 67:1216–1233. doi: 10.1111/j.{12}}.2005.00200.x
105. Gupta J, Mitra N, Kanetsky PA, Devaney J, Wing MR, Reilly M, Shah VO, Balakrishnan VS, Guzman NJ, Girndt M u.c. Saistība starp albuminūriju, nieru darbību un iekaisuma biomarķieru profilu CKD gadījumā CRIC. Clin J Am Soc Nephrol. 2012; 7:1938–1946. doi: 10.2215/CJN.03500412
106. Amdur RL, Feldman HI, Gupta J, Yang W, Kanetsky P, Shlipak M, Rahman M, Lash JP, Townsend RR, Ojo A u.c. Iekaisums un progresēšana CKD: CRIC pētījums. Clin J Am Soc Nephrol. 2016; 11:1546–1556. doi: 10.2215/CJN.13121215
107. Sun J, Axelsson J, Machowska A, Heimbürger O, Bárány P, Lindholm B, Lindström K, Stenvinkel P, Qureshi AR. Sirds un asinsvadu slimību biomarķieri un mirstības risks pacientiem ar progresējošu CKD. Clin J Am Soc Nephrol. 2016;11:1163–1172. doi: 10.2215/CJN.10441015
108. Jalal D, Chonchol M, Etgen T, Sander D. C-reaktīvais proteīns kā kardiovaskulāru notikumu prognozētājs gados vecākiem pacientiem ar hronisku nieru slimību. J Nefrols. 2012; 25:719–725. doi: 10.5301/Jn.5000047
109. Menon V, Greene T, Wang X, Pereira AA, Marcovina SM, Beck GJ, Kusek JW, Collins AJ, Levey AS, Sarnak MJ. C-reaktīvais proteīns un albumīns kā visu cēloņu un sirds un asinsvadu mirstības prognozētāji hroniskas nieru slimības gadījumā. Kidney Int. 2005; 68:766–772. doi: 10.1111/j.{9}}.2005.00455.x
110. Yilmaz MI, Solak Y, Saglam M, Cayci T, Acikel C, Unal HU, Eyileten T, Oguz Y, Sari S, Carrero JJ u.c. Saistība starp IL-10 līmeni un kardiovaskulāriem notikumiem pacientiem ar HNS. Clin J Am Soc Nephrol. 2014; 9:1207–1216. doi: 10.2215/CJN.08660813
111. Ridker PM, MacFadyen JG, Glynn RJ, Koenig W, Libby P, Everett BM, Lefkowitz M, Thuren T, Cornel JH. Kanakinumaba izraisītā interleikīna-1b inhibīcija un kardiovaskulārie rezultāti pacientiem ar hronisku nieru slimību. J Am Coll Cardiol. 2018;71:2405–2414. doi 10.1016/j.jacc.2018.03.490
112. Ridker PM. No RESCUE līdz ZEUS: vai interleikīna-6 inhibīcija ar ziltivekimabu izrādīsies efektīva kardiovaskulāro notikumu mazināšanai? Cardiovasc Res. 2021;117:e138–e140. doi: 10.1093/cvr/cvab231
113. Hung MJ, Cherng WJ, Hung MY, Wu HT, Pang JHS. Interleikīns-6 inhibē endotēlija slāpekļa oksīda sintāzes aktivāciju un palielina endotēlija slāpekļa oksīda sintāzes saistīšanos ar stabilizētu kaveolīnu-1 cilvēka asinsvadu endotēlija šūnās. J Hipertensija. 2010;28:940–951. doi: 10.1097/HJH.0b013e32833992ef
114. Venugopal SK, Devaraj S, Yuhanna I, Shaul P, Jialal I. Demonstrācija, ka C-reaktīvais proteīns samazina eNOS ekspresiju un bioaktivitāti cilvēka aortas endotēlija šūnās. Aprite. 2002;106:1439–1441. doi 10.1161/01.cir.0000033116.22237.f9
115. Yang YC, Fu H, Zhang B, Wu YB. Interleikīns-6 samazina asinsvadu endotēlija kadherīna ekspresiju un palielina caurlaidību nieru glomerulārās endotēlija šūnās, izmantojot transsignalizācijas ceļu. Iekaisums. 2022;45:2544–2558. doi: 10,1007/s10753-022-01711-3
116. Alsaffar H, Martino N, Garrett JP, Adam AP. Interleikīns-6 veicina ilgstošu endotēlija barjeras funkcijas zudumu, izmantojot Janus kināzes mediētu STAT3 fosforilāciju un de novo proteīnu sintēzi. Am J Physiol Cell Physiol. 2018;314:C589–C602. doi: 10.1152/ajpcell.00235.2017
117. Huang Y, Yan L, Rong S, Haller H, Kirch T. TNF-a izraisa endotēlija disfunkciju, izmantojot PKC-z atkarīgu NADPH oksidāzes aktivāciju. J Huazhong Univ Sci Technolog Med Sci. 2012; 32:642–647. doi: 10,1007/s{10}}
118. Csiszar A, Ungvari Z, Koller A, Edwards JG, Kaley G. Proinflammatoriskais fenotips koronāro artēriju veicina endotēlija apoptozi novecošanā. Fizioloģiskā genomika. 2004;17:21–30. doi: 10.1152/physiolgenomics.00136.2003
119. Rosin DL, Okusa MD. Bīstamība: DAMP reakcija uz bojājumiem un šūnu nāvi nieru slimību gadījumā. J Am Soc Nephrol. 2011;22:416–425. doi: 10.1681/ASN.2010040430
120. Hara M, Ando M, Morito T, Nokiba H, Iwasa Y, Tsuchiya K, Nitta K. S100A12 gēna ekspresija ir palielināta perifērajos leikocītos hroniskas nieru slimības stadijā 4-5 pacientiem ar sirds un asinsvadu slimībām. Nephron Clin prakse. 2013;123:202–208. doi: 10.1159/000353808
121. Folco EJ, Mawson T, Vromman A, Bernardes-Souza B, Franck G, Persson O, Nakamura M, Newton G, Luscinskas FW, Libby P. Neitrofilu ekstracelulārie slazdi inducē endotēlija šūnu aktivāciju un audu faktoru veidošanos, izmantojot interleikīnu{2 }}a un katepsīns G. Arterioscler Thromb Vasc Biol. 2018;38:1901–1912. doi: 10.1161/ATVBAHA.118.311150
Konstance CFMJ Bātena, Sonja Vondenhofa, Heidija Noelsa






