Kinurenīna ceļš — jauna saikne starp iedzimto un adaptīvo imunitāti autoimūnās endokrinopātijās, 1. daļa
Jul 07, 2023
Anotācija:
Kinurenīna ceļš (KP) ir ļoti regulēts imūnsistēmā, kur tas veicina imūnsupresiju, reaģējot uz infekciju vai iekaisumu. Indoleamīnam 2,3-dioksigenāzei 1 (IDO1), galvenajam KP enzīmam, ir plašs darbības spektrs imūnšūnu regulēšanā, kontrolējot līdzsvaru starp stimulāciju un imūnsistēmas nomākšanu lokāla iekaisuma vietās, kas ir svarīgas plašs autoimūnu un iekaisuma slimību klāsts. Līdz šim ir identificētas dažādas autoimūnas slimības, tostarp endokrinopātijas, taču, neskatoties uz ievērojamo progresu to diagnostikā un ārstēšanā, tās joprojām ir saistītas ar ievērojamām komplikācijām, saslimstību un mirstību. Precīzi šūnu un molekulārie mehānismi, kas izraisa autoimūno slimību rašanos un attīstību, līdz šim joprojām ir slikti noskaidroti. Pārkāpjot toleranci, iedzimtās imunitātes šūnas nodrošina izšķirošu mikrovidi, kas regulē imūno šūnu diferenciāciju, izraisot adaptīvās imunitātes aktivizēšanos. Pašreizējais pārskats sniedza visaptverošu prezentāciju par zināmo IDO1 un KP aktivācijas lomu imūnsistēmas iedzimto un adaptīvo roku regulēšanā. Ievērojama uzmanība ir pievērsta IDO1 imūnregulējošajai lomai visizplatītākajās orgānu specifiskajās autoimūnajās endokrinopātijās — 1. tipa cukura diabēta (T1DM) un autoimūna tiroidīta gadījumā.
Kinurenīna ceļš ir svarīgs bioķīmisks ceļš, kas ir cieši saistīts ar suņu imunitāti. Jaunākie pētījumi liecina, ka kinurenīna ceļš var uzlabot suņu imunitāti un uzlabot suņu izturību pret slimībām, izmantojot dažādus mehānismus.
Pirmkārt, kinurenīna ceļš var veicināt T šūnu proliferāciju un aktivāciju suņiem, tādējādi uzlabojot šūnu imūnreakciju suņiem. Šī reakcija tiek panākta, T šūnām tieši uzbrūkot un iznīcinot patogēnos mikroorganismus, tāpēc to loma ir ļoti svarīga. Turklāt kinurenīna ceļš var arī veicināt suņu dabisko imūno funkciju, tas ir, pretoties patogēniem mikroorganismiem, izmantojot mehānismus, kuriem nav nepieciešama T-šūnu līdzdalība. Šis dabiskais imūnmehānisms var ātri reaģēt, kad suns ir pakļauts patogēniem mikroorganismiem, tādējādi novēršot slimību rašanos.
Turklāt kinurenīna ceļš var arī veicināt brūču dzīšanu un audu atjaunošanos suņiem, tādējādi atjaunojot bojāto audu normālu darbību. Šis efekts ir cieši saistīts arī ar suņu imunitāti, jo tikai tad, kad viņu ķermenis ir labā stāvoklī, tie var efektīvi cīnīties pret patogēniem mikroorganismiem.
Visbeidzot, kinurenīna ceļš var uzlabot suņu imunitāti, izmantojot dažādus mehānismus, tādējādi uzlabojot suņu izturību pret slimībām. Tāpēc mums ir aktīvi jāveicina normāla kinurenīna ceļa darbība, lai uzturētu normālu suņa imūnsistēmas stāvokli. Vienlaikus jāpievērš uzmanība arī suņu veselībai, uzturam un drošībai, lai labāk uzlabotu viņu imunitāti un novērstu dažādu slimību rašanos. Tas liecina, ka mums ir jāuzlabo imunitāte. Cistanche var ievērojami uzlabot mūsu imunitāti. Tā kā gaļā esošie polisaharīdi var regulēt cilvēka imūnsistēmas imūnreakciju, uzlabot imūnsistēmu stresa spēju un pastiprināt imūnšūnu baktericīdo iedarbību.

Noklikšķiniet uz cistanche deserticola papildinājuma
Atslēgvārdi:
indoleamīns 2, 3-dioksigenāze 1 (IDO1); kinurenīna ceļš (KP); iedzimta imunitāte; adaptīvā imunitāte; autoimūna slimība; autoimūnas endokrinopātijas; 1. tipa cukura diabēts (T1DM); autoimūns tiroidīts.
1. Ievads
Epidemioloģiskie pētījumi liecina, ka 3–5 procenti iedzīvotāju cieš no autoimūnām slimībām, ar katru gadu pieaugot. Autoimūno slimību patofizioloģija parasti rodas paštolerances zuduma rezultātā, kas izraisa autoantivielu un pašreaktīvu limfocītu veidošanos, kas izraisa audu iznīcināšanu. Līdz šim ir aprakstītas aptuveni 80 dažādas autoimūnas slimības — vairākām no tām ir raksturīga orgānu specifiska imūnsistēmas disfunkcija (piemēram, Hašimoto slimība (HD), 1. tipa cukura diabēts (T1DM)), bet pārējās ir sistēmiskas imūnās disfunkcijas, kas saistītas ar vairākiem. orgāni, piemēram, sistēmiskā sarkanā vilkēde, multiplā skleroze un citi [1,2].
Gandrīz puse no diagnosticētajām autoimūnām slimībām ir autoimūnas endokrinopātijas, no kurām biežākās ir vairogdziedzera slimības, T1DM, celiakija un vitiligo. Autoimūna procesa sekas parasti ir endokrīno dziedzeru mazspēja; tomēr vienīgais zināmais izņēmums ir Greivsa slimība (GD), kurā vairogdziedzeris netiek iznīcināts, tomēr kļūst pārāk aktīvs specifisku antivielu klātbūtnes dēļ. Autoimūnas endokrinopātijas var pastāvēt līdzās tiem pašiem indivīdiem. Turklāt bieži tiek novērota tā sastopamība ģimenē. Patofizioloģija izriet no sarežģītas ģenētiskās noslieces un vides/endogēno faktoru mijiedarbības. Orgānu specifisko autoantivielu noteikšanai un atbilstošam hormonu novērtēšanai ir izšķiroša nozīme diagnostikas procesā un ārstēšanas stratēģijā [3].
HD ir autoimūns tireoidīts, kam raksturīga vairogdziedzera folikulu šūnu atrofija, limfocītu infiltrācija iekaisušajā orgānā un progresējoša fibroze [4]. Sākotnējā HD stadija var būt asimptomātiska, savukārt dažiem pacientiem būs tikai antivielas pret tiroglobulīnu (anti-Tg). Anti-vairogdziedzera peroksidāzes antivielu (anti-TPO) parādīšanās tiek uzskatīta par prognozējošu faktoru, kas norāda uz subklīniskas hipotireozes pāreju uz atklātu hipotireozi, ko novēro aptuveni 20–30 procentiem pacientu ar autoimūnu tireoidītu [5].
GD ir visizplatītākais hipertireozes cēlonis apgabalos, kuros ir pietiekami daudz joda. Autoantivielu veidošanās pret TSH receptoru (TRAb) liecina par slimības progresēšanu; tomēr faktori, kas nosaka slimības ierosināšanu, līdz šim nav zināmi [6]. GD ietekmē vairuma sistēmu darbību cilvēka organismā un parasti izraisa hipertireozes, asinsvadu goitera, Graves orbitopātijas (25 procenti gadījumu), vairogdziedzera dermatopātijas (apmēram 4 procenti gadījumu) klīnisko simptomu attīstību; tādēļ ar GD saistītās pazīmes un simptomi var stipri atšķirties un būtiski ietekmēt vispārējo labsajūtu [7,8].
T1DM raksturo novirzes imūnās atbildes reakcijas pret specifiskiem šūnu autoantigēniem, kā rezultātā rodas insulīna deficīts un hiperglikēmija, kas attīstās ģenētiskās jutības un vides faktoru mijiedarbības rezultātā. Lai gan T1DM etioloģija nav pilnībā izprotama, tiek uzskatīts, ka slimības patoģenēze ietver -šūnu autoimunoloģisku iznīcināšanu [9]. Vislielākais T1DM diagnozes biežums tiek novērots bērnībā un pusaudža gados [10], tomēr simptomi var attīstīties visa mūža garumā.
Apmēram 90 procentos nesen diagnosticētu T1DM gadījumu ir nosakāmas antivielas pret specifiskiem šūnu proteīniem, piemēram, insulīnu, insulinomas antigēnu 2, glutamāta dekarboksilāzi, tetraspanīnu-7 vai cinka transportētāju 8 [11]. Tomēr lielākā daļa cilvēku ar vienu autoantivielu neprogresē uz T1DM. Divu vai vairāku seruma autoantivielu klātbūtne bērniem ir saistīta ar 84% klīniskās T1DM risku līdz 18 gadu vecumam [12]. Pamatojoties uz šiem novērojumiem, T1DM patoģenēze tika sadalīta trīs posmos: 1. stadija (presimptomātiska) tiek definēta kā divu vai vairāku autoantivielu klātbūtne ar normoglikēmiju, 2. stadija (presimptomātiska) kā šūnu autoimunitātes klātbūtne ar patoloģisku glikēmiju un 3. stadija kā simptomātiskas slimības sākums [13]. Norādītās T1DM patogēnās stadijas ļauj prognozēt slimības progresēšanu riska grupām un nodrošina pamatu profilaktiskās terapijas pētniecībai un attīstībai.
Dažas paralēli sastopamas autoimūnas slimības var veidoties specifiskos sindromos, ko sauc par autoimūno poliendokrīno sindromu (APS), ko var definēt kā divu vai vairāku dziedzeru funkcionālus traucējumus. 1. tipa APS raksturo Addisona slimība, kas pastāv vienlaikus ar gļotādas kandidozi un autoimūnu hipoparatireozi; tomēr tas var izpausties arī ar T1DM, GD, hipogonādismu, vitiligo vai kaitīgu anēmiju. 2. tipa APS var izpausties ar Addisona slimību, autoimūnu tireoidītu, T1DM, hipogonādismu, vitiligo, myasthenia gravis un alopēciju. 3A tipa APS ir saistīta ar T1DM un autoimūnu tireoidītu, tomēr arī ar augšanas hormona deficītu un citām novirzēm, savukārt APS 3C tipa gadījumā T1DM ir saistīta ar psoriāzi un celiakiju [14–16].
Autoimūnā Addisona slimība (AAD) ir pazīstama kā APS1 un APS2 dominējošā sastāvdaļa. Turklāt AAD ir galvenais primārās virsnieru mazspējas cēlonis, kas tiek diagnosticēts ar zemu bazālo kortizola līmeni serumā, augstu adrenokortikotropā hormona (AKTH) koncentrāciju plazmā un traucētu kortizola sekrēciju pēc AKTH stimulācijas testa. Vēl viens būtisks diagnozes nosacījums ir autoantivielu klātbūtne pret 21- hidroksilāzi (21-OHAbs); tomēr virsnieru garozas autoantivielas var tikt konstatētas arī 40–80 procentiem pacientu ar ADD. Sakarā ar destruktīvu autoimūnu procesu, kas izraisa pilnīgu kortizola sekrēcijas deficītu, AAD pacientiem nepieciešama mūža hidrokortizona aizstājterapija [17].
Visām autoimūnām slimībām ir kopīga patoģenēze, kas ietver imūnsistēmas izraisītu uzbrukumu, kas izraisa ķermeņa orgānu iznīcināšanu. Jāpiemin, ka šajā procesā ir iesaistīta iedzimtā un adaptīvā imūnsistēma, ko var apstiprināt imunoloģiskos, ģenētiskos un histopatoloģiskajos pētījumos [18–24]. Triptofāna metabolisma kinurenīna ceļš (KP) ir endogēna sistēma ar imūnsupresīvām iezīmēm, kas ir iesaistīta iekaisuma kontrolē un ilgstošas imūnās tolerances izraisīšanā dažādos orgānos visā organismā [25–27]. Šajā pārskatā mēs koncentrējamies uz indoleamīna 2, 3-dioksigenāzes-1 (IDO1) un triptofāna katabolītu — kinurenīnu — ieguldījumu, lai regulētu mijiedarbību starp iedzimtas un adaptīvās imūnsistēmas komponentiem. Īpaša uzmanība tika pievērsta IDO1 un KP metabolītu lomai autoimūno endokrinopātiju rašanās un progresēšanas procesā.

2. Kinurenine ceļš
Pēdējo divu desmitgažu laikā ir parādījusies teorija, ka TRP metabolisms caur KP ir iesaistīts imūnreakciju kontrolē, lai kontrolētu autoimunitāti [28–30]. TRP ir būtiska aminoskābe, kas ir būtiska proteīnu sintēzei un vairāku bioaktīvu savienojumu ar svarīgām fizioloģiskām funkcijām, tostarp serotonīna, triptamīna, indolu, kinurenīnu un nikotīnamīda adenīna dinukleotīda (NAD plus) ģenerēšanai [31]. Cilvēkiem trūkst bioķīmisko ceļu, lai sintezētu TRP, kas jāsavāc no uztura. Pēc TRP uzsūkšanās caur enterocītiem zarnās tas ar aknu vārtu sistēmu tiek transportēts aknās, kur tiek izmantots proteīnu sintēzei (mazāk nekā 1 procents no uzņemtā TRP), savukārt aptuveni 95 procenti ar uzturu iegūtā TRP tiek metabolizēti caur KP aknās. Atlikušais TRP tiek izdalīts asinsritē, un to var izmantot perifēro audu šūnas, piemēram, asinsvadu endotēlija šūnas, fibroblasti un iedzimtas imunitātes šūnas [32]. Turklāt TRP var arī transportēt cauri asins-smadzeņu barjerai, lai regulētu smadzeņu serotonīna sintēzi [33].
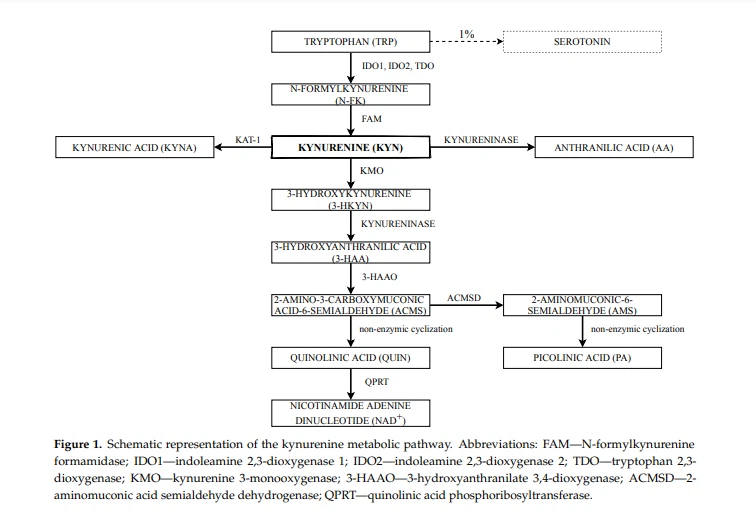
Kinurenīna ceļš ir galvenais TRP metabolisma veids [34]. Galvenie KP enzīmi un substrāti ir shematiski parādīti 1. attēlā. Vispirms TRP ir jāpārvērš N-formilkinurenīnā, ko mediē indoleamīns 2, 3-dioksigenāze (IDO) un triptofāns 2, 3-dioksigenāze (TDO), un pēc tam kinurenīnā (KYN), izmantojot Nformilkinurenīna formamidāzi (FAM) [35]. Pirmo soli TRP degradācijā normālos apstākļos veic TDO, kas ir galvenais TRP ekstrahepatiskās pieejamības noteicošais faktors un ko inducē pats TRP, estrogēni un glikokortikoīdi. Tomēr ar augstu kortizola koncentrāciju un iekaisuma stāvokli TDO ekspresija aknās tiek nomākta, savukārt IDO1 ekspresija tiek inducēta imūnsistēmas šūnās kā daļa no negatīvās atgriezeniskās saites cilpas, kuras mērķis ir kontrolēt iekaisuma reakcijas [36].
Ekstrahepatiskā KP paliek divu atšķirīgu IDO enzīmu kontrolē: IDO1 un IDO2, kuru aktivitātes var atšķirties viena no otras. IDO1 aktivitātei bazālos apstākļos nav nozīmes, bet to spēcīgi inducē vairāki iekaisuma stimuli, piemēram, interferons (IFN-), lipopolisaharīds (LPS), audzēja nekrozes faktors (TNF-), proinflammatori interleikīni (IL), infekcija un transformācija. augšanas faktors (TGF ) [37,38]. IDO1 galvenokārt darbojas imūnsistēmas šūnās, gļotādas audos un dažos audzējos; tomēr to var kavēt paaugstināts TRP līmenis. Pretiekaisuma citokīni IL-4 un IL-13 izraisa IDO1 mRNS ekspresijas samazināšanos un TRP katabolisma samazināšanos [39], lai gan dati par IL{15 lomu ir pretrunīgi. }} ir ziņots arī [40]. IDO2 fermentatīvā aktivitāte ir aptuveni 500–1000-reižu zemāka nekā zīdītāju IDO1, un IDO2 galvenokārt izpaužas aknās, epididīmā un nierēs [41]. Pašreizējie pētījumi parādīja daudzveidīgu un galveno IDO1 lomu imūnregulācijā infekcijas, grūtniecības, autoimūnu slimību un dažādas izcelsmes neoplāzijas laikā [26, 28, 42, 43].
TDO tiek uzskatīts par "augstāku katalītiskās aktivitātes" enzīmu salīdzinājumā ar IDO1 [32]; tomēr IDO1 ir plašāka substrāta specifika nekā TDO. Galvenie TDO avoti cilvēka organismā ir aknas un centrālā nervu sistēma [44], tomēr tas ir identificēts arī gļotādās, epididīmā un smadzenēs [45].
KYN un tā metabolīti ir bioloģiski aktīvi. Līdz ar to to ražošana ir stingri jākontrolē. KYN ir KP centrālais starpprodukts, kur vielmaiņas ceļš ir sadalīts divās dažādās nozarēs. KYN kinurenīna 3-monooksigenāze (KMO) var pārveidot par 3-hidroksikinurenīnu (3-HKYN), kas ir pazīstams kā viens no toksiskajiem metabolītiem. Cilvēka KMO ir proteīns, kura katalītiskajai darbībai nepieciešams nikotīnamīda adenīna dinukleotīda fosfāts (NADPH) [46]. Rezultātā kinurenināze var pārvērst 3-HKYN par 3-hidroksiantranilskābi (3-HAA). Tomēr kinurenināze var arī tieši pārvērst kinurenīnu antranilskābē (AA) [47]. Parasti pēdējais KP solis ir 3-HAA pārvēršana hinolīnskābē (QUIN) ar 3- hidroksiantranilāta 3,4-dioksigenāzi (3-HAAO) caur šīs reakcijas nestabilais produkts — 2-amino-3-karboksimukonāts-6-semialdehīds (ACMS) —, kas tālāk tiek pakļauts neenzīmu ciklizācijai, iegūstot QUIN. Pikolīnskābi (PA) veido arī aminomukonskābes semialdehīda (AMS) neenzīmu ciklizācija. Tomēr PA veidošanās ir atkarīga no enzīma 2- aminomukonskābes semialdehīda dehidrogenāzes (ACMSD) substrāta piesātinājuma pakāpes [35]. Visbeidzot, QUIN tiek pārstrādāts galaproduktā NAD plus ar hinolīnskābes fosforiboziltransferāzi (QPRT) [48].
Tomēr ir zināma arī cita KP atzara — parastos apstākļos tas ir mazsvarīgs, savukārt TRP vai KYN pārpilnības laikā palielinās, un satur KYN pārvēršanos par kinurēnskābi (KYNA), kas arī tiek atzīta par N-metilD endogēnu antagonistu. -aspartāta (NMDA) receptori. Iepriekš minēto soli katalizē kinurenīna aminotransferāze 1 (KAT-1) [48,49].
3. IDO1 un KP metabolītu loma imūnsistēmas regulēšanā
3.1. Iedzimtā un adaptīvā imunitāte
Imūnsistēma nepārtraukti uztur izsmalcinātu līdzsvaru starp iebrukušajiem patogēniem un toleranci pret nekaitīgiem antigēniem un pašantigēniem. Kopumā imūnsistēmu veido iedzimta un adaptīva imunitāte, no kurām katra ir atbildīga par atšķirīgu kapacitāti un veido dažādus šūnu un ne-šūnu komponentus [50]. Iedzimta imunitāte ir pirmā aizsardzības līnija un nodrošina sākotnējo akūtu iekaisuma reakciju pret audu bojājumiem, svešiem antigēniem vai patogēniem [51]. Iedzimtā imunitāte zināmā mērā ir nespecifiska un ir sadalīta šūnu un ne-šūnu sistēmās. Iedzimtās sistēmas šūnu komponenti ir monocīti/makrofāgi, dendrītiskās šūnas (DC), dabiskās slepkavas (NK) šūnas, eozinofīli un neitrofīli. Nešūnu sistēma ir ārkārtīgi daudzveidīga — tā ar dažādu citokīnu palīdzību piesaista imūnās šūnas traumas/infekcijas vietai, veicina fagocitozi un aktivizē komplementa kaskādi un adaptīvo imūnsistēmu [51,52].
Adaptīvās imūnsistēmas aktivizēšana izraisa antigēnam specifisku saimniekorganisma reakciju, ko mediē T un B šūnas. B šūnas izdala antigēnam specifiskas antivielas, lai neitralizētu patogēnus, veicinātu alerģiskas reakcijas un autoimunitāti, kā arī radītu imūnās atmiņas šūnas. T šūnas ir iesaistītas citokīnu ražošanā, tiešā citotoksiskā iedarbībā pret inficētiem audiem un citu imūno šūnu aktivizēšanā [50]. Šūnu šķērsruna ir adaptīvās imunitātes pazīme. Pirms naivu B šūnu proliferācijas un diferenciācijas, reaģējot uz lielāko daļu antigēnu, ir jāveic stimulācija ar T šūnām, kas ir specifiskas tiem pašiem antigēniem. Tāpat T šūnām, lai vairotos, reaģējot uz antigēniem, ir nepieciešami papildu signāli, ko nodrošina B šūnas [50]. Tādējādi iedzimtā un adaptīvā imunitāte darbojas kopā, lai izveidotu un uzturētu audu homeostāzi. Jebkāda veida regulēšanas traucējumi var traucēt regulāru imūnreakciju un izraisīt hroniska iekaisuma noturību vai pat izraisīt autoimūnas reakcijas uzņēmīgākiem indivīdiem.
3.2. Kinurenīni imūnregulācijā — "TRP izsīkuma teorija" pret "TRP izmantošanas teoriju"
Pēdējā laikā KP loma gan iedzimto, gan adaptīvo imūnreakciju regulēšanā nerada šaubas, lai gan tā joprojām nav pilnībā izskaidrota. Agrāk pastāvēja divas pretējas teorijas, atsaucoties uz TRP metabolisma nozīmi, izmantojot KP, imūnregulācijā. Pirmajā "izsīkšanas teorijā" tika pieņemts, ka TRP samazināšanās ir ar imūnsistēmu saistītās IDO1 indukcijas primārā funkcija, kas ir atzīta par iedzimtu imūnreakciju saimnieka aizsardzības mehānismu. Pfeferkorns parādīja, ka Toxoplasma gondii augšanu var kavēt IFN- -mediēta IDO1 indukcija, kas bija saistīta ar TRP koncentrācijas samazināšanos [53]. Citos in vitro pētījumos TRP koncentrācijas papildināšana barotnē atjaunoja vēža šūnu, baktēriju un parazītu augšanu, atbalstot TRP samazināšanās teoriju [54].
Šī teorija mainījās, kad Munn et al. [55] atklāja, ka IDO1 aktivitāte ir nepieciešama, lai novērstu T šūnu izraisītu alogēnu augļu atgrūšanu grūsnām pelēm. Viņi arī atklāja, ka T šūnu proliferāciju var kavēt in vitro, stimulējot kopā kultivētus monocītus ar IFN-, kas izraisīja IDO{4}}mediētu TRP samazināšanos no barotnes. Vēlākais pētījums par Lee et al. [56] parādīja, ka T šūnas, kas aktivizētas bez TRP, iekļuva šūnu ciklā; tomēr šūnu cikla progresēšana tiek apturēta G1 fāzē, un T šūnas kļuva jutīgas pret nāvi, izmantojot apoptozi, daļēji ar Fas starpniecību. Turklāt samazināta TRP pieejamība ir saistīta ar vispārējās kontroles nenomācošo 2 kināžu (GCN2K) ceļa aktivizēšanu, rapamicīna (mTOR) mērķa zīdītāju inhibīciju un proteīnkināzes C signālu pārraidi, kas izraisa T šūnu autofagiju un enerģiju. 57]. Saskaņā ar pašreizējo konceptualizāciju TRP samazināšanās darbojas, lai ierobežotu specifisku saimniekšūnu proliferāciju, kas kļuva jutīgākas pret apoptotiskiem stimuliem [56].
TRP samazināšanās hipotēze izskaidro tikai IDO1 aktivāciju, savukārt imūnās atbildes laikā daudzos audos tiek ģenerēti gan KYN, gan citi KYN metabolīti: 3-HKYN, 3-HAA, PA KYNA un QUIN [43] ]. Tika pierādīts, ka šie metabolīti spēcīgi kavē T šūnu proliferāciju, inducējot T šūnu apoptozi.

Pētījums ar sirds transplantācijas modeli žurkām apstiprināja šos rezultātus in vivo [58], veidojot pamatu tā sauktajai "TRP izmantošanas teorijai" [59]. Norādītajā teorijā tika pieņemts, ka IDO1 imūnmodulējošās īpašības ir saistītas ar KYN metabolītu uzkrāšanos kopā ar TRP samazināšanos [32].
3.3. IDO1 imūnregulējošā darbība
IDO1 tiek plaši ekspresēts dažādās šūnās, kas pieder imūnsistēmai, piemēram, makrofāgos, monocītos, DC, eozinofīlos, neitrofilos, dažās T šūnu apakšgrupās un regulējošās B šūnās [60–65]. IDO1 ekspresijas un aktivitātes indukcija profesionālās antigēnu prezentējošās šūnās (APC), piemēram, DC un monocītu atvasinātos makrofāgos, kā arī citos iedzimtas imūnsistēmas komponentos — NK šūnās, eozinofīlos un neitrofīlos ir daudzvirzienu ietekme uz šo šūnu funkcija imūnsistēmā (2. attēls).

3.3.1. IDO1 un DC
Dendrītiskās šūnas ir profesionāli APC un galvenie imūnsistēmas regulatori. DC veic daudzas funkcijas imūnsistēmā, ieskaitot antigēnu uzņemšanu, apstrādi un prezentēšanu naivām T šūnām, efektoru T šūnu un NK šūnu aktivizēšanu, kā arī citokīnu un citu imūnmodulējošu molekulu sekrēciju, lai veidotu T un B šūnu atbildes reakcijas. . Ir aprakstītas divas galvenās cilvēka perifēro asiņu DC apakškopas: parastie DC (cDC) un plazmacitoīdie DC (pDC) [66]. pDC ir unikāla šūnu populācija, kas apvieno iedzimtās un adaptīvās imūnās atbildes, lai aizsargātos pret patogēniem, autoimunitāti un vēzi [67]. pDC izdala lielu daudzumu I un III tipa interferonu un var izdalīt IL-6, IL-12, IL-23, TNF- un interferonu inducējamo proteīnu 10 (IP-10). ). Tie izsaka arī galveno II klases histokompatibilitātes kompleksu (MHC-II), MHC-I un kostimulējošās molekulas (CD40, CD80, CD86) antigēnu prezentācijai [67, 68]. Iepriekš minēto molekulu ražošana ļauj pDC veidot imūnās atbildes veidu.
Piemēram, IL-12 var izraisīt Th1 reakciju un CD8 plus T-šūnu un NK-šūnu aktivāciju, kas ir svarīgas vīrusu un intracelulāro patogēnu infekciju apkarošanai, savukārt IL-6 un IL{{6} } var virzīt imūno aktivitāti uz Th17 reakciju, kam ir svarīga loma neitrofilu un makrofāgu piesaistē, imūnās atbildes reakcijās pret sēnīšu infekcijām un autoimūnām slimībām [69]. pDC var veikt arī tiešas efektora funkcijas. Tie var ekspresēt ar TNF saistīto apoptozi inducējošo ligandu (TRAIL), kas izraisa pret TRAIL jutīgu šūnu nāvi [70]. Turklāt pDC var iznīcināt mērķa šūnas, atbrīvojot serīna proteāzes granzīmu B [71]. Nesen tika ierosināta pDC loma autoimūnās slimībās. pDC var tieši iedarboties uz autoreaktīvo B šūnu diferenciāciju/uzturēšanu un veicināt autoreaktivitāti netieši caur T šūnām vai citiem šūnu veidiem [72]. No otras puses, traucēta pDC aktivitāte ir saistīta ar imūndeficīta stāvokļiem vai neefektīvām imūnreakcijām [73].
Lai gan DC ir būtiska loma iekaisuma reakciju ierosināšanā, tie spēj arī izraisīt imūntoleranci, cita starpā, paaugstinot intracelulārā enzīma IDO1 regulēšanu. Šīs šūnas ekspresē gan konstitutīvus, gan IFN- -inducējamus fermenta veidus [74,75]. Jo īpaši ir pierādīts, ka pDC spēj radīt lielu daudzumu IDO1 [60]. Neskatoties uz to, pDC ir aprakstīti kā diezgan vāji to antigēnu prezentēšanas funkcijā salīdzinājumā ar cDC [76]. IFN viens pats var izraisīt IDO1 ziņojuma augšupregulāciju DC; tomēr papildu stimuls, piemēram, CD40L vai LPS, rada ievērojami augstāku IDO1 ekspresiju [75]. Arilogļūdeņraža receptoru (AhR) aktivācija DC ir šāds svarīgs faktors IDO1 ekspresijai šajās šūnās. Ir konstatēts, ka KYN un citi KP metabolīti — 3-HKYN un KYNA — ir AhR endogēni ligandi, un šis mehānisms var noteikt tolerogēnu DC fenotipu, kas veicina Trega paplašināšanos [77,78].
Šķiet, ka IDO1 ekspresija pDC drīzāk var modulēt efektoršūnu imūnreakciju, jo IDO1- ekspresējošo pDC izsīkšana izraisīja pastiprinātu T šūnu proliferāciju un iekaisuma pastiprināšanos [79]. Iepriekš minētais atklājums tika apstiprināts daudzos pētījumos, kuros IDO1-izpaušanas DC darbojas kā daļa no "atgriezeniskās saites" procesa, lai ierobežotu hronisku vai pārmērīgu imūnsistēmas aktivāciju. DC, kas ražo IDO1, var nomākt efektoru T šūnu proliferāciju un var izraisīt T šūnu apoptozi [75, 80]. IDO1- ekspresējošie pDC veicina receptoru zeta ķēdes pazemināšanos T šūnās un veicina forkhead box P3 plus (Foxp3 plus ) T regulējošo šūnu (Tregs) paplašināšanos [81]. IDO1 ekspresija DC var arī novirzīt CD4 un T-helpera šūnas no proinflammatoriskā fenotipa Th1 vai Th17 līdz tolerogēniem Tregs [82]. Tādējādi IDO1 ekspresija ar DC ir saistīta ar perifēro toleranci un imūnsupresijas indukciju.
Ir pierādīts, ka vairākas molekulas, kas izraisa imūnsupresiju/toleranci, veicina to aktivitāti, izmantojot IDO1. B7 molekulu ligēšana uz DC ar citotoksisko T-limfocītu antigēnu 4 (CTLA-4), koinhibējošo molekulu, kas ekspresēta uz Tregs, var izraisīt IDO1 ekspresiju DC [83,84]. Mijiedarbība starp ieprogrammētajiem nāves 1 (PD-1) receptoriem uz T šūnām un to ligandiem uz DC var arī veicināt IDO1 augšupregulāciju [85]. Turklāt imūnsupresīvais TGF- var izraisīt un uzturēt IDO1 ekspresiju pDC [86]. Tāpat arī citas molekulas, piemēram, LPS vai INF-, kas var izraisīt AhR ekspresiju DC, var arī uzturēt IDO1 augstā līmenī, izmantojot šo pozitīvo mehānismu [77, 87].
IDO1 piemīt spēja kontrolēt DC nobriešanu, migrāciju un imūnregulācijas īpašības. DC pastāv perifērijā kā nenobriedušas šūnas, kas ir atbildīgas par antigēnu uztveršanu naivu T šūnu sagatavošanai. Pēc nobriešanas DC migrē uz drenējošajiem limfoīdajiem orgāniem, kur tie var izraisīt imunitāti. Ir pierādīts, ka IDO1 ekspresija un aktivitāte palielinājās DC nobriešanas laikā, kas bija saistīts ar fenotipiskām un funkcionālām izmaiņām, kas ir būtiskas MHC / peptīdu kompleksu ģenerēšanai un T šūnu gruntēšanai [88].
Turpretim IDO1 deficīts izraisīja samazinātu DC fenotipisko un funkcionālo nobriešanu in vitro un in vivo [89]. Tomēr Bracho-Sanchez et al. [90] parādīja, ka DC, kas apstrādāti ar cilvēka eksogēnu rekombinanto IDO, saglabā nenobriedušu fenotipu, neietekmējot to dzīvotspēju, un nodrošina antigēnu specifisko T šūnu proliferācijas nomākšanu in vitro. Turklāt IL-12p70 ražošana DC tika ievērojami samazināta, bet IL-10 saglabājās, kas liecina, ka naivā Th šūnu diferenciācija var tikt novirzīta uz imūnsupresīvu Th2 vai Tregs. Šie rezultāti liecina, ka DC kondicionēšanu izraisīja IDO1 fermentatīvā darbība un ka DC izraisītā T šūnu nomākšana bija atkarīga gan no TRP dzēšanas, gan no kinurenīnu klātbūtnes, kas kopā bija efektīvāki T šūnu stimulācijas atcelšanā.
3.3.2. IDO1 un monocīti/makrofāgi
Monocītiem un makrofāgiem ir plašas iekaisuma, imūnmodulējošas un audus atjaunojošas īpašības. Tie pieder pie aizsardzības šūnu priekšējās līnijas un var aktivizēt imūnsistēmu, lai izraisītu imūnreakciju. Pirms polarizācijas makrofāgi pastāv kā nesaistīti (M0), kas pēc stimulācijas ar atbilstošiem citokīniem un mikrobu produktiem spēs izteikt specializētās funkcijas. Stimulēšana noved pie M0 šūnu polarizācijas 2 grupās: M1- un M2- tipa makrofāgos, kas tiek atzīti attiecīgi par klasiski un alternatīvi aktivizētiem makrofāgiem. M1 makrofāgus var inducēt granulocītu-makrofāgu koloniju stimulējošais faktors (GM-CSF), IFN- un LPS, savukārt M2-tipa makrofāgi var tikt polarizēti pēc imūnkompleksu iedarbības, IL-4 , IL-13, IL-10 un glikokortikoīdi [91].
Parasti M1 makrofāgi tiek uzskatīti par iekaisumu veicinošiem, un tie izdala IL-12 un TNF-, savukārt M2 makrofāgiem ir imūnmodulējošas, brūču labošanas un audu remodelēšanas funkcijas, un tie ražo IL-4 un IL-10 [ 92]. Makrofāgiem ir augsta funkcionālās plastiskuma pakāpe: tie var viegli pārslēgties no M1 tipa uz M2 un otrādi, atkarībā no citokīniem, kas atrodas to vidē [93]. Tomēr dažu autoimūnu slimību gadījumā vienlaikus tika novēroti gan M1, gan M2 makrofāgi, kā arī to producētie citokīni [92]. Turklāt dažās slimībās tika konstatētas makrofāgu starpformas, kas līdzās ekspresē gan M1-, gan M2-specifiskus marķierus [94]. Šie atklājumi norādīja, ka makrofāgu polarizācija ir dinamisks un atgriezenisks process, kas ir atkarīgs ne tikai no vietējās vides, bet arī no slimības stadijas.
Makrofāgi un monocīti var ekspresēt IDO1, bet tikai pēc IFN stimulācijas [74]. IDO1 indukcija var mainīt makrofāgu fenotipu no pro-iekaisuma M1 uz tolerogēnu M2. Wang et al. [61] parādīja, ka IDO1 ekspresija M1-tipa makrofāgos, kas diferencēti no THP-1 šūnām, kas apstrādātas ar IFN-, bija ievērojami augstāka nekā M2-tipa, kas polarizējās no THP. -1 šūnas, kas kultivētas ar M-CSF. Viņi arī parādīja, ka IDO1 pārmērīga ekspresija veicina THP-1 šūnu diferenciāciju, ko plaši izmanto kā monocītu/makrofāgu diferenciācijas modeli, no M2-tipa makrofāgiem. Gluži pretēji, IDO1 klusums izraisa M1-tipa makrofāgu veidošanos [61].
IDO1 var kavēt makrofāgu piesaisti un fagocitozes procesu Aspergillus fumigatus keratīta peļu modeļos. Tomēr IDO1 var arī veicināt makrofāgu polarizāciju M1 fenotipā, aktivizējot mitogēnu aktivētu proteīnkināzes / ārpusšūnu signālu regulēto (MAPK / ERK) signālu ceļu, norādot, ka tas ir būtiski, lai saglabātu līdzsvaru starp pretiekaisuma un proinflammatorisko iedarbību. šajā modelī [95]. Makrofāgu daudzveidīgā loma iekaisuma reakcijās daļēji var būt saistīta ar AhR klātbūtni. Ir ziņots, ka makrofāgi ar AhR deficītu uzrādīja augstāku proinflammatorisko citokīnu līmeni pēc LPS stimulācijas un ka peles ar AhR deficītu bija jutīgākas pret LPS izraisītu letālu šoku nekā savvaļas tipa peles [96]. Nesen Suchard un kolēģi [97] apkopoja esošo literatūru un parādīja, ka paaugstināta IDO1 aktivitāte tiek uzskatīta par M2 makrofāgu aktivācijas pazīmi.
Iekaisuma stāvokli raksturo augsts šūnu stresa līmenis un enerģijas patēriņš, ko bieži pavada paaugstināts DNS bojājumu līmenis. Ir atzīmēts, ka TRP oksidēšana caur KP var rekonstruēt NAD plus līmeņus, lai apmierinātu enerģijas prasības un atbalstītu DNS remonta mehānismus makrofāgos, palielinot to dzīvotspēju [98].
3.3.3. IDO1 un NK šūnas
NK šūnas ir citotoksiski limfocīti, kuriem ir nozīmīga loma imūnās atbildes reakcijās pret eksogēniem patogēniem, kā arī aizsardzībā pret vēža šūnām. Cirkulējošās NK šūnas galvenokārt parādās miera fāzē; tomēr stress infekcijas vai ļaundabīgo audzēju rezultātā izraisa to aktivāciju un citotoksisku granulu jeb nāves receptoru ligandu sekrēciju [99]. NK šūnu aktivizēšanā svarīga loma ir aktivējošajiem un inhibējošiem receptoriem, kas atrodas uz to virsmas. Inhibējošie receptori sastāv no killer imūnglobulīniem līdzīgiem receptoriem (KIR), Ig līdzīgiem receptoriem (CD158), C tipa lektīna receptoriem (CD94-NKG2A) un leikocītu inhibējošiem receptoriem (LIR1, LAIR{8). }}). Svarīgi NK aktivējošie receptori ir NKG2D, DNAM1 un dabiskie citotoksiskie receptori: NKp46, NKp30, NKp44 un CD16 (FcgRIII), kas ir iesaistīti no antivielām atkarīgā citotoksicitātē. Pēc atbilstošo ligandu saistīšanas šie aktivizējošie un inhibējošie receptori sadarbojas un izlemj, vai NK šūnu citotoksicitāti ietekmēt mērķa šūnās [100]. NK šūnu tiešā citotoksiskā iedarbība galvenokārt ir saistīta ar diviem ceļiem: mērķa šūnas apoptozes indukciju, izdalot membrānu graujošus proteīnus un proteāzes, vai no kaspāzes atkarīgu apoptozi, iesaistot nāves receptorus (piemēram, Fas/CD95) uz mērķa šūnām. [99].
NK šūnas, kas ir viena no galvenajām iedzimtās imūnsistēmas sastāvdaļām, veido saikni starp iedzimto un adaptīvo imunitāti. Papildus tiešajai citotoksicitātei NK šūnas atbrīvo dažādus citokīnus un ķemokīnus, piemēram, GM-CSF, IFN-, TNF- un ķemokīnus: CCL3, CCL4 un CCL5 [101] vai saskaras ar citām imūnšūnām, piemēram, T un B šūnām un DC [102,103]. Turklāt tiem ir imunoloģiska atmiņa, kas var saglabāties, saskaroties ar radniecīgu antigēnu [104]. Janus kināzes/signālu pārvades un transkripcijas aktivatora (JAK-STAT) ceļam ir svarīga loma NK šūnu nobriešanā, citotoksicitātē vai izdzīvošanā, un ir zināms, ka lielākā daļa citokīnu, kas var aktivizēt vai bloķēt NK šūnas, to regulē [105]. Ir konstatēts, ka IL-2, kam ir svarīga loma NK šūnu proliferācijā un receptoru ekspresijā, var aktivizēt STAT1, 3 un 5. Turklāt STAT5 aktivizē IL-15 un STAT1 un 3. tiek aktivizēti ar IL-21, kas izraisa NK šūnu proliferāciju, nobriešanu un aktivāciju [106]. Tāpēc NK šūnu hiperaktivācija un disfunkcija ir saistīta ar dažu iekaisuma un autoimūnu slimību patoģenēzi. Tomēr NK šūnām šajās slimībās var būt gan aizsargājoša, gan patogēna loma atkarībā no slimības veida un apkārtējās vides [107, 108].
Kai et al. [109] identificēja INF atkarīgo IDO1 mRNS ekspresiju NK šūnās, un IDO1 farmakoloģiskā inhibīcija samazināja NK šūnu citotoksicitāti pret vēža šūnām. Šis atradums tika apstiprināts in vivo zemādas B16 audzēju modelī pelēm [64]. Šie rezultāti liecināja, ka IDO1 efektoru NK šūnās uztur normālu citotoksicitāti pret audzēja šūnām. Tomēr ir arī ziņots, ka IDO1 katabolīti bloķē NK šūnu proliferāciju [110]. Nesenais pētījums par Park et al. [111] parādīja, ka IDO1 aktivizēšana audzēja šūnās izraisīja aktivējošo dabisko citotoksisko receptoru NKp46 un NKG2D pazemināšanos NK šūnās, nomācot to citolītisko aktivitāti un izraisot NK šūnu nāvi. Šo destruktīvo efektu izraisīja IDO1 regulēšana un KYN ražošana, kas caur AhR iekļūst NK šūnās uz to virsmām un tieši pasliktina NK šūnu darbību. Ārstēšana ar KYN izraisīja samazinātu STAT1 un STAT3 fosforilēšanos NK šūnās no devas atkarīgā veidā, norādot, ka KYN regulē NK šūnas, izmantojot STAT signalizācijas ceļus. Turpretim IDO1 aktivitātes farmakoloģiskā bloķēšana audzēja šūnās atjaunoja NK šūnu citolītisko aktivitāti un receptoru ekspresiju [111]. Šie dati liecina, ka IDO1 aktivācija NK šūnās, kas atrodas audzēja vidē, var spēlēt pretvēža funkciju, savukārt IDO1, ko ražo pašas audzēja šūnas, var darboties kā negatīvas atgriezeniskās saites mehānisms pret pretvēža imūnreakcijām.
3.3.4. IDO1 un eozinofīli
Eozinofīli ir daudzfunkcionāli leikocīti, kas ir iesaistīti iekaisuma procesu, tostarp helmintu infekciju un alerģisku slimību, patoģenēzē. Tās tiek uzskatītas par šūnām, kas galvenokārt darbojas kā pirmās līnijas aizsardzība pret parazītiem vai var modulēt imūnās atbildes reakciju uz dažādiem stimuliem. IL-5, ko galvenokārt ražo Th2 šūnas, ir būtisks citokīns eozinofilu diferenciācijai, sagatavošanai un izdzīvošanai [112]. Neskatoties uz to, paši eozinofīli kalpo par dažādu citokīnu un augšanas faktoru avotu, kas ir cieši saistīti ar vairākām imūnmodulējošām funkcijām, un ir iesaistīti daudzos homeostatiskos procesos aizkrūts dziedzerī, piena dziedzeros, dzemdē un kuņģa-zarnu traktā [113,114]. Tie uzrāda ķīmijaksi pret limfoīdo ķīmokīnu un uzrāda APC līdzīgas īpašības, stimulējot ar dažiem citokīniem.
Šo šūnu antigēnu prezentējošās īpašības ir iespējamas, pateicoties antigēnu prezentācijas un kostimulācijas molekulu, tostarp MHC-II, CD80, CD86, CD28 un CD40 [115], ekspresijai. tāpat kā viņu tiešās savstarpējās sarunās ar DC [116]. Eozinofilu spēja uzrādīt antigēnus un alergēnu izraisīta piesaiste plaušu audos ir ierosināta kā pierādījums mijiedarbībai starp eozinofiliem un T limfocītiem [117]. Pētījums par Venge et al. [118] astmas pacientiem liecina, ka eozinofīli aktīvi piedalās plaušu audu fibrozē un remodelācijā, saistot tos ar šīs slimības iespējamo etioloģiju un pacientu dzīves kvalitātes pasliktināšanos. No otras puses, ir pierādīts, ka eozinofīli var piedalīties audu atjaunošanā, jo tie ir aprīkoti ar audu bojājumu noteikšanas sistēmu un var atbrīvot vairākas audus atjaunojošas molekulas, piemēram, dažādus augšanas faktorus [112].
Cilvēka eozinofīli ekspresē funkcionāli aktīvo IDO1 gan konstitutīvi, gan pēc IFN indukcijas [62,119], un KYN sintezējošu eozinofilu kopkultūra ar IFN ražojošām T šūnām, bet ne IL-4- ražojošām T šūnu apakšgrupām, izraisīja apoptozi un inhibīciju. Th1 apakšgrupas proliferāciju, bet Th2 šūnu līnija tika saglabāta [62]. Tā pati komanda parādīja, ka IDO1 farmakoloģiskā inhibīcija in vivo izraisīja perorālās imūnās tolerances maiņu ovalbumīna (OVA) inducētā peļu modelī un ka atkārtota intranazāla OVA ievadīšana radīja toleranci un novērsa turpmāku sensibilizāciju pret OVA [120]. Šie rezultāti norādīja, ka ar IFN- -apstrādāti eozinofīli var veicināt Th2 polarizāciju, izpaužot funkcionāli aktīvu IDO1 limfoīdos audos. Turklāt eozinofīli var izraisīt Th2 reakciju, jo tie pēc stimulācijas spēj ražot kanoniskus Th2 citokīnus, piemēram, IL-4, IL-5 un IL-13 [121]. Tomēr Tulic et al. [122] novēroja funkcionāla IDO1 klātbūtni, kas cilvēka zīdaiņa dzīves laikā nepatoloģisku apstākļu laikā tika konstitutīvi izteikts aizkrūts dziedzera eozinofilos. Vienlaikus KYN tika atklāts intracelulāri un ap šūnām, kas morfoloģiski atgādina eozinofilus. IDO1 un TRP katabolīta-KYN indukcija veicināja Th2 šūnu dominēšanu pār Th1 šūnām, kuras šajos apstākļos tiek pakļautas selektīvai apoptozei. Iepriekš minētie dati liecina par IDO{28}}izpaušanas eozinofilu imūnmodulējošu lomu, kas var būtiski ietekmēt adaptīvo imūno attīstību.

3.3.5. IDO1 un neitrofīli
Neitrofīli ir polimorfonukleāri leikocīti, un tie ir parādīti kā viens no būtiskiem spēlētājiem akūtu iekaisuma stāvokļu laikā, kurus dažu minūšu laikā var piesaistīt no asinsrites uz traumas vietām. Tie likvidē iebrukušos patogēnus, izmantojot vairākus mehānismus, piemēram, baktericīdu molekulu sekrēciju, iesaistīšanos fagocitozē, degranulācijā un proteolītisko enzīmu un reaktīvo skābekļa sugu (ROS) sekrēcijā vai kodolmateriāla atbrīvošanu neitrofilu ārpusšūnu slazdu veidā [123]. Cirkulējošie neitrofīli parasti ir "atpūtas šūnas", un to kaitīgais intracelulāro granulu saturs netiek atbrīvots, lai izvairītos no saimnieka audu bojājumiem. Tomēr neitrofīli var kļūt sagatavoti imūnsistēmas apstākļos, kad to reakcija uz proinflammatorisko stimulāciju var palielināties 10- līdz 20- reizes, kā rezultātā pastiprinās apkārtējo veselo audu bojājumi [124]. Neitrofilu pārmērīga aktivācija un piesaiste ir saistīta ar dažādu hronisku iekaisuma stāvokļu attīstību, piemēram, reimatoīdo artrītu, iekaisīgu zarnu slimību, reimatoīdo artrītu, metabolisko sindromu, aterosklerozi un vēzi [123, 125]. No otras puses, neitrofīli var arī veicināt brūču dzīšanu un iekaisuma ierobežošanu [126, 127].
Papildus neitrofilu galvenajai lomai iedzimtajā imunitātē šīs šūnas var būtiski modulēt adaptīvās imunitātes galvenās sastāvdaļas, iedarbojoties uz B šūnām un T šūnām. Neitrofīli ražo citokīnus — B šūnu aktivējošo faktoru (BAFF) un proliferāciju izraisošo ligandu (APRIL), kas nepieciešami B šūnu izdzīvošanai un aktivizēšanai, kā arī to stimulēšanai, lai tās ražotu antivielas [128]. Neitrofīli var ražot argināzi-1 un ROS, un tādā veidā tie var kavēt T šūnu proliferāciju un aktivāciju [129]. Tie var darboties arī kā APC, veicinot Th1 un Th17 diferenciāciju [130], un var uzrādīt antigēnus tieši T šūnām vai pārnest tos uz DC [131].
Ir zināmi daži neitrofilu apakštipi, un starp tiem ir identificētas neitrofīlās mieloīdās nomācošās šūnas (MDSC), kurām ir liela nozīme imūnās atbildes regulēšanā vēža un daudzu ar hronisku iekaisumu saistīto patoloģisko stāvokļu gadījumā [132]. Precīzi šūnu mehānismi, ar kuriem MDSC var nomākt T-šūnu atbildes, nav pilnībā izskaidroti, bet Novitskiy et al. [133] atklāja, ka MDSC inkubācija ar IL-17 palielināja šo šūnu nomācošo aktivitāti, palielinot argināzes 1, IDO1 un ciklooksigenāzes-2 ekspresiju piena dziedzera karcinomas modelī pelēm. Loughman et al. [134] novēroja, ka uropatogēnā Escherichia coli (UPEC) infekcija samazināja fagocītu nogalināšanu un mazināja neitrofilu antimikrobiālo ROS veidošanos, kā arī pazemināja to proinflammatorisko signālu pārraidi, ķīmijaksi, adhēziju un migrāciju.
Tā pati komanda parādīja, ka UPEC vājināja iedzimtas reakcijas, in vitro inducējot IDO1 ekspresiju cilvēka uroepitēlija šūnās un neitrofilos, un ka neitrofilu apstrāde ar specifisku IDO1 inhibitoru ievērojami uzlaboja to transepitēlija migrāciju, reaģējot uz UPEC. Turklāt neitrofilu funkcija netika ietekmēta IDO1-nokautajām pelēm [135]. Līdzīgi, sākotnējā Plasmodium vivax iedarbība izraisīja iedzimtas imunitātes aktivizēšanos, taču šo efektu pavadīja spēcīga imūnsupresija, ko izraisīja IDO1- ekspresējošie DC, kas bija saistīti ar dažu neitrofilu populāciju izsīkšanu. Tā kā neitrofīli regulē DC darbību infekcijas laikā, šķiet, ka šo šūnu populāciju savstarpējā saruna ir svarīga iedzimtas imūnās atbildes sastāvdaļa [136]. Šie rezultāti liecināja, ka IDO1 ekspresijas indukcija neitrofilos kavē proinflammatoriskas iedzimtas reakcijas un veicina patogēnu kolonizāciju, apstiprinot IDO1 lomu kā kritisku regulatoru agrīnā saimnieka un patogēna savstarpējās sarunās. No otras puses, tika arī ierosināts, ka regulējošie Tregi, kas radās IDO{11}}mediētas imūnsupresijas laikā, varēja veicināt TGF ražošanu, kā arī IDO1 un hema oksigenāzes{14}} ekspresiju ar neitrofilu palīdzību. Tādējādi Tregs var spēlēt nozīmīgu lomu iedzimtu imūnreakciju tiešā kontrolē, inducējot neitrofilus ar imūnsupresīvām īpašībām [137].
For more information:1950477648nn@gamil.com
