Urīna mērstieņa proteīnūrijas līmenis un tā saistība ar holelitiāzes risku Ⅱ
Feb 28, 2024
REZULTĀTI
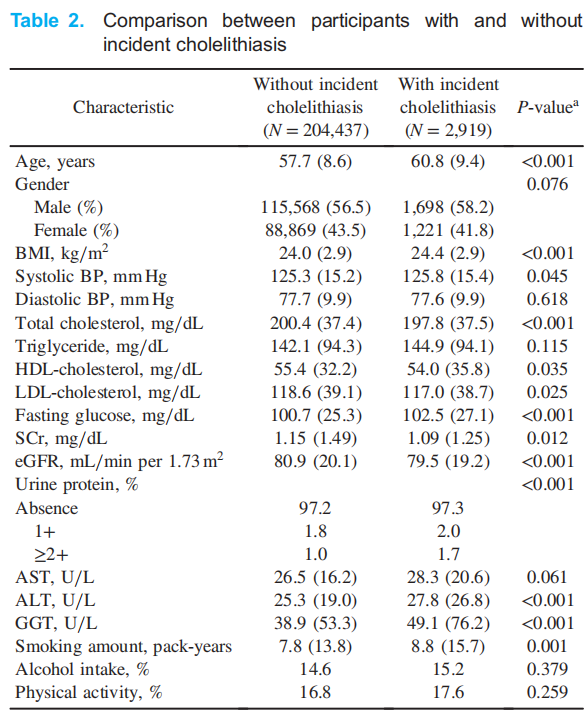
904 360 persongadu novērošanas laikā no 2009. līdz 2013. gadam attīstījās 2919 (1,41%) holelitiāzes gadījumi. Tabula1 apraksta pētījuma dalībnieku sākotnējos raksturlielumus trīs grupās nourīna olbaltumvielu līmenis. Bija zīmesfinevar diFfatšķirības starp trim grupām visos bāzes raksturlielumos, izņemotZBL-holesterīnsun fiziskās aktivitātes. Grupām ar lielāku proteīnūriju bija sliktāki klīniskie apstākļi nekā tām, kurām nebijaproteīnūrija, kas bija pamanāmāks tukšā dūšā glikozes, triglicerīdu, eGFR un SCr vidējās vērtībās nekā citi mainīgie. Tomēr, neskatoties uz statistiski nozīmīgiemfinevar diFference iekšāP- attiecībā uz tendenci daži mainīgie neuzrādīja klīniski nozīmīgu diFfstarp grupām. Jo īpaši šisfinding bija atšķirīgs mainīgajos, kas saistīti araptaukošanās un aknu darbība,ieskaitot ĶMI, AST, ALT un GGT, kas bija normas robežās visās grupās. Novērošanas laikā tika konstatēti 2919 gadījumi ar holelitiāzi, un šo personu īpašības, salīdzinot ar pārējo kohortu, ir parādītas tabulā.2. Atšķirībā no dalībniekiem bezincidents holelitiāze, tie, kuriem bija konstatēta holelitiāze, bija vecāki (60,8 [SD, 9,4] pret 57,7 [SD, 8,6] gadiem), un tiem bija mazāk labvēlīgas sākotnējās ĶMI, sistoliskā rakstura pazīmes.BP, TG, ABL-holesterīns, eGFR, ASAT, ALT, GGT un smēķēšanas daudzums. Jo īpaši grupai ar negadījumu holelitiāzi bija augstāks sākotnējo raksturlielumu līmenis saistībā ar aptaukošanos un aknu darbību, piemēram, ĶMI, ASAT, ALAT un GGT. Tomēr visi mainīgie lielumi neparādīja specifikufic virzienā, un grupai bez cho holelitiāzes bija augstāks diastoliskā asinsspiediena, kopējā holesterīna, ZBL holesterīna, SCr,alkohola lietošana, un fiziskām aktivitātēm. Tabula3 parāda HR un 95% CI holelitiāzei atbilstoši trim grupām. Nekoriģētajā modelī holelitiāzes HR, salīdzinot vieglas un smagas proteīnūrijas grupu ar negatīvo grupu, bija 1,12 (95% TI, 0.87).–1,45) un 1,77 (95% TI, 1,33–2,34), attiecīgi (P tendencei<0.001). Adjustment for covariates attenuated this association, but statistical signifivēzis saglabājās smagas proteīnūrijas grupā (HR 1,46; 95% TI, 1,09–1,96). Pēc pielāgošanas kovariātiem holelitiāze bija zīmīgaficieši saistīta ar ĶMI, vecumu, alkohola lietošanu, smēķēšanu un GGT. Dzimumu apakšgrupu analīze liecināja, ka smaga proteīnūrija sievietēm bija nozīmīgaficieši saistīts ar paaugstinātu holelitiāzes risku (HR 1,68; 95% TI, 1,06–2.65) pat pēc tampielāgošana kovariātiem (1. tabula). Vīrieši arī parādīja zīmifiaprunātības asociācija nekoriģētajā modelī (HR 1,65; 95% TI, 1,15–2,37), kas pazuda pēc kovariātu korekcijas (HR 1,31; 95% TI, 0,89–1,92). Vecuma apakšgrupu analīzē (2. tabula), grupas vecumsLielāks par vai vienāds ar56 gadi parādīja zīmifiapzināta saistība starp smagu proteīnūriju un akūtu holelitiāzi (HR 1,44; 95% TI, 1,01–2.03), bet grupas vecumsMazāks par vai vienāds ar55 gadi neliecināja par zīmifiaprunātības saistība pēc kovariātu korekcijas (HR 1,47; 95% TI, 0,85–2.55).

KLIKŠĶINIET ŠEIT, LAI IEGŪTU DABĪGU ORGANISKO CISTANŠES EKSTRAKTU AR 25% EHINAKOZĪDU UN 9% AKTEOZĪDU NIERU FUNKCIJAI
Wecistanche atbalsta dienests - lielākā cistanche eksportētāja Ķīnā:
E-pasts:wallence.suen@wecistanche.com
Whatsapp/Tel.:+86 15292862950
Iegādājieties sīkāku informāciju par specifikācijām:
https://www.xjcistanche.com/cistanche-shop

AST, aspartātaminotransferāze; ALAT, alanīna aminotransferāze; ĶMI, ķermeņa masas indekss; BP, asinsspiediens; eGFR, aprēķinātais glomerulārās filtrācijas ātrums; GGT, gamma-glutamiltransferāze; ABL, augsta blīvuma lipoproteīns; ZBL, zema blīvuma lipoproteīns; SCr, seruma kreatinīns. Dati ir vidējie (standarta novirze), mediānas (starpkvartiļu diapazons) vai procenti. P vērtība ar ANOVA testu nepārtrauktiem mainīgajiem un Hī kvadrāta tests kategoriskiem mainīgajiem.
BP, TG, ABL-holesterīns, eGFR, ASAT, ALT, GGT un smēķēšanas daudzums. Jo īpaši grupai ar negadījumu holelitiāzi bija augstāks sākotnējo raksturlielumu līmenis saistībā ar aptaukošanos un aknu darbību, piemēram, ĶMI, ASAT, ALAT un GGT. Tomēr visi mainīgie lielumi neparādīja konkrētu virzienu, un grupai bez cholelitiāzes bija augstāks diastoliskā asinsspiediena, kopējā holesterīna, ZBL holesterīna, SCr, alkohola uzņemšanas un fiziskās aktivitātes līmenis. 3. tabulā parādīti HR un 95% TI holelitiāzei atbilstoši trim grupām. Nekoriģētajā modelī holelitiāzes HR, salīdzinot vieglas un smagas proteīnūrijas grupu ar negatīvo grupu, bija attiecīgi 1,12 (95% TI, 0,87–1,45) un 1,77 (95% TI, 1,33–2,34) ( P tendencei<0.001). Adjustment for covariates attenuated this association, but statistical significance was maintained in the heavy proteinuria group (HR 1.46; 95% CI, 1.09–1.96). After adjusting for covariates, cholelithiasis was significantly associated with BMI, age, alcohol intake, smoking, and GGT. Gender subgroup analysis indicated that heavy proteinuria in women was significantly associated with an increased risk of incident cholelithiasis (HR 1.68; 95% CI, 1.06–2.65) even after adjusting for covariates (table 1). Men also showed a significant association in the unadjusted model (HR 1.65; 95% CI, 1.15–2.37), which disappeared after adjustment for covariates (HR 1.31; 95% CI, 0.89–1.92). In age subgroup analysis (table 2), the group age ≥56 years showed a significant association between heavy proteinuria and incident cholelithiasis (HR 1.44; 95% CI, 1.01–2.03), but the group age ≤55 years did not show a significant association after adjustment for covariates (HR 1.47; 95% CI, 0.85–2.55).
AST, aspartātaminotransferāze; ALAT, alanīna aminotransferāze; ĶMI, ķermeņa masas indekss; BP, asinsspiediens; eGFR, aprēķinātais glomerulārās filtrācijas ātrums; GGT, gamma-glutamiltransferāze; ABL, augsta blīvuma lipoproteīns; ZBL, zema blīvuma lipoproteīns; SCr, seruma kreatinīns. Dati tiek izteikti kā vidējie (standarta novirze) vai procenti. P-vērtība ar t-testu nepārtrauktiem mainīgajiem un Hī kvadrāta tests kategoriskiem mainīgajiem.

DISKUSIJA
Valsts mēroga datu garengriezuma analīzē mēs novērtējām negadījuma holelitiāzes risku atbilstoši urīna mērstieņa proteīnūrijas līmenim. Mūsu rezultāti liecināja, ka urīna mērstieņa proteīnūrija {{0}} vai lielāka ir būtiski saistīta ar paaugstinātu holelitiāzes risku. Studiju priekšmetu bāzes raksturlielumu analīze nodrošina potenciālu mehānismu šim konstatējumam. Personām ar augstāku urīna mērstieņa proteīnūriju bija sliktāki vielmaiņas un nieru stāvokļi, kas līdzīgi tika novēroti pacientiem ar nejaušu holelitiāzi. Šie atklājumi liecina, ka nelabvēlīgiem klīniskiem apstākļiem bija nozīme žultsakmeņu attīstībā. Šo secinājumu apstiprina iepriekšējie pētījumi, kas parāda vielmaiņas traucējumu, piemēram, insulīna rezistences, aptaukošanās un dislipidēmijas lomu žultsakmeņu, proteīnūrijas un HNS attīstībā.14–16 Tādējādi tiek pieņemts, ka vielmaiņas vide, kas veicina proteīnūriju, izraisa patofizioloģiskie procesi, kas saistīti ar žultsakmeņu veidošanos. Tomēr ir interesanti, ka mūsu rezultāti bija statistiski nozīmīgi pat pēc kovariantu pielāgošanas, tostarp tādiem tradicionālajiem žultsakmeņu riska faktoriem kā vecums, dzimums, ĶMI, sistoliskais BP, glikozes līmenis tukšā dūšā, kopējais holesterīns, GGT, alkohola lietošana un fiziskā aktivitāte. Šis rezultāts norāda, ka proteīnūrija var būt neatkarīgs žultsakmeņu riska faktors. Iepriekšējie pētījumi arī ir parādījuši, ka ar proteīnūriju saistītas nieru slimības, iespējams, ir saistītas ar žultsakmeņiem. Šķērsgriezuma pētījumā, kurā piedalījās 2686 vīrieši un 2087 sievietes Taivānā11, žultsakmeņu izplatība bija 13,1% pacientu ar HNS un 4,9% pacientu grupā bez HNS (P < 0,001). Turklāt ir pierādīts, ka žultsakmeņu izplatība bija ievērojami augstāka pacientiem ar beigu stadijas nieru slimību (ESRD), kas tika ārstēti ar dialīzi, salīdzinot ar neurēmisku grupu.17,18 Novērošanas pētījumi ir parādījuši būtisku saistību starp žultsakmeņiem un nierēm. akmeņi.19,20 Šie rezultāti rada hipotēzi, ka starp nieru slimību un žultsakmeņu slimības patofizioloģiskajiem mehānismiem var būt ievērojama pārklāšanās. Turklāt, ņemot vērā, ka proteīnūrija ir nieru slimību, tostarp HNS un nierakmeņu, klīniska izpausme, šie rezultāti var saistīt proteīnūriju ar žultsakmeņiem. Tomēr iepriekšējos pētījumos ir ierobežota tiešā proteīnūrijas ietekme uz žultsakmeņiem. To ierobežojumi ir saistīti ar šķērsgriezuma dizainu, 10,11 mazāku rezultātu vispārināmību, kas iegūti tikai no ESRD pacientiem,17,18 un vāju cēloņsakarību starp nierakmeņiem un proteīnūriju.19,20 Turklāt vairākos pētījumos ir ziņots, ka žultsakmeņi neatšķīrās starp dialīzes pacientiem un veselām kontrolēm.21–23 Turpretim mēs analizējām garenvirziena saistību starp urīna mērstieņa proteīnūrijas līmeni un žultsakmeņu rašanās risku, kas var būt priekšrocība, nosakot nieru slimību klīniskās sekas. proteīnūriju kā žultsakmeņu riska faktoru.

Mūsu analīzē smaga proteīnūrija (lielāka vai vienāda ar {{0}}) bija nozīmīgi saistīta ar paaugstinātu žultsakmeņu risku, savukārt viegla proteīnūrija (1+) neuzrādīja statistiski nozīmīgu saistību ar žultsakmeņi. Iepriekšējie pētījumi ir parādījuši, ka proteīnūrijas līmenis bija uzticams sākuma faktors, kas cieši korelē ar eGFR samazināšanās ātrumu un progresējošu HNS.24,25 Tādējādi tiek uzskatīts, ka smagas proteīnūrijas grupā bija lielāks progresējošas HNS ar urēmiju īpatsvars nekā pacientiem ar urēmiju. vieglas proteīnūrijas grupā novērošanas periodā. Urēmiskais stāvoklis var izjaukt sarežģīto neirālo un hormonālo faktoru procesu, kas kontrolē žultspūšļa kustīgumu.26–28 Neironu un hormonālo nelīdzsvarotība var izmainīt žultspūšļa kustīgumu, veicinot žultsakmeņu veidošanos ar žultspūšļa stāzi HNS pacientiem.26–28 Tomēr mēs nevaram garantēt. ka urēmiskais stāvoklis, ko izraisa CKD, ir galvenais mehānisms saistībā ar proteīnūriju un holelitiāzi mūsu pētījumā. Mēs nevarējām novērtēt nieru funkcijas izmaiņas novērošanas laikā, jo netika veikti SCr un eGFR papildu mērījumi. Turpmākajos pētījumos jāizpēta ilgtermiņa saistība starp sākotnējo proteīnūriju, nieru funkcijas izmaiņām un holelitiāzes risku. Pētījuma priekšrocības ir lielais studiju priekšmetu skaits, labi sakārtoti medicīniskie dokumenti (tostarp holelitiāzes diagnoze) un laboratoriskie mērījumi, kuru pamatā ir ticami valsts mēroga dati. Šīs priekšrocības ļauj kvantitatīvi noteikt gadījuma holelitiāzes risku atbilstoši urīna mērstieņa proteīnūrijas līmenim. Tomēr mēs atzīstam pētījuma ierobežojumus. Pirmkārt, proteīnūrijas līmenis tika novērtēts tikai, izmantojot urīna mērstieņa testu. Lai gan urīna mērstieņa tests ir plaši pieejams proteīnūrijas skrīningam, ar to nepietiek, lai precīzi noteiktu proteīnūriju. Otrkārt, novērošanas periods vidēji 4,36 gadi bija salīdzinoši īss. Kumulatīvais holelitiāzes sastopamības biežums mūsu pētījumā bija 2,5%, bet ilgāka novērošana var izraisīt gan zemāku holelitiāzes sastopamības biežumu, gan lielāku kumulatīvo holelitiāzes sastopamību. Treškārt, mūsu pētījums tika veikts tikai salīdzinoši gados vecākiem korejiešiem, kuru vidējais vecums bija 57, 8 (SD, 8, 6) gadi. Mūsu pētījums parādīja, ka proteīnūrijas +1 un Lielāka vai vienāda ar 2+ proteīnūrijas izplatība ir attiecīgi 1,8% un 1.0%. Tomēr kohortas pētījumā, kurā piedalījās 18 201 275 korejieši ar vidējo vecumu 45,3 (SD, 14,6) gadi, pamatojoties uz NHID, 1+ proteīnūrijas un lielāka vai vienāda ar 2+ proteīnūrijas izplatība bija 1,18% ( Attiecīgi n=214,883) un 0,56% (n=103,745).29 Lielāka proteīnūrijas izplatība mūsu pētījumā var būt saistīta ar mūsu subjektu vecāku vecumu. Ceturtkārt, mēs nevarējām pārbaudīt holelitiāzes sastopamības derīgumu pētījumā, jo trūka apstiprinājuma holelitiāzes sastopamības biežumam no iepriekšējām analīzēm, izmantojot NHID. Piektkārt, neskatoties uz iespējamību, ka pēcpārbaudes laikā var tikt zaudēta novērošana, mēs nevarējām veikt jutīguma analīzi mūsu neapstrādāto datu ierobežojumu dēļ. NHID nebija paredzēts pētījumiem, bet gan korejiešu veselības stāvokļa izpētei. Tāpēc mēs nevarējām noteikt jutīguma analīzei nepieciešamo informāciju.
Šie ierobežojumi garantē nepieciešamību veikt turpmākus pētījumus ar precīzākām metodēm, kas nosaka proteīnūriju, ilgāku novērošanu un lielu skaitu priekšmetu, tostarp jaunākas vecuma grupas. Noslēgumā jāsaka, ka personām ar lielāku proteīnūriju bija lielāks holelitiāzes sastopamības biežums, un urīna mērstieņa proteinūrija 2+ vai lielāka bija nozīmīgi saistīta ar paaugstinātu holelitiāzes risku. Šie rezultāti papildina pierādījumus hipotēzei, ka nieru slimības klātbūtne, ko atspoguļo proteīnūrija, ir neatkarīgs žultsakmeņu slimības riska faktors.
PATEICĪBA
Mēs izmantojām Nacionālā veselības apdrošināšanas dienesta – Nacionālās izlases kohortas datubāzi, un datu kopa tika iegūta no Nacionālā veselības apdrošināšanas dienesta. Mūsu pētījuma rezultāti nebija saistīti ar Valsts veselības apdrošināšanas dienestu. Autora ieguldījums: Jae-Hong Ryoo ir šī darba garants, un tādējādi viņam ir pilnīga piekļuve visiem pētījuma datiem, un viņš uzņemas atbildību par datu integritāti un datu analīzes precizitāti. Sung Keun Park piedalījās studiju plānošanā, manuskriptu sagatavošanā un manuskriptu rediģēšanā un kā pirmais autors rakstīja manuskriptu. Chang-Mo Oh piedalījās pētījuma izstrādē un manuskripta sagatavošanā. Dong-Young Lee un Jung Wook Kim piedalījās datu analīzes interpretācijā un manuskriptu pārskatīšanā. Min-Ho Kim un Hee Yong Kang piedalījās datu iegūšanā, datu un algoritmu kvalitātes kontrolē, datu analīzē un interpretācijā, kā arī statistiskajā analīzē. Eunhee Ha piedalījās datu iegūšanā un manuskriptu pārskatīšanā. Ju Young Jung piedalījās manuskripta rediģēšanā. Interešu konflikti: nav paziņots.
PIELIKUMS A. PAPILDU DATI
Ar šo rakstu saistītos papildu datus var atrast vietnē https:== doi.org=10.2188=jea.JE20190223.
ATSAUCES
1. Lee JY, Keane MG, Pereira S. Žultsakmeņu slimības diagnostika un ārstēšana. Praktizētājs. 2015; 259:15–19, 2.
2. Jorgensens T, Jensens KH. Kam ir žultsakmeņi? Pašreizējie epidemioloģiskie pētījumi. Nord Med. 1992;107:122–125.
3. Lu SN, Chang WY, Wang LY u.c. Žultsakmeņu riska faktori ķīniešu vidū Taivānā. Sabiedrības sonogrāfiskā aptauja. J Clin Gastroenterol. 1990;12:542–546.
4. Sandler RS, Everhart JE, Donowitz M u.c. Atsevišķu gremošanas slimību slogs Amerikas Savienotajās Valstīs. Gastroenteroloģija. 2002; 122: 1500–1511.
5. Marschall HU, Einarsson C. Žultsakmeņu slimība. J Intern Med. 2007. gads; 261:529–542.
6. Ansaloni L, Pisano M, Coccolini F u.c. 2016. gada WSES vadlīnijas par akūtu calculous holecistītu. Pasaules J Emerg Surg. 2016;11:25.
7. Ruhl CE, Everhart JE. Žultsakmeņu slimība ir saistīta ar paaugstinātu mirstību Amerikas Savienotajās Valstīs. Gastroenteroloģija. 2011; 140:508–516.
8. Méndez-Sánchez N, Bahena-Aponte J, Chávez-Tapia NC u.c. Spēcīga saistība starp žultsakmeņiem un sirds un asinsvadu slimībām. Esmu J Gastroenterols. 2005;100(4):827–830.
9. Méndez-Sánchez N, Zamora-Valdés D, Flores-Rangel JA u.c. Žultsakmeņi ir saistīti ar karotīdu aterosklerozi. Liver Int. 2008;28(3):402–406.
10. Ahmeds MH, Barakat S, Almobarak AO. Saikne starp nierakmeņu slimību un holesterīna žultsakmeņiem: viegli noticēt un grūti izgūt metaboliskā sindroma teoriju. Ren Fail. 2014; 36:957–962.







