Ar NADC{0}}piemēram, PRRSV celmu inficētām cūkām eksosomālo MiRNS izteikto profilu sistemātiska identificēšana un salīdzināšana
Dec 27, 2023
Vienkāršs kopsavilkums:Eksosomām ir unikāla loma vīrusu infekcijā, antigēnu prezentācijā un ķermeņa imunitātes nomākšanā/veicināšanā. Cūku reproduktīvā un respiratorā sindroma vīruss (PRRSV) ir viens no kaitīgākajiem patogēniem cūkkopības nozarē. Šeit mēs izmantojām PRRSV NADC30-, piemēram, CHsx1401 celmu, lai mākslīgi inficētu 42-dienu vecas cūkas, izolētu seruma eksosomas un identificētu 33 ievērojami atšķirīgi ekspresētas (DE) eksosomu miRNS starp infekcijas un kontroles grupām. 18 DE miRNS, kas saistītas ar PRRSV infekciju un imunitāti, tika pārbaudītas kā potenciālas funkcionālas molekulas, kas iesaistītas PRRSV vīrusa infekcijas regulēšanā ar eksosomu palīdzību.
Abstract:Eksosomas ir bioloģiskas pūslīši, ko izdala un atbrīvo šūnas, kas darbojas kā starpšūnu komunikācijas mediatori un kurām ir unikāla loma vīrusu infekcijā, antigēnu prezentācijā un ķermeņa imunitātes nomākšanā/veicināšanā. Cūku reproduktīvā un respiratorā sindroma vīruss (PRRSV) ir viens no kaitīgākajiem patogēniem cūkkopības nozarē un var izraisīt reproduktīvos traucējumus sivēnmātēm, elpceļu slimības cūkām, samazinātu augšanas veiktspēju un citas slimības, kas izraisa cūku mirstību. Šajā pētījumā mēs izmantojām PRRSV NADC{0}}piemēram, CHsx1401 celmu, lai mākslīgi inficētu 42-dienu vecas cūkas un izolētu seruma eksosomas. Pamatojoties uz augstas caurlaidspējas sekvencēšanas tehnoloģiju, seruma eksosomās pirms un pēc inficēšanās tika identificētas 305 miRNS, no kurām 33 miRNS tika izteikti atšķirīgi starp grupām (13 relatīvi paaugstināti un 20 relatīvi pazemināti). CHsx1401 genoma sekvences saglabāšanas analīze identificēja 8 konservētus reģionus, no kuriem kopumā tika prognozēts, ka 16 atšķirīgi ekspresētas (DE) miRNS saistās ar konservēto reģionu, kas ir vistuvāk 3.0 CHsx1401 genoma UTR, ieskaitot 5 DE miRNS, kas spēj saistīties ar CHsx1401 30 UTR (ssc-miR-34c, ssc-miR-375, ssc-miR-378, ssc-miR-486, ssc-miR-6529). Turpmākā analīze atklāja, ka atšķirīgi ekspresētu miRNS mērķa gēni bija plaši iesaistīti ar eksosomu funkciju saistītos un iedzimtos imunitātes signalizācijas ceļos un 18 DE miRNS (ssc-miR-4331-3p, ssc-miR-744 Tika pārbaudīti ssc-miR-320, ssc-miR-10b, ssc-miR-124a, ssc-miR-128 u.c.), kas saistīti ar PRRSV infekciju un imunitāti. kā potenciālas funkcionālas molekulas, kas iesaistītas PRRSV vīrusa infekcijas regulēšanā ar eksosomu palīdzību.

cistanche augu paaugstinošā imūnsistēma
Atslēgvārdi:PRRSV; seruma eksosoma; miRNS
1. Ievads
Cūku reproduktīvā un respiratorā sindroma vīruss (PRRSV) ir vienpavedienu pozitīvas virknes RNS vīruss ar apvalka struktūru, kas pieder pie Nidovirales kārtas, Arteriviridae dzimtas, Betaarterivirus ģints [1,2]. Tas ir sfērisks vai elipsoidāls ar diametru 50–65 nm zem saldēšanas elektronu mikroskopa [3,4]. PRRSV genoms ir aptuveni 15 kb garš ar 50 vāciņu un 30 poliA asti, un tajā ir vismaz 10 atvērti lasīšanas kadri (ORF), kurus papildina netulkotie reģioni (UTR) gan 50, gan 30 galos [5,6] un ir iesaiņots ar nukleokapsīda proteīnu ar lipīdu divslāņu pārklājumu, veidojot vīrusa daļiņas. Eksosomas pieder pie pūslīšiem ar vienslāņu membrānas struktūrām, un tām ir tāda pati topoloģiskā struktūra kā šūnām [7]. Forma elektronu mikroskopā ir "krūzītveida" vai "diska formas" [8,9]. Eksosomas var pastāvēt asinsrites sistēmā ilgu laiku, un eksosomās esošās vielas var absorbēt blakus esošās šūnas vai attālās receptoru šūnas un pēc tam regulēt receptoru šūnas, lai tās piedalītos ģenētisko materiālu apmaiņā starp šūnām [10,11]. Tos galvenokārt veido membrānas virsmas vielas un saturs, tostarp šūnu virsmas receptori, membrānas proteīni, šķīstošie proteīni, lipīdi, RNS (mRNS, miRNS, lncRNS un vīrusu RNS utt.), genoma DNS, mitohondriju DNS [12–14] ]. MikroRNS (miRNS) ir 18–25 nukleotīdu (nt) evolucionāri konservētu endogēnu nekodējošu vienpavedienu mazo RNS klase, kas kavē translācijas procesu, izraisot mērķa mRNS degradāciju vai saistoties ar 30 UTR mērķa mRNS, kā rezultātā uz pēctranskripcijas gēnu klusēšanu, pēc tam regulējot gēnu ekspresiju pēctranskripcijas līmenī [15–17]. Tiek lēsts, ka miRNS pēc transkripcijas regulē vairāk nekā 60% zīdītāju gēnu [18,19]. MiRNS ir svarīga loma starpšūnu komunikācijā, un tās var izmantot arī kā potenciālu funkcionālu molekulu slimību un vīrusu infekcijām, pārnešanai un aizsardzībai [20]. Arvien vairāk pētījumu ir parādījuši, ka miRNS var atrasties ķermeņa šķidrumos, piemēram, siekalās, urīnā, mātes pienā un asinīs, un darboties caur ķermeņa šķidruma asinsrites sistēmu [21,22]. Eksosomālās miRNS tiek uzskatītas par endogēniem gēnu ekspresijas un metabolisma regulatoriem un var norādīt uz dažādiem patoloģiskiem stāvokļiem [23, 24].

cistanche tubulosa-uzlabo imūnsistēmu
Pēdējo divu desmitgažu laikā ir pierādīts, ka miRNS ir izšķiroša loma imūno šūnu attīstības, iedzimtu imūnreakciju un iegūto imūnreakciju regulēšanā. Tiek ziņots, ka dažas citas miRNS pasliktina PRRSV infekciju, izmantojot šādus veidus, tieši vērstas pret PRRSV genomu vai PRRSV receptoru vai spēlē lomu, regulējot saimnieka iedzimto imūnreakciju. MiR-26 saime var būtiski bojāt vīrusu replikāciju, un miR-26a var kavēt 1. un 2. tipa PRRSV celmu replikāciju cūku alveolārajos makrofāgos (PAM), regulējot I tipa interferonu (IFN) ceļš, kas ir efektīvāks par miR-26b [25,26]. Ir identificēts, ka miR-30c un miR-125b modulē saimniekorganisma iedzimto imūnreakciju, mērķējot attiecīgi uz I tipa IFN ceļu un NF-κB ceļu [27–29]. MiR-23, miR-378 un miR-505 ir pretvīrusu saimniekfaktori, kas vērsti pret PRRSV, un tiem ir konservatīvas mērķa vietas 2. tipa PRRSV celmos [30]. Tajā pašā laikā ir konstatēts, ka saimnieks miR-506 inhibē PRRSV replikāciju, tieši mērķējot uz PRRSV receptoru CD151 MARC-145 šūnās [31]. miR-181 var arī netieši inhibēt PRRSV replikāciju, samazinot PRRSV receptoru CD163 asins monocītos un PAM [32]. Turklāt miRNS var veicināt PRRSV replikāciju, traucējot pamata šūnu fizioloģiju. MiR-24-3p un miR-22 PRRSV infekcijas laikā ir tieši vērstas uz HO-1 30 UTR, lai izvairītos no hēma oksigenāzes-1 (HO-1) inhibīcijas. karstuma šoka proteīns (pazīstams arī kā HSP32) uz PRRSV [33,34]. Ir zināms, ka cūkas ir jutīgākas pret PRRSV un mazāk spēj aizsargāties pret šī patogēna iekļūšanu organismā [35]. Šajā pētījumā ar šo vīrusu inficēto cūku iedzimtā imunitāte un iegūtā imunitāte tika pētīta molekulārā līmenī, izmantojot uz lauka izplatītu celmu. Seruma eksosomu izolācijas komplekts, transmisijas elektronu mikroskopija (TEM), nanodaļiņu izsekošanas analīze (NTA) un Western blot (WB) tika izmantots, lai izolētu un identificētu seruma eksosomas pirms un pēc inficēšanās ar PRRSV, kam sekoja neliela RNS sekvencēšanas analīze, identifikācija, un diferenciālās ekspresijas rezultātu analīze, izmantojot bioinformātikas metodes, lai iegūtu vairākas ar PRRSV saistītus seruma eksosomu miRNS, kam seko datu rezultātu identificēšana, izmantojot kvantitatīvu reālā laika PCR (qRT-PCR).
2. Materiāli un metodes
2.1. Eksperimenti ar dzīvniekiem
Sešas PRRSV antigēnu un antivielu dubultnegatīvas veselīgas 42-dienu vecas lielas baltas cūkas tika ievietotas cūku tīrās barošanas sistēmā izolācijai, veselības aprūpei un vides pielāgošanai. Visas cūkas varēja brīvi ēst un dzert bez ierobežojumiem. Kad cūkas bija iepazinušās ar apstākļiem izolatorā, cūkas nazāli inokulēja ar 2 ml 105 TCID50/mL PRRSV NADC30-, piemēram, CHsx1401, ko minēja priekšgājēji [36, 37]. Cūku asinis pirms (kontroles grupa, n=6) un 7 dienas pēc (ārstēšanas grupa, n=6) vīrusa inokulācijas tika savāktas no priekšējās dobās vēnas seruma izolēšanai. Šūnu atliekas serumā tika noņemtas, centrifugējot pie 3000 g 15 minūtes. Visus eksperimentus ar dzīvniekiem mūsu pētījumā apstiprināja Ķīnas Lauksaimniecības zinātņu akadēmijas (CAAS) (Pekina, Ķīna), IAS Dzīvnieku zinātnes institūta Dzīvnieku ētikas komiteja2022-130.
2.2. Seruma eksosomu izolēšana un attīrīšana
Eksosomu izolēšana un attīrīšana tika veikta, izmantojot exoEasy Maxi komplektu (QIAGEN, Hilden, Vācija, kat. nr. 76064) saskaņā ar ražotāja protokolu.
2.3. Transmisijas elektronu mikroskopija (TEM)
Ekstrahētās eksosomu suspensijas tika uzklātas uz formvar karbo pārklājuma vara sieta, un eksosomas tika izskalotas ar PBS un pakļautas standarta uranilacetāta krāsošanai 3 minūtes istabas temperatūrā. Pēc žāvēšanas vairākas minūtes istabas temperatūrā režģis tika vizualizēts un fotografēts pie 100 kV ar transmisijas elektronu mikroskopu (HT-7700, Hitachi-High Tech, Tokija, Japāna).
2.4. Nanodaļiņu izsekošanas analīze (NTA)
Ekstrahētās eksosomas tika atšķaidītas ar 1 × PBS, mainot tilpumu no 10 līdz 30 µL. Pēc parauga pārbaudes seruma eksosomu koncentrācija un lielums tika analizēti ar N30E plūsmas nanoanalizatoru, ievērojot ražotāja norādījumus (NanoFCM, Xiamen, Ķīna).
2.5. Western Blot
Ekstrahētie eksosomu paraugi tika pievienoti RIPA lizātam, kas sajaukts ar proteāzes inhibitoru (Invitrogen, Waltham, MA, ASV) un fenilmetilsulfonilfluorīdu (PMSF), lai ekstrahētu eksosomu proteīnu, kas tika lizēts uz ledus 30 minūtes. Pēc tam saskaņā ar Bredforda komplekta norādījumiem mēs kvantitatīvi noteicām seruma eksosomu proteīna koncentrāciju. Eksosomu proteīni tika termiski denaturēti. Tāds pats olbaltumvielu daudzums tika atdalīts uz 12% SDS-PAGE gēla un pēc tam pārnests uz polivinilidēnfluorīda (PVDF) membrānu (Millipore, Burlington, MA, ASV). Tas tika mērcēts TBST, kas satur 5% vājpiena pulvera, un slēgts 1 stundu istabas temperatūrā. Mēs iemērcām membrānu atšķaidītā primārajā antivielā (anti-CD9 antiviela, Abcam, Boston, MA, ASV, #ab92726; anti-CD81 antiviela, Abcam, Boston, MA, ASV, #ab109201) 4 ◦C temperatūrā un atguvām. primārā antiviela. Mēs iemērcām membrānu atšķaidītā sekundārajā antivielā, inkubējām to istabas temperatūrā 1 stundu un atguvām sekundāro antivielu. Mēs uzlikām mazgāto PBST plēvi uz svaigi saglabājošās plēves, pievienojām vienāda tilpuma sajauktu ECL a / b hromogēno šķīdumu un ievietojām to hemiluminiscences attēlveidā.

cistanche priekšrocības vīriešiem - stiprina imūnsistēmu
Noklikšķiniet šeit, lai skatītu Cistanche Enhance Immunity produktus
【Jautājiet vairāk】 E-pasts:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
2.6. Eksosomu mazo RNS sekvencēšana un datu analīze
Kopējā RNS no eksosomām tika ekstrahēta ar Trizol saskaņā ar ražotāja norādījumiem. Pēc tam mēs noteicām RNS koncentrāciju un optiskā blīvuma (OD) vērtību un atklājām RNS noārdīšanos un tīrību ar 1% agarozes gēla elektroforēzi. Tikmēr RNS integritātes noteikšanai tika izmantots Agilent Bioanalyzer 2100. Pēc kvalitātes pārbaudes mēs izmantojām kopējo eksosomu RNS. Saskaņā ar ražotāja norādījumiem mēs izmantojām NEB NEXT multiplex mazās RNS bibliotēkas sagatavošanas komplektu Illumina® (Illumina, Sandjego, CA, ASV). Komplekts sagatavoja nelielu RNS cDNS bibliotēku un sekvencēja to, lai radītu 50 nt viena gala nolasījumus, izmantojot Illumina Novaseq 6000 platformu. Visas nelielas RNS bibliotēkas sagatavošanas procedūras veica Novogene (Pekina, Ķīna). Dati pēc kvalitātes kontroles tika saskaņoti ar cūku atsauces genomu (Sus scrofa 11.1), izmantojot tauriņu. Zināmās miRNS tika identificētas, izmantojot miRbase (v22.0) datubāzi [38] (https://www.mirbase.org, piekļūts 2022. gada 14. janvārī), miRdeep2 (v0.0.5) [39] un miRevo (v1.1). ) [40] un tika izmantoti jaunu miRNS prognozēšanai. Tajā pašā laikā miRNS diferenciālās ekspresijas analīzi veica DESeq (v1.24.0) [41], kas prasīja |reizes izmaiņas| > 1,6 un p < 0,05. Izlīdzināšana tika veikta, izmantojot MEGA (V11) [42], kam sekoja vienas bāzes punktu noteikšana, izmantojot PHAST (v1.6.9) [43], un 10 vīrusa gēnu konservatīvāko reģionu novērtējums, tostarp WUH3 (GenBank pievienošanās numurs HM853973), VR2332 ( GenBank pievienošanās nr. U87392), JXA1 (GenBank pievienošanās nr. EF112445), CH-1a (GenBank pievienošanās nr. AY032626), NADC30 (GenBank pievienošanās nr. HN654459), HUN4 (GenEF6HL50D6),3 JZD6. 22-1812 (GenBank pievienošanās nr. MN648450), SC/DJY (GenBank pievienošanās nr. MT075480) un Lelystad (GenBank pievienošanās nr. M96262.2). RNShibrīds (V2.0) [44] tika izmantots, lai prognozētu identificētās miRNS sekvences saistīšanos ar CHsx1401 vīrusa genoma 3 0 UTR. Gēnu prognozēšanai tika izmantota Miranda (v3.3a) un RNAhybrid. Klastera profila [45] R pakotne tika izmantota GO (Gene Ontology) mērķa gēnu funkcionālās bagātināšanas analīzei un KEGG (Kyoto Encyclopedia of Genes and Genomes) ceļa bagātināšanas analīzei.
2.7. MiRNS ekspresijas apstiprināšana ar RT-qPCR
Kopējā RNS tika izolēta no seruma eksosomām, izmantojot Trizol (Invitrogen, Šanhaja, Ķīna) saskaņā ar ražotāja protokolu. Izolētā RNS tika pārbaudīta ar RT-qPCR paraugiem (n=6 katrā grupā). cDNS tika sintezēta saskaņā ar miRNS 1. virknes cDNS sintēzes (ar cilmes cilpas) komplekta instrukcijām (Vazyme, Nanjing, Ķīna), un fluorescences kvantitatīvā noteikšana tika veikta, izmantojot ABI 7500 saskaņā ar miRNA universālā SYBR qPCR galvenā maisījuma instrukcijas (Vazyme, Nanjing, Ķīna). Izmantotie termiskā cikla parametri bija šādi: pirmais posms: 95 ◦C 30 s; 2. posms: 95 ◦C 5 s, 60 ◦C 34 s un 40 cikli; 3. posms: 95 ◦ C 15 s, 60 ◦ C 1 min un 95 ◦ C 15 s. MiRNS primer sekvences, U6 gēns, tika izmantotas kā atsauce [46] un uzskaitītas S1 papildu tabulā. Visas qRT-PCR pārbaudes tika veiktas, izmantojot trīs bioloģiskos atkārtojumus un trīs atkārtojumus katram paraugam. Transkriptu relatīvais daudzums tika aprēķināts ar 2-Ct metodi, un datu analīzei un kartēšanai tika izmantoti attiecīgi SPSS (v22.0) un GraphPad Prism (v8.0). p < 0,05 nozīmē, ka atšķirība ir statistiski nozīmīga.
3. Rezultāti
3.1. Antigēna un antivielu relatīvā vērtība pēc vīrusa inokulācijas
PRRSV antigēna un antivielu testu rezultāti pirms (0. diena) un pēc (7. diena) ir parādīti 1. tabulā. PRRSV antigēna un antivielu seroloģiskā noteikšana pirms provokācijas bija negatīva, un antigēns tika konstatēts. pozitīvs pēc izaicinājuma, norādot, ka cūkas tika veiksmīgi inficētas ar CHsx1401.
3.2. Seruma eksosomu izolēšana un identifikācija
No seruma izolētās vezikulas atklāja TEM. Lielākā daļa pūslīšu vidū var redzēt ieliektas apakštasītes vai diska formas eksosomas. Ir redzama eksosomu membrānas mala, un morfoloģija ir salīdzinoši pilnīga (1.A, B attēls). Nanodaļiņu izsekošanas analīze parādīja, ka 95, 73% eksosomu diametrs bija 30–150 nm, galvenokārt aptuveni 72, 25 nm, ar vidējo diametru 76, 22 nm, kas atbilda eksosomu izmēra īpašībām (1. C attēls). Šis lieluma diapazons bija līdzīgs TEM noteiktajam un vēl vairāk apstiprināja šo pūslīšu identitāti kā eksosomas. Western blot analīze parādīja, ka no seruma paraugiem izolētie pūslīši bija pozitīvi attiecībā uz CD9 un CD81 proteīniem (1D attēls). Iepriekš minētie raksturlielumi atbilst eksosomu identifikācijas standartiem, ko MISEV2018 formulējusi Starptautiskā Extrace Vesicles biedrība (ISEV) [47].
1. tabula. Antigēns un antiviela (diena 0) un (7. diena) ar provokācijas vīrusu.

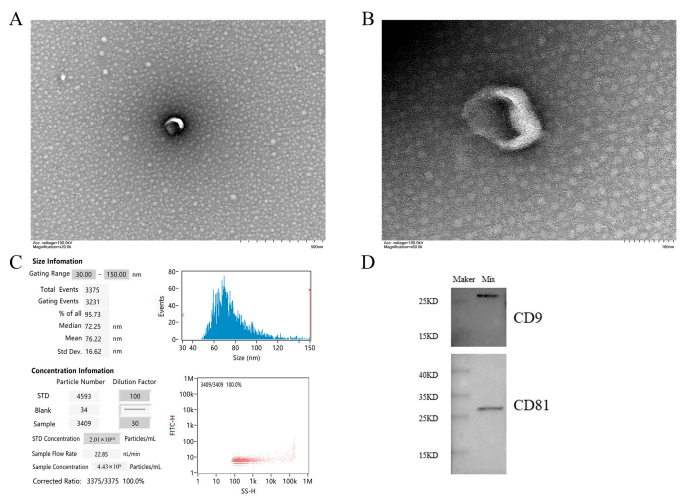
1. attēls. Seruma eksosomu galvenie raksturlielumi. (A, B) parāda vezikulu morfoloģiskās īpašības ar TEM. Mēroga joslas ir attiecīgi 500 nm un 100 nm. (C) NTA parāda vairuma pūslīšu diametru un koncentrāciju. (D) Western blot parādīja eksosomu marķieru CD81 un CD9 klātbūtni seruma eksosomās. Piezīme. Mix in WB rezultāti ir parauga jauktā suspensija, kas izolēta ar exoEasy Maxi komplektu
3.3. Seruma eksosomu mazā RNS sekvencēšana
Katram paraugam tīrie dati sasniedza 0,5 Gb, un 30. ceturkšņa bāzes procentuālā vērtība pārsniedza 96,20%. Katra parauga tīrie nolasījumi tika saskaņoti ar cūkas atsauces genomu. No 12 paraugiem kontroles grupa ieguva attiecīgi 10 920 887, 10 248 696, 10 109 117, 10 655 494, 9 217 285 un 9 782 523 nolasījumus. Ārstēšanas grupa ieguva attiecīgi 11 889 518, 10 593 504, 10 593 504, 12 846 080, 10 105 325, 11 729 451 un 9 789 542 lasījumus. Vidēji 77,96% no visiem tīrajiem nolasījumiem bija 19–22 nukleotīdu (nt) garumā (2.A attēls). Nolasījumi pēc kvalitātes kontroles veidoja vairāk nekā 92,59% no kopējā nolasījumu skaita. Apstrādātie tīrie nolasījumi tika saskaņoti ar cūku atsauces genomu, un 12 bibliotēku kartētais ātrums genomā bija vairāk nekā 92,30%, un kartētais rādītājs bija 94,98% (2.B attēls). Tas norādīja, ka izveidotā seruma eksosomālā miRNS bibliotēka bija augstas kvalitātes un piemērota turpmākai analīzei. Sīkāka informācija ir norādīta S2 papildu tabulā.

2. attēls. Mazo RNS transkriptu datu pārskats. (A) seruma eksosomu paraugu nolasīto skaita garuma sadalījums (nt=nukleotīdi); (B) 12 paraugu ātrums, kas kartēts ar atsauces genomu
3.4. MiRNS diferenciālas ekspresijas analīze
Pēc identificētās miRNS ekspresijas kvantitatīvās analīzes miRNS tika pārbaudītas pēc sliekšņiem, kas aprakstīti iepriekš 2.6. Kopā tika iegūtas 305 miRNS pirms un pēc CHsx1401 celma inokulācijas (kontrole, n=6; apstrāde, n=6). Abās grupās tika identificētas pavisam 33 atšķirīgi ekspresētas (DE) miRNS, 13 DE miRNS tika paaugstināti regulētas un 20 DE miRNS tika samazinātas ārstēšanas grupā (3. attēls un S3 papildu tabula).
3.5. miRNS mērķa gēnu funkcionālās bagātināšanas analīze
Kopumā 33 DE miRNS prognozēja 7283 mērķa gēnus, un mērķa gēnu funkcijas galvenokārt koncentrējās MAPK kaskādes pozitīvajā regulēšanā, lipīdu metabolisma procesā, intracelulārā signāla transdukcijas regulēšanā, ERK1 un ERK2 kaskādē uc (4.A attēls). ). Runājot par molekulārajām funkcijām, atšķirīgi izteiktie miRNS mērķa gēni galvenokārt koncentrējas uz GTP-enzīmu regulējošo aktivitāti, kināzes aktivitāti, nukleozīdu trifosfatāzes regulējošo aktivitāti un citām funkcijām, kas saistītas ar signālu pārraidi un enerģijas metabolismu (4.B attēls). Turklāt starp šūnu komponentiem mērķa gēni galvenokārt piedalās supramolekulāro polimēru, Golgi, autofagosomu, šūnu virsmas, agrīno endosomu uc bioloģiskajās funkcijās (4.C attēls). Šo komponentu funkcijas ir cieši saistītas ar eksosomu veidošanos, kas arī izskaidro sekvencēšanas precizitāti. KEGG ceļa bagātināšanas analīze parādīja, ka mērķa gēni bija ievērojami bagātināti ar endocitozi, MAPK signalizācijas ceļu, Rap1 signalizācijas ceļu, sfingolipīdu signalizācijas ceļu un PI3K Akt signālu ceļu (p < 0.05) (5A attēls) ). Tajā pašā laikā bagātinātie ceļi tika klasificēti un analizēti. Rezultāti parādīja, ka mērķa gēna KEGG ceļš galvenokārt bija bagātināts ar vides informācijas apstrādi, cilvēku slimībām un bioloģiskajām sistēmām (5.B attēls).

3. attēls. MiRNS diferenciālā ekspresija eksosomās. (A) miRNS vulkāna diagramma starp kontroles un ārstēšanas grupām; (B) DE miRNS hierarhiskā klasterizācijas karte starp kontroles un ārstēšanas grupām.
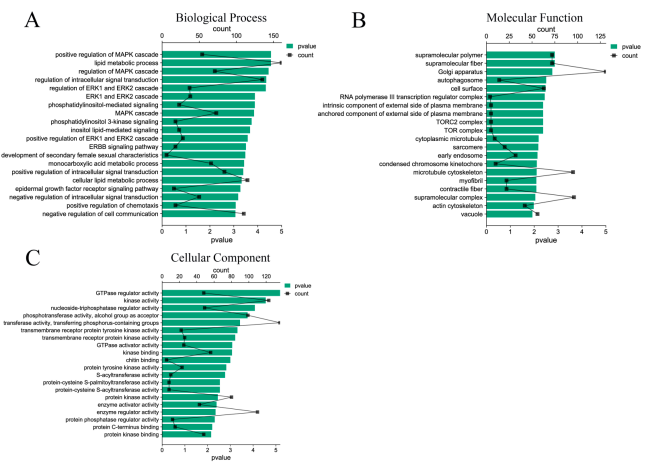
4. attēls. DE miRNS mērķa gēnu GO funkciju bagātināšanas analīze. (A) DE miRNS mērķa gēnu bioloģiskais process; (B) DE miRNS mērķa gēnu molekulārās funkcijas; (C) DE miRNS mērķa gēnu šūnu komponenti

5. attēls. Mērķa gēnu KEGG ceļa bagātināšanas analīze. (A) ievērojami bagātināts KEGG ceļš ar DE miRNS mērķa gēniem; (B) ievērojami bagātinātu KEGG ceļu klasifikācija.
3.6. Seruma eksosomālās miRNS un PRRSV CHsx1401 genoma mērķa prognoze
Saskaņā ar vienas bāzes phastCons punktu skaitu pēc izlīdzināšanas ar PHAST, starp vīrusu genomiem tika iegūti kopumā astoņi visvairāk konservēti segmenti (melnas joslas virs pīķa kartes) (6. attēls). Tika konstatēts, ka pavisam 31 DE miRNS saistās ar konservēto segmentu, paredzot miRNS, kas saistītas ar konservēto segmentu. Tostarp konservētajā reģionā (14 644–15 020 nt), kas ir vistuvāk CHsx1401 genoma 30 UTR (14 870–15 020), tiek prognozēts, ka ar to saistās 16 DE miRNS, tostarp 5 miRNS (ssc-}}miR{{15). c, ssc-miR-375, ssc-miR-378, ssc-miR-486 un ssc-miR-6529), kas var saistīties ar CHsx1401 30 UTR. No šīm miRNS tikai ssc-miR-223 tika regulēts pēc inficēšanās, un citas miRNS tika pazeminātas pēc inficēšanās. Sīkāku informāciju skatiet S4 papildu tabulā.

6. attēls. Konservēti segmenti CHsx1401 celma genomā, ko paredz PHAST
3.7. DE miRNS skrīnings saistībā ar eksosomu funkciju un PRRSV
Izmantojot mērķa gēnu funkcionālās bagātināšanas analīzi, tika atrastas dažādas diferencēti izteiktas miRNS, kas saistītas ar eksosomu un PRRSV funkciju. Starp tiem 11 DE miRNS, piemēram, ssc-miR-4331-3p, ssc-miR-744 un ssc-miR-320, ir iesaistīti eksosomu uzņemšanā, un to mērķa gēni galvenokārt ir koncentrēti Ras gēnu saime, aneksīnu saime un ADP ribosilācijas gēnu saime. Astoņpadsmit DE miRNS, tostarp sscmiR-10b, ssc-miR-124a un ssc-miR-128, piedalās ar imūnsistēmu saistītos ceļos, un to mērķa gēni galvenokārt ir koncentrēti MAPK. gēnu saime, PIK3 gēnu saime un proteīna fosfatāzes gēnu saime. Kamēr vīrusu invāzijā ir iesaistīti 11 DE miRNS, saistītie mērķa gēni galvenokārt ir koncentrēti MAPK gēnu ģimenē un proteīna fosfatāzes gēnu ģimenē. Turklāt vairākas atšķirīgi izteiktas miRNS, piemēram, jaunas_102. Sešas DE miRNS, tostarp ssc-miR-320, ssc-miR-423-5p, ssc-miR-4331-3p, ssc-miR-7137-3p un ssc-miR{{ 25}}, tiek līdzekspresēti eksosomu funkcijā, PRRSV vīrusa invāzijā un ar imūnsistēmu saistītos ceļos, kā parādīts 7. attēlā. Sīkāka informācija ir parādīta S5 papildu tabulā.
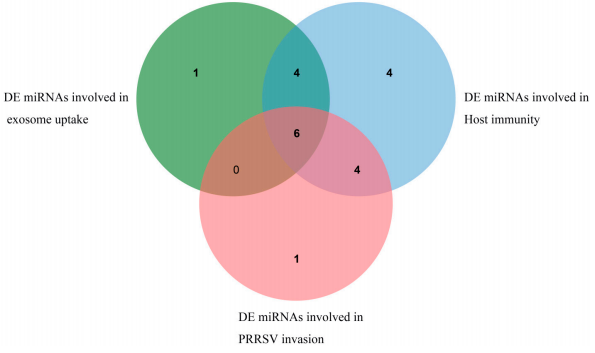
7. attēls. DE miRNS, kas saistītas ar eksosomu uzņemšanu, PRRSV invāziju un imunitāti
3.8. DE miRNS QRT-PCR tests starp abām grupām
Verifikācijai nejauši tika atlasītas piecas DE miRNS. Saskaņā ar qRT-PCR rezultātiem ssc-miR-19a un ssc-miR-32 ekspresija ārstēšanas grupā palielinājās, savukārt ssc-miR-124a, ssc-miR{ {8}} un ssc-miR-34c uzrādīja augstāku izteiksmi kontroles grupā, kas atbilst secības datiem (8. attēls).

8. attēls. Piecas DE miRNS, kas apstiprinātas ar qRT-PCR
4. Diskusija
PRRSV joprojām ir spītīgs patogēns globālajā cūkkopības nozarē, radot milzīgus ekonomiskos zaudējumus pasaulē. Pašlaik vakcināciju galvenokārt izmanto PRRSV profilaksei un kontrolei, starp kurām visplašāk tiek izmantota modificētā dzīvā (MLV) vīrusa vakcīna [48]. Lai gan šī vakcīna bija efektīva PRRS uzliesmojumu un sastopamības samazināšanā, tā arī ievērojami palielināja vīrusa ģenētisko variāciju un daudzveidību un izraisīja vīrusu rekombināciju starp savvaļas un dzīviem vakcīnas vīrusiem uz lauka [49,50]. Pēdējos gados rekombinantā vīrusa NADC30-līdzīgā PRRSV celma izplatība un izplatība Ķīnā ir izraisījusi vairākus cūku reproduktīvā un respiratorā sindroma uzliesmojumus. Šajā pētījumā izmantotā CHsx1401 un NADC30 līdzība saglabājās 92, 2–99, 1%. Kopš tā laika tas ir kļuvis par epidēmisku celmu Ķīnā. Eksosomas kā šūnu komunikācijas mediatori ir plaši sastopamas dažādos ķermeņa šķidrumos, un tām ir unikālas priekšrocības slimību diagnostikā un ārstēšanā [51,52]. Saskaņā ar iepriekšējiem ziņojumiem eksosomām ir svarīga komunikācijas loma antigēnu prezentācijā [53], imūnās atbildes reakcijā [53, 54], vīrusa replikācijā [54], vēzī [55], neirodeģeneratīvās slimībās [56], angioģenēzē [57], audzēja šūnā. migrācija [58] un invāzija [59], un tiem ir augsta pētnieciskā vērtība.
Šajā pētījumā tika izmantota augstas caurlaidības sekvencēšanas tehnoloģija, lai izveidotu seruma eksosomu miRNS ekspresijas profilu, un tika identificētas 33 DE miRNS. Kā mēs visi zinām, saimnieka kodētā miRNS var saistīties ar vīrusa genomu un pēc tam regulēt vīrusa replikāciju, sintēzi un izdalīšanos, lai ierobežotu infekciju un ietekmētu patoloģisko procesu [15]. Ir atkārtoti ziņots arī par miRNS pētījumiem, kas vērsti uz vīrusa genomu, ar dzīvniekiem. gga-miR-454 un gga-miR-130b cāļu infekciozās bursālās slimības gadījumā var mērķēt uz vīrusa genomu, lai kavētu vīrusa replikāciju, savukārt gga-miR-21 ir tieši vērsts pret vīrusa proteīnu VP1, lai inhibētu. vīrusu proteīnu translācija [60,61]. PRRSV pētījumos ssc-miR-181 īpaši saistās ar ļoti konservētu reģionu lejpus vīrusa genoma ORF4 un spēcīgi inhibē PRRSV replikāciju [62]. Šajā pētījumā ssc-miR-181 izteiksmes atšķirība starp abām grupām nesasniedza nozīmīgu līmeni. Mūsu pētījumā deviņu dažādu PRRSV vīrusu genomi tika salīdzināti ar CHsx1401 celma genomiem, un tika identificēti astoņi visvairāk konservētie segmenti. Tika prognozēts, ka 31 DE miRNS varētu saistīties ar 8 visvairāk konservētajiem CHsx1401 segmentiem un 16 DE miRNS varētu saistīties ar konservētajām sekvencēm, kas ir tuvu CHsx1401 30 UTR. Tostarp 5 DE miRNS (ssc-miR-34c, ssc-miR-375, ssc-miR-378, ssc-miR-486 un ssc-miR{{ 36}}) var vienlaikus saistīties ar CHsx1401 30 UTR. Turklāt tika prognozēts, ka ssc-miR-223 augšupregulētā ekspresija saistās ar PRRSV genoma 30 UTR mērķi. Rezultāti parādīja, ka vīrusa genoma konservētajām sekvencēm var būt galvenā loma tā patogenitātē, un miRNS, kas var saistīties ar konservētajām sekvencēm starp dažādu PRRSV celmu genomiem, var būt nozīmīgas vīrusa patogenitātes kontrolē. Iepriekšējos pētījumos ir pierādīts, ka dažas diferencēti izteiktas miRNS ir saistītas ar PRRSV un pat ir tieši iesaistītas PRRSV regulēšanā, tostarp ssc-miR-10b [63], ssc-miR-378 [30]. , ssc-miR-124a [64], let-7f-5p [65], ssc-miR-744 [66] un ssc-miR{{57 }}a [67].
PRRSV var izvairīties no saimnieka aizsardzības, traucējot iedzimtu imūnreakciju. Šo procesu regulē daudzi signalizācijas ceļi, tostarp MAPK signalizācijas ceļš, PI3K Akt signalizācijas ceļš, autofagija, kemokīns un TNF signalizācijas ceļš. Pašlaik MAPK signalizācijas ceļš ietver trīs galvenos ceļus: ERK1/2, JNK un p38 ceļu. MAPK kaskādes aktivizēšana var veicināt saimniekšūnu apoptozi, palīdzēt vīrusam izbēgt no saimnieka imūnās aizsardzības reakcijas un veicināt PRRSV replikāciju [68]. Turklāt c-Jun N-terminālo kināžu (JNK) un p38 aktivizēšana var arī veicināt iekaisuma faktora IL-10 [68–70] izdalīšanos un pastiprināt iekaisuma efektu. Papildus apoptozes ierosināšanai PRRSV var izraisīt arī autofagiju, kas var veicināt PRRSV replikāciju. PI3K/Akt aktivizēšana ir nepieciešama vīrusa iekļūšanai un vīrusa replikācijas veicināšanai, un PRRSV aktivētais Akt inhibē saimniekšūnu apoptozi, negatīvi regulējot JNK ceļu [71]. TNF Tam var būt nozīmīga loma iekaisuma reakcijas ierosināšanā un regulēšanā kopā ar citiem iekaisuma faktoriem, bet TNF ekspresiju ietekmē PRRSV replikācijas negatīvā regulēšana [72]. Šajā pētījumā miRNS (ssc-miR-10b, ssc-miR-122-5p, ssc-miR-124a, ssc-miR-128, ssc-miR{ {24}}a-5p utt.), kas bagātināti ar šiem ceļiem, ir iesaistīti PRRSV izraisītā apoptozē, autofagijā un iekaisumā un ir cieši saistīti ar vīrusu imūnreakciju, imūno izvairīšanos un replikāciju.

cistanche tubulosa-uzlabo imūnsistēmu
Šūnu plazmas membrāna ir bagāta ar dažādiem lipīdu plostiem, un ar sfingolipīdiem un holesterīnu bagāti sfingolipīdi (sfingomielīns un glikosfingolipīdi) ir galvenās lipīdu plostu molekulas. Dažu vīrusa proteīnu lipīdu atpazīšana var būt nepieciešams nosacījums vīrusa iekļūšanai [73]. Apvalka vīrusi ievada vīrusa apvalka glikoproteīnus lipīdu plostos vīrusa iekļūšanas stadijā, mijiedarbojas ar receptoriem, kas atrodas lipīdu plostos, vai pāriet no to dabiskā stāvokļa uz aktivētu formu, lai uzsāktu vai veicinātu vīrusu internalizāciju/saplūšanu, piemēram, HSV, SARS koronavīrusu un sivēnu epidēmiskās caurejas vīruss [73,74]. Iepriekšējie pētījumi atklāja, ka holesterīna noņemšana no MARC-145 šūnu virsmas ievērojami samazināja PRRSV infekciju, parādot, ka PRRSV infekcijas inhibīciju īpaši veicināja šūnu holesterīna noņemšana. Šūnu membrānas holesterīna samazināšanās ievērojami kavēja vīrusa iekļūšanu, īpaši vīrusa piesaisti un atbrīvošanos [75]. Sfingolipīdu metabolisms var regulēt membrānas struktūru un adhēziju, kam ir liela nozīme PRRSV vīrusa invāzijā. Endocitoze bija visnozīmīgākā bagātināšana šajā pētījumā. Endocitoze ir svarīgs mērķa šūnu eksosomu uzņemšanas mehānisms. Iepriekšējie pētījumi ir parādījuši, ka eksosomu uzņemšana ir enerģijas prasīgs un no citoskeleta atkarīgs process, kas izceļ endocitozes iespējamo lomu šajā procesā [76]. Ir pierādīts, ka šo procesu var veicināt vairāki ceļi, tostarp fagocitoze, makropinocitoze, klatrīns utt. [77,78], kas noveda pie dažādām endocitozēto vielu klasifikācijām un lomām. Atšķirīgi izteiktu eksosomu miRNS bagātināšana šajā ceļā norāda, ka eksosomām ir svarīga loma PRRSV infekcijā, un satura transportēšanas un uzņemšanas regulēšana eksosomās var izraisīt patofizioloģiskas izmaiņas mērķa šūnās un orgānos.

cistanche tubulosa-uzlabo imūnsistēmu
5. Secinājumi
Veicot ar PRRSV inficētu cūku seruma eksosomālo miRNS identifikāciju un bioinformātisko analīzi, šajā pētījumā tika iegūti dažādi ar PRRSV saistīti ceļi un diferencēti izteiktas miRNS, piemēram, ssc-miR-4331-3p, ssc-miR{{ 5}}, sscmiR-320, ssc-miR-10b, ssc-miR-124a, ssc-miR-128 utt., kam ir potenciāla funkcionāla loma PRRSV -izraisīta imūnreakcija, invāzija un eksosomu uzņemšana. Turklāt, tā kā viena miRNS var mērķēt uz vairākiem gēniem un vienu gēnu regulē arī vairākas miRNS, vairākas miRNS veic vairākas funkcijas iepriekšminētajos ceļos. Ir pārbaudīts, ka dažas miRNS regulē PRRSV infekciju, iedarbojoties uz galvenajiem receptoriem vai tieši mērķējot uz vīrusa genomu, piemēram, ssc-miR-10b, ssc-miR-378, miR-124a, ļaujiet visvairāk konservēts fragments no CHX1401 vīrusa genoma 30 UTR, tostarp ssc-miR-34c, ssc-miR-375, ssc-miR-378, ssc-miR{{34} } un ssc-miR-6529, kas var būt svarīgi vīrusu patogenitātes regulēšanai.
Atsauces
1. Snijder, EJ; Kikerts, M.; Fang, Y. Arterivirus molekulārā bioloģija un patoģenēze. J. ģenerālis Virols. 2013, 94 Pt 10, 2141–2163. [CrossRef] [PubMed]
2. Lu, Y.; Džans, Y.; Xiang, X.; Šarma, M.; Liu, K.; Vejs, J.; Šao, D.; Li, B.; Tongs, G.; Olševskis, MA; un citi. Notch signalizācija veicina iekaisuma citokīnu ekspresiju, ko izraisa ļoti patogēna cūku reproduktīvā un respiratorā sindroma vīrusa (HP-PRRSV) infekcija cūku alveolārajos makrofāgos. Izstrādātājs Comp. Immunol. 2020, 108, 103690. [CrossRef] [PubMed]
3. Dea, S.; Sojers, N.; Alēns, R.; Athanassious, R. Cūku reproduktīvā un respiratorā sindroma vīrusa ultrastrukturālās īpašības un morfoģenēze, kas izplatīta ļoti pieļaujamajā MARC-145 šūnu klonā. Adv. Exp. Med. Biol. 1995, 380, 95–98. [PubMed]
4. Dokland, T. PRRSV strukturālā bioloģija. Virus Res. 2010, 154, 86–97. [CrossRef] [PubMed]
5. Džonsons, CR; Grigs, TF; Gnanandarajah, J.; Murtaugh, MP Jauns strukturālais proteīns cūku reproduktīvā un respiratorā sindroma vīrusā, ko kodē alternatīvs ORF5, kas atrodas visos arterivīrusos. J. ģenerālis Virols. 2011, 92 Pt 5, 1107–1116. [CrossRef] [PubMed]
6. Lī, SC; Lī, S.; Yoo, GW; Choi, HW; Nē, JH; Parks, CE; Shin, JH; Yoon, IJ; Kanga, SY; Lee, C. Vājināta cūku reproduktīvā un respiratorā sindroma vīrusa celma fenotipiskā un genotipiskā analīze pēc sērijveida pasāžas kultivētos cūku alveolārajos makrofāgos. J. Vet. Sci. 2018, 19, 358–367. [CrossRef] [PubMed]
7. Zebrovska, A.; Skovroneks, A.; Vojakovska, A.; Vidlaks, P.; Pietrowska, M. Metabolome of Exosomes: Koncentrējieties uz pūslīšiem, ko atbrīvo vēža šūnas un kas atrodas cilvēka ķermeņa šķidrumos. Int. J. Mol. Sci. 2019, 20, 3461. [CrossRef]
8. Bēbelmans, deputāts; Smits, MJ; Pegtels, DM; Baglio, SR Ekstracelulāro pūslīšu bioģenēze un funkcija vēža gadījumā. Pharmacol. Tur. 2018, 188, 1.–11. [CrossRef]
9. Zaborovskis, deputāts; Balajs, L.; Breakfield, XO; Lai, CP Ārpusšūnu pūslīši: Sastāvs, bioloģiskā nozīme un pētījumu metodes. Bioscience 2015, 65, 783–797. [CrossRef]
10. Almughlliq, FB; Koh, YQ; Peiris, HN; Vasvani, K.; Holande, O.; Meiers, S.; Roche, JR; Bērks, CR; Crookenden, MA; Arachchige, BJ; un citi. Cirkulējošās eksosomas var identificēt biomarķierus govīm, kurām ir vielmaiņas disfunkcijas risks. Sci. Rep. 2019, 9, 13879. [CrossRef]
11. Džans, RC; Du, WQ; Džans, Dž. Yu, SX; Lu, FZ; Ding, HM; Cheng, YB; Ren, C.; Geng, DQ Mezenhimālo cilmes šūnu ārstēšana perifēro nervu bojājumu gadījumā: stāstījuma pārskats. Neirāls Regēns. Res. 2021, 16, 2170–2176. [PubMed]
12. Bryzgunova, OE; Zaripovs, MM; Skvorcova, TE; Lekčnovs, EA; Grigorjeva, AE; Zaporožčenko, IA; Morozkins, ES; Rjabčikova, EI; Jurčenko, YB; Voitsitskis, VE; un citi. Ekstracelulāro pūslīšu salīdzinošs pētījums no veselu indivīdu un prostatas vēža slimnieku urīna. PLoS ONE 2016, 11, e0157566. [CrossRef] [PubMed]
13. Camussi, G.; Deregibus, MC; Bruno, S.; Greinžs, C.; Fonsato, V.; Tetta, C. Eksosomu/mikrovezikulu mediētā šūnu epiģenētiskā pārprogrammēšana. Am. J. Cancer Res. 2011, 1, 98–110. [PubMed]
14. Tamkovičs, SN; Tutanovs, OS; Laktionovs, PP Eksosomas: ģenerēšana, struktūra, transports, bioloģiskā aktivitāte un diagnostikas pielietojums. Biochem. Mosk. Suppl. Ser. Biedrs. Cell Biol. 2016, 10, 163–173. [CrossRef]
15. Bartel, DP MicroRNS: genomika, bioģenēze, mehānisms un funkcija. Cell 2004, 116, 281–297. [CrossRef]
16. Gordino, G.; Kosta-Pereira, S.; Korredeira, P.; Alvess, P.; Kosta, L.; Gomes, AQ; Silva-Santos, B.; Ribot, JC MicroRNA-181a ierobežo cilvēka δ T šūnu diferenciāciju, mērķējot uz Map3k2 un Notch2. EMBO Rep. 2022, 23, e52234. [CrossRef]
17. Liu, B.; Jans, L.; Čī, Y.; Saule, Y.; Yang, X. Gara nekodējoša RNS AFAP1-AS1 veicina olnīcu vēža progresēšanu, regulējot miR-107/PDK4 asi. J. Ovarian Res. 2021, 14, 60. [CrossRef]
18. Kima, Y.; Lī, DH; Parks, SH; Džeons, TI; Jung, CH MikroRNS un transkripcijas faktoru mijiedarbība autofagijas regulēšanā bezalkoholisko taukaino aknu slimību gadījumā. Exp. Mol. Med. 2021, 53, 548–559. [CrossRef]
19. Kazmierčaks, D.; Jopeks, K.; Šteržinska, K.; Novickis, M.; Ručinskis, M.; Januchowski, R. MikroRNS ekspresijas profils un iespējamā loma zāļu rezistentu gēnu regulēšanā cisplatīna un paklitaksela rezistentu olnīcu vēža šūnu līnijās. Int. J. Mol. Sci. 2022, 23, 526. [CrossRef]
20. Gongs, Y.; Vejs, X.; Saule, V.; Ren, X.; Čens, Dž.; Aveja, Dž. Ma, H.; Čans, KG; Džans, Y.; Li, S. Exosomal miR-224 veicina hemolimfas mikrobiotas homeostāzi bakteriālas infekcijas laikā vēžveidīgajiem. PLoS Patogs. 2021, 17, e1009837. [CrossRef]
21. Čens, Y.; Kou, V.; Žu, D.; Yu, X.; Zhu, Y. Nākotnes virzieni virsnieru garozas karcinomas diagnostikā, prognozēšanā un slimību uzraudzībā: jauni neinvazīvi biomarķieri. Priekšpuse. Endokrinols. 2022, 12, 811293. [CrossRef] [PubMed]
22. Gallo, A.; Tandons, M.; Alevizos, I.; Illei, GG Lielākā daļa serumā un siekalās nosakāmo mikroRNS ir koncentrētas eksosomās. PLoS ONE 2012, 7, e30679. [CrossRef] [PubMed]
23. Fans, B.; Šops, M.; Džans, ZG; Liu, XS Jaunās mikroRNS lomas kā diabētiskās neiropātijas biomarķieru un terapeitisko mērķu loma. Priekšpuse. Neirol. 2020, 11, 558758. [CrossRef] [PubMed]
24. Vejs, H.; Čens, K.; Līns, L.; Ša, C.; Li, T.; Liu, Y.; Iņ, X.; Sju, Y.; Čens, L.; Gao, V.; un citi. Eksosomu ražošanas un kravu šķirošanas regulēšana. Int. J. Biol. Sci. 2021, 17, 163–177. [CrossRef]
25. Jia, X.; Bi, Y.; Li, J.; Xie, Q.; Jans, H.; Liu, W. Cellular microRNA miR-26a nomāc cūku reproduktīvā un respiratorā sindroma vīrusa replikāciju, aktivizējot iedzimto pretvīrusu imunitāti. Sci. Rep. 2015, 5, 10651. [CrossRef]
26. Li, L.; Vejs, Z.; Džou, Y.; Dzjans, Y.; Jū, L.; Džens, H.; Tongs, V.; Jans, S.; Džens, H.; Šans, T.; un citi. Saimnieks miR-26a nomāc cūku reproduktīvā un respiratorā sindroma vīrusa replikāciju, pārregulējot I tipa interferonus. Virus Res. 2015, 195, 86–94. [CrossRef]
27. Liu, F.; Van, H.; Du, L.; Vejs, Z.; Džans, K.; Feng, WH MicroRNA-30c ir vērsta uz interferona-alfa/beta receptoru beta ķēdi, lai veicinātu 2. tipa PRRSV infekciju. J. ģenerālis Virols. 2018, 99, 1671–1680. [CrossRef]
28. Džans, K.; Huangs, C.; Yang, Q.; Gao, L.; Liu, HC; Tangs, Dž.; Feng, WH MicroRNA-30c modulē I tipa IFN reakcijas, lai atvieglotu cūku reproduktīvā un respiratorā sindroma vīrusa infekciju, mērķējot uz JAK1. J. Immunol. 2016, 196, 2272–2282. [CrossRef]
29. Van, D.; Cao, L.; Sju, Z.; Fangs, L.; Džons, Y.; Čens, K.; Luo, R.; Čens, H.; Li, K.; Xiao, S. MiR-125b samazina cūku reproduktīvā un respiratorā sindroma vīrusa replikāciju, negatīvi regulējot NF-κB ceļu. PLoS ONE 2013, 8, e55838. [CrossRef]
30. Džans, Q.; Guo, XK; Gao, L.; Huangs, C.; Li, N.; Jia, X.; Liu, V.; Feng, WH MicroRNA-23 inhibē PRRSV replikāciju, tieši mērķējot uz PRRSV RNS un, iespējams, pārregulējot I tipa interferonus. Virusoloģija 2014, 450–451, 182–195. [CrossRef]
31. Vū, Dž.; Pengs, X; Džou, A.; Cjao, M.; Vu, H.; Sjao, H.; Liu, G.; Džens, X.; Džans, S.; Mei, S. MiR-506 inhibē PRRSV replikāciju MARC-145 šūnās, izmantojot CD151. Mol. Šūna. Biochem. 2014, 394., 275.–281. [CrossRef]
32. Gao, L.; Guo, XK; Van, L.; Džans, K.; Li, N.; Čens, XX; Van, Y.; Feng, WH MicroRNA 181 nomāc cūku reproduktīvā un respiratorā sindroma vīrusa (PRRSV) infekciju, mērķējot uz PRRSV receptoru CD163. J. Virols. 2013, 87, 8808–8812. [CrossRef]
33. Sjao, S.; Du, T.; Vangs, X.; NIH.; Jans, Y.; Li, N.; Džans, C.; Džans, A.; Gao, J.; Liu, H.; un citi. MiR-22 veicina cūku reproduktīvā un respiratorā sindroma vīrusa replikāciju, mērķējot uz saimniekfaktoru HO-1. Veterinārs. Microbiol. 2016, 192, 226–230. [CrossRef]
34. Sjao, S.; Vangs, X.; NIH.; Li, N.; Džans, A.; Liu, H.; Pū, F.; Sju, L.; Gao, J.; Džao, Q.; un citi. MikroRNS miR-24-3p veicina cūku reproduktīvā un respiratorā sindroma vīrusa replikāciju, nomācot hēma oksigenāzes-1 ekspresiju. J. Virols. 2015, 89, 4494–4503. [CrossRef]
35. Batlers, JE; Sinkora, M.; Van, G.; Stepanova, K.; Li, Y.; Cai, X. Timocītu attīstības traucējumi ir PRRS pandēmijas pamatā: pārbaudāma hipotēze. Priekšpuse. Immunol. 2019, 10, 1077. [CrossRef]
36. Džou, L.; Van, Z.; Dings, Y.; Stepanova, K.; Li, Y.; Cai, X. NADC{1}}līdzīgs cūku reproduktīvā un respiratorā sindroma vīrusa celms, Ķīna. Emerg. Inficējiet. Dis. 2015, 21, 2256–2257. [CrossRef]
37. Džou, L.; Jans, B.; Sju, L.; Jin, H.; Ge, X.; Guo, X.; Han, J.; Yang, H. Trīs modificētu dzīvu vīrusu vakcīnu efektivitātes novērtējums pret cūku reproduktīvā un respiratorā sindroma vīrusa NADC30- celmu. Veterinārs. Microbiol. 2017., 207., 108.–116. [CrossRef]
38. Vongs, N.; Wang, X. miRDB: tiešsaistes resurss mikroRNS mērķa prognozēšanai un funkcionālām anotācijām. Nucleic Acids Res. 2015, 43, D146–D152. [CrossRef]
39. Frīdlenders, MR; Makovjaka, SD; Li, N.; Čens, V.; Rajewsky, N. miRDeep2 precīzi identificē zināmus un simtiem jaunu mikroRNS gēnu septiņos dzīvnieku klados. Nucleic Acids Res. 2012, 40, 37–52. [CrossRef]
40. Veņs, M.; Shen, Y.; Ši, S.; Tang, T. miREvo: Integratīva mikroRNS evolūcijas analīzes platforma nākamās paaudzes sekvencēšanas eksperimentiem. BMC Bioinform. 2012, 13, 140. [CrossRef]
41. Anderss, S.; Huber, W. Diferenciālās izteiksmes analīze secību skaitīšanas datiem. Genoms Biol. 2010, 11, R106. [CrossRef] [PubMed]
43. Tamura, K.; Štečers, G.; Kumar, S. MEGA11: Molekulārās evolūcijas ģenētikas analīzes versija 11. Mol. Biol. Evol. 2021, 38, 3022–3027. [CrossRef] [PubMed]
43. Hubišs, MJ; Pollards, KS; Siepel, A. PHAST un RPHAST: Filoģenētiskā analīze ar telpas/laika modeļiem. Īsumā. Bioinform. 2011, 12, 41–51. [CrossRef] [PubMed]
44. Krīgers, J.; Rehmsmeier, M. RNAhibrīds: mikroRNS mērķa prognozēšana vienkārša, ātra un elastīga. Nucleic Acids Res. 2006, 34, W451–W454. [CrossRef]
45. Yu, G.; Vangs, LG; Han, Y.; Viņš, QY clusterProfiler: R pakotne gēnu klasteru bioloģisko tēmu salīdzināšanai. OMIKS 2012, 16, 284–287. [CrossRef]
46. Kve, R.; Dings, G.; Čens, Dž.; Cao, L. Seruma eksosomālo mikroRNS un pacientu ar aizkuņģa dziedzera adenokarcinomu klīnisko patoloģisko pazīmju analīze. Pasaules J. Surg. Oncol. 2013, 11, 219. [CrossRef]
47. Théry, C.; Witwer, KW; Aikava, E.; Alkarass, MJ; Andersons, Dž. Andriantsitohaina, R.; Antoniou, A.; Arābs, T.; Arčers, F.; Atkins-Smits, GK; un citi. Minimālā informācija ārpusšūnu pūslīšu pētījumiem 2018 (MISEV2018): Starptautiskās ārpusšūnu pūslīšu biedrības nostājas paziņojums un MISEV2014 vadlīniju atjauninājums. J. Extracell. Vesicles 2018, 7, 1535750. [CrossRef]
48. Liū, K.-S.; Choi, JY; Hāns, TW; Parks, KT; Kim, HK Vakcinācijas ar modificētu dzīvu cūku reproduktīvo un respiratorā sindroma vīrusa vakcīnu ietekme uz nobarojamo cūku augšanas veiktspēju lauka apstākļos. J. Vet. Med. Sci. 2016, 78, 1533–1536. [CrossRef]
49. Bjans, T.; Saule, Y.; Hao, M.; Džou, L.; Ge, X.; Guo, X.; Han, J.; Yang, H. Rekombinants 2. tipa cūku reproduktīvā un respiratorā sindroma vīruss starp NADC30-līdzīgo un MLV līdzīgu: ģenētiskais raksturojums un patogenitāte sivēniem. Inficējiet. Genet. Evol. 2017, 54, 279–286. [CrossRef]
50. Li, Y.; Dži, G.; Van, Dž.; Tan, F.; Džuans, Dž.; Li, X.; Tian, K. NADC pilnīga genoma secība{1}}Tāpat kā cūku reproduktīvā un respiratorā sindroma vīruss, kam raksturīga rekombinācija ar citiem celmiem. Genoms Announc. 2016, 4, e00330-16. [CrossRef]
51. Kalluri, R.; Lebleu, VS Eksosomu bioloģija, funkcijas un biomedicīnas pielietojumi. Zinātne 2020, 367, eaau6977. [CrossRef] [PubMed]
52. Miao, XY Nesenie sasniegumi, lai izprastu miRNS lomu eksosomās un to terapeitisko potenciālu. J. Integr. Lauksaimniecības. 2017, 16, 753–761. [CrossRef]
53. Šenoda, BB; Ajit, SK Imūnās atbildes modulācija ar eksosomām, kas iegūtas no antigēnu prezentējošām šūnām. Clin. Med. Insights Pathol. 2016, 9 (S1 papildinājums), CPath-S39925. [CrossRef] [PubMed]
54. Li, S.; Li, S.; Vu, S.; Chen, L. Exosomes modulē vīrusa replikāciju un saimniekorganisma imūnās atbildes HBV infekcijā. BioMed Res. Int. 2019, 2019, 2103943. [CrossRef]
55. Apzaļumošana, DW; Gopal, SK; Sju, R.; Simpsons, RJ; Chen, W. Eksosomas un to loma imūnsistēmas regulēšanā un vēzis. Semināros šūnu un attīstības bioloģijā; Akadēmiskā prese: Kembridža, MA, ASV, 2015; 40.sējums, 72.–81.lpp.
56. Havits, Dž. Hill, AF Eksosomas neirodeģeneratīvo slimību patoloģijā. J. Biol. Chem. 2016, 291, 26589–26597. [CrossRef]
57. Ribeiro, MF; Žu, H.; Millard, RW; Fan, G. Eksosomas darbojas pro- un anti-angioģenēzē. Curr. Angiogenesis 2013, 2, 54–59. [CrossRef]
58. Lan, J.; Saule, L.; Sju, F.; Liu, L.; Hu, F.; Dziesma, D.; Hou, Z.; Vu, V.; Luo, X.; Van, Dž.; un citi. No M2 makrofāgiem iegūtās eksosomas veicina šūnu migrāciju un invāziju resnās zarnas vēža gadījumā. Cancer Res. 2019, 79., 146.–158. [CrossRef]
59. Aga, M.; Bentz, GL; Raffa, S.; Torisi, MR; Kondo, S.; Vakisaka, N.; Jošizaki, T.; Pagano, JS; Shackelford, J. Exosomal HIF1 atbalsta ar nazofaringeālu karcinomu saistīto LMP1-pozitīvo eksosomu invazīvo potenciālu. Onkogēns 2014, 33, 4613–4622. [CrossRef]
60. Fu, M.; Vangs, B.; Čens, X.; Viņš, Z.; Van, Y.; Li, X.; Cao, H.; Zheng, SJ gga-miR-454 nomāc infekciozās bursālās slimības vīrusa (IBDV) replikāciju, tieši mērķējot uz IBDV genoma segmentu B un citokīnu signalizācijas 6 (SOCS6) šūnu supresoriem. Virus Res. 2018., 252., 29.–40. [CrossRef]
61. Fu, M.; Vangs, B.; Čens, X.; Viņš, Z.; Van, Y.; Li, X.; Cao, H.; Zheng, SJ MicroRNA gga-miR-130b nomāc infekciozās bursālās slimības vīrusa replikāciju, mērķējot uz vīrusa genomu un citokīnu signalizācijas šūnu nomācējiem 5. J. Virol. 2018, 92, e01646-17. [CrossRef]
63. Guo, XK; Džans, K.; Gao, L.; Li, N.; Čens, XX; Feng, WH MikroRNS 181 ekspresijas palielināšana kavē cūku reproduktīvā un respiratorā sindroma vīrusa replikāciju un ietekmē vīrusu infekcijas kontroli. J. Virols. 2013, 87, 1159–1171. [CrossRef] [PubMed]
63. Cong, P.; Sjao, S.; Čens, Y.; Van, L.; Gao, J.; Li, M.; Viņš, Z.; Guo, Y.; Džao, G.; Džans, X.; un citi. Cūku alveolāro makrofāgu (PAM šūnu) integrētie miRNS un mRNS transkripti identificē celmam specifiskus miRNS molekulāros parakstus, kas saistīti ar H-PRRSV un N-PRRSV infekciju. Mol. Biol. Rep. 2014, 41, 5863–5875. [CrossRef] [PubMed]
64. Li, N.; Huangs, K.; Čens, Y.; Huangs, Z.; Džans, Y.; Lengs, C.; Liu, Y.; Ši, J.; Sjao, S.; Yao, L. MicroRNA ssc-miR-124a uzrāda pretvīrusu aktivitāti pret cūku reproduktīvo un respiratorā sindroma vīrusu, nomācot saimniekgēnus CD163. Veterinārs. Microbiol. 2021, 261, 109216. [CrossRef] [PubMed]
65. Li, N.; Du, T.; Jans, Y.; Džans, A.; Gao, J.; Hou, G.; Sjao, S.; Džou, EM MicroRNA let-7f-5p inhibē cūku reproduktīvā un respiratorā sindroma vīrusu, mērķējot uz MYH9. Sci. Rep. 2016, 6, 34332. [CrossRef]
66. Džens, Y.; Van, F.; Liangs, V.; Liu, J.; Gao, G.; Van, Y.; Sju, X.; Su, Q.; Džans, K.; Liu, B. Atšķirīgi izteiktas nekodējošas RNS identificēšana cūku alveolārajos makrofāgos no Tongcheng un lielām baltajām cūkām reaģēja uz PRRSV. Sci. Rep. 2018, 8, 15621. [CrossRef]
67. Džou, X.; Mihals, Dž. Dzjans, Z.; Liu, B. MikroRNS ekspresijas profilēšana vietējo ķīniešu Tongcheng cūku alveolārajos makrofāgos, kas inficētas ar PRRSV in vivo. J. Appl. Genet. 2017, 58, 539–544. [CrossRef]
68. Lī, YJ; Lee, C. Cūku reproduktīvā un respiratorā sindroma vīrusa replikācija tiek nomākta, inhibējot ārpusšūnu signālu regulētās kināzes (ERK) signalizācijas ceļu. Virus Res. 2010, 152, 50–58. [CrossRef]
69. Dziesma, S.; Bi, J.; Vangs, D.; Fangs, L.; Džans, L.; Li, F.; Čens, H.; Xiao, S. Cūku reproduktīvā un respiratorā sindroma vīrusa infekcija aktivizē IL-10 ražošanu, izmantojot NF-κB un p38 MAPK ceļus cūku alveolārajos makrofāgos. Izstrādātājs Comp. Immunol. 2013, 39., 265.–272. [CrossRef]
70. Iņ, S.; Huo, Y.; Dongs, Y.; Fan, L.; Jans, H.; Van, L.; Ning, Y.; Hu, H. C-Jun NH (2)-termināla kināzes aktivizēšana ir nepieciešama cūku reproduktīvajai un respiratorā sindroma vīrusa izraisītai apoptozei, bet ne vīrusa replikācijai. Virus Res. 2012, 166., 103.–108. [CrossRef]
71. Fan, L. Signalizācijas ceļi, kas iesaistīti apoptozes indukcijas regulēšanā saimniekšūnās pēc PRRSV infekcijas. Virus Genes 2019, 55, 433–439. [CrossRef]
72. Lopesa-Fuertesa, L.; Kamposs, E.; Domeneks, N.; Ezkerra, A.; Kastro, Dž. M.; Domingess, Dž.; Alonso, F. Cūku reproduktīvā un respiratorā sindroma (PRRS) vīruss samazina TNF veidošanos inficētos makrofāgos. Virus Res. 2000, 69, 41–46. [CrossRef]
73. Teissier, É.; Pécheur, EI Lipīdi kā vīrusu saplūšanas proteīnu mediētas membrānas saplūšanas modulatori. Eiro. Biophys. J. 2007, 36, 887–899. [CrossRef]
74. Džeons, JH; Lee, C. Cellular holesterīns ir nepieciešams cūku nidovīrusa infekcijai. Arch. Virol. 2017, 162, 3753–3767. [CrossRef]
75. Saule, Y.; Sjao, S.; Vangs, D.; Luo, R.; Li, B.; Čens, H.; Fang, L. Šūnu membrānas holesterīns ir nepieciešams cūku reproduktīvā un respiratorā sindroma vīrusa iekļūšanai un izdalīšanai MARC-145 šūnās. Sci. Ķīna Life Sci. 2011, 54, 1011–1018. [CrossRef]
76. Tjans, T.; Zhu, YL; Džou, YY; Liang, GF; Vanga, YY; Hu, FH; Xiao, ZD Eksosomu uzņemšana ar klatrīna izraisītu endocitozi un makropinocitozi un starpniecību miR-21. J. Biol. Chem. 2014, 289, 22258–22267. [CrossRef]
77. Mulkahi, LA; Rozā, RC; Kārters, DRF Ekstracelulāro pūslīšu uzņemšanas ceļi un mehānismi. J. Extracell. Vesicles 2014, 3, 24641. [CrossRef]
78. Džans, M.; Zang, X.; Vangs, M.; Li, Z.; Cjao, M.; Hu, H.; Chen, D. Uz eksosomām balstīti nanonesēji kā bioloģiski iedvesmoti un daudzpusīgi transportlīdzekļi zāļu piegādei: jaunākie sasniegumi un izaicinājumi. J. Mater. Chem. B 2019, 7, 2421–2433. [CrossRef]
